在0.1mol·L-1 CH3COOH溶液中存在如下电离平衡:
 CH3COOH CH3COO-+H+对于该平衡,下列叙述正确的是()
CH3COOH CH3COO-+H+对于该平衡,下列叙述正确的是()
| A.加入水时,平衡向逆反应方向移动 |
| B.加入少量NaOH固体,平衡向正反应方向移动 |
| C.加入少量0.1mol.L-1 HCl溶液,溶液中c(H+)减小 |
| D.加入少量CH3COONa固体,平衡向正反应方向移动 |
pH相同的盐酸和醋酸两种溶液中,它们的()
| A.H+的物质的量相同 | B.物质的量浓度相同 |
| C.H+的物质的量浓度不同 | D.H+的物质的量浓度相同 |
某一元弱酸HA的相对分子质量为M。在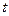 ℃时,将
℃时,将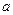 g HA完全溶解于水,得V mL饱和溶液,测得该溶液的密度为
g HA完全溶解于水,得V mL饱和溶液,测得该溶液的密度为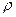 g·cm
g·cm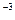 ,其中n(A
,其中n(A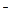 )为b mol。下列叙述中错误的是
)为b mol。下列叙述中错误的是
A.溶液中c(H+)=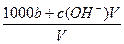
B.物质的量浓度c(HA)=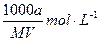
C.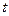 ℃时,HA的溶解度S
℃时,HA的溶解度S g
g
D.HA的质量分数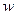 (HA)=
(HA)=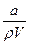 ×100%
×100%
一定温度下,氢氧化镁饱和溶液中存在如下关系:c(Mg2+)·[c(OH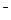 )]2=KSP,其中KSP为常数,称为该温度下Mg(OH)2的溶度积常数。试推断氢氧化镁在下列物质中的溶解度由大到小的顺序是
)]2=KSP,其中KSP为常数,称为该温度下Mg(OH)2的溶度积常数。试推断氢氧化镁在下列物质中的溶解度由大到小的顺序是
①0.1mol·L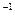 AlCl3溶液 ②0.1mol·L
AlCl3溶液 ②0.1mol·L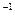 NH4C1溶液
NH4C1溶液
③0.1mol·L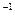 KCl溶液 ④0.1mol·L
KCl溶液 ④0.1mol·L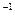 KAlO2溶液
KAlO2溶液
| A.①④③② | B.①②③④ | C.③①④② | D.④①③② |
(Ⅰ)常温下,将某一元酸HA(甲、乙、丙、丁代表不同的一元酸)和NaOH溶液等体积混合,两种溶液的物质的量浓度和混合溶液的pH如下表所示:
| 实验编号 |
HA的物质的量 浓度(mol·L-1) |
NaOH的物质的量 浓度(mol·L-1) |
混合后 溶液的pH |
| 甲 |
0.1 |
0.1 |
pH=a |
| 乙 |
0.12 |
0.1 |
pH=7 |
| 丙 |
0.2 |
0.1 |
pH>7 |
| 丁 |
0.1 |
0.1 |
pH=10 |
(1)从甲组情况分析,如何判断HA是强酸还是弱酸? ▲ 。
(2)乙组混合溶液中离子浓度c(A—)和c(Na+)的大小关系是 ▲ 。
A.前者大 B. 后者大 C. 二者相等 D.无法判断
(3)从丙组实验结果分析,该混合溶液中离子浓度由大到小的顺序是 ▲ 。
(4)分析丁组实验数据,写出该混合溶液中下列算式的精确结果(列式):
c(Na+)—c(A-)= ▲ mol·L-1
(Ⅱ)某二元酸(化学式用H2B表示)在水中的电离方程式是:
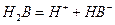

回答下列问题:
(5)在0.1mol/L的Na2B溶液中,下列粒子浓度关系式正确的是 ▲ 。
A.c( B2—)+c(HB—)=0.1mol/L B.c( B2—)+ c(HB—)+c(H2B)=0.1mol/L
C c(OH—)=c(H+)+ c(HB—) D.c(Na+)+c(OH)=c(H+)+ c(HB—)
已知H2B在水溶液中存在以下电离:

 一级电离:H2B H++HB-,二级电离:HB- H++B2-
一级电离:H2B H++HB-,二级电离:HB- H++B2-
请回答以下问题:
(1)NaHB溶液 (填“呈酸性”、“呈碱性”或“无法确定”),原因是
。
(2)若0.1mol·L-1的H2B溶液在某温度下的pH=3,c(B2-)=1×10-6mol·L-1,则H2B的一级电离的电离度为 。
(3)某温度下,在0.1mol·L-1的NaHB溶液中,以下关系一定不正确的是 ( )
A.c(H+)·c(OH-)=1×10-14
B.pH>1
C.c(OH-)=2c(H2B)+c(HB-)+c(H+)
D.c(Na+)=0.1mol·L-1≥c(B2-)
|
 (4)某温度下,FeB(s) Fe2+(aq)+B2-(aq)
(4)某温度下,FeB(s) Fe2+(aq)+B2-(aq)
下列溶液一定呈中性的是 ( )
| A.pH=7的溶液 |
| B.c(NH4+)=c(Cl-)的NH4Cl和氨水的混合溶液 |
| C.PH=2的CH3COOH和PH=12的NaOH溶液等体积混合 |
| D.CH3COONa溶液 |
(Ⅰ)常温下,将某一元酸HA(甲、乙、丙、丁代表不同的一元酸)和NaOH溶液等体积混合,两种溶液的物质的量浓度和混合溶液的pH如下表所示:
| 实验编号 |
HA的物质的量 浓度(mol·L-1) |
NaOH的物质的量 浓度(mol·L-1) |
混合后 溶液的pH |
| 甲 |
0.1 |
0.1 |
pH=a |
| 乙 |
0.12 |
0.1 |
pH=7 |
| 丙 |
0.2 |
0.1 |
pH>7 |
| 丁 |
0.1 |
0.1 |
pH=10 |
(1)从甲组情况分析,如何判断HA是强酸还是弱酸? ▲ 。
(2)乙组混合溶液中离子浓度c(A—)和c(Na+)的大小关系是 ▲ 。
A.前者大 B. 后者大 C. 二者相等 D.无法判断
(3)从丙组实验结果分析,该混合溶液中离子浓度由大到小的顺序是 ▲ 。
(4)分析丁组实验数据,写出该混合溶液中下列算式的精确结果(列式):
c(Na+)—c(A-)= ▲ mol·L-1
(Ⅱ)某二元酸(化学式用H2B表示)在水中的电离方程式是:
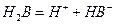

回答下列问题:
(5)在0.1mol/L的Na2B溶液中,下列粒子浓度关系式正确的是 ▲ 。
A.c( B2—)+c(HB—)=0.1mol/L B.c( B2—)+ c(HB—)+c(H2B)=0.1mol/L
C c(OH—)=c(H+)+ c(HB—) D.c(Na+)+c(OH)=c(H+)+ c(HB—)
下列有关溶液的叙述正确的是
| A.常温下的醋酸铵溶液呈中性,则溶液中c(H+)=c(OH-)=10-7mol·L-1 |
| B.在pH=2的醋酸溶液中加入等体积c(酸)=2mol·L-1的某酸溶液后,混合溶液的pH一定会减小 |
| C.pH相同的醋酸溶液和盐酸,分别用蒸馏水稀释至原溶液的m倍和n倍,若稀释后两溶液的pH仍相同,则m>n |
| D.导电性强的溶液中自由移动离子数目一定比导电性弱的溶液中自由移动离子数目多 |
常温下,有甲、乙两份体积均为1 L、浓度均为0.1 mol/L的氨水,其pH为11。①甲用蒸馏水稀释100倍后,溶液的pH变为a;②乙与等体积、浓度为0.2 mol/L的盐酸混合,在混合溶液中:n(NH4+ )+n(H+)-n(OH-) =" b" mol。则a、b正确的答案组合是
| A.9~11之间;0.1 | B.9~11之间;0.2 |
| C.12~13之间;0.2 | D.13;0.1 |
把氢氧化钙放入蒸馏水中,一定时间后达到如下平衡:
Ca(OH)2(s)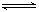 Ca2++2OH- 加入以下溶液,可使Ca(OH)2减少的是
Ca2++2OH- 加入以下溶液,可使Ca(OH)2减少的是
| A.Na2S溶液 | B.AlCl3溶液 | C.NaOH溶液 | D.CaCl2溶液 |
在下列叙述中,能说明盐酸是强酸,醋酸是弱酸的是( )
| A.将pH=4的盐酸和醋酸稀释成pH=5的溶液,醋酸所需加入的水量多 |
| B.盐酸和醋酸都可用相应的钠盐与浓硫酸反应制取 |
| C.相同pH的盐酸和醋酸溶液中分别加入相应的钠盐固体,醋酸的pH变大 |
| D.相同pH的盐酸和醋酸分别跟锌反应时,产生氢气的起始速率相等 |
草酸是二元弱酸,草酸氢钾溶液呈酸性,在0.1mol/LKHC2O4溶液中,下列关系正确的是( )
| A.c(K+)+c(H+)=c(HC2O4-)+c(OH-)+ c(C2O42-) | B.c(HC2O4-)+ c(C2O42-)=0.1mol/L |
| C.c(C2O42-)>c(H2C2O4) | D.c(K+)= c(H2C2O4)+ c(HC2O4-)+ c(C2O42-) |
已知室温时,0.1某一元酸HA在水中有0.1
发生电离,下列叙述错误的是:()

| A. |
该溶液的 |
| B. |
升高温度,溶液的 |
| C. |
此酸的电离平衡常数约为1×10-7 |
| D. |
由 |
试题篮
()