用水稀释0.1mol· L-1的醋酸溶液,下列说法正确的是
| A.醋酸的电离程度逐渐增大,溶液的PH值减小 |
| B.Kw逐渐减小 |
| C.水的电离程度增大 |
D. 变大 变大 |
在一定温度下,向2L体积固定的密闭容器中加入1molHI,2HI H2(g)+I2(g)△H>0,H2的物质的量随时间的变化如图示,下列说法正确有是
H2(g)+I2(g)△H>0,H2的物质的量随时间的变化如图示,下列说法正确有是
A.该温度下,反应的平衡常数是 |
| B.0~2min内的HI的平均反应速率为0.05mol·L-1·min-1 |
| C.恒压下向该体系中加入N2,平衡不移动,反应速率不变 |
| D.升高温度,平衡向正反应方向移动,只有正反应速率加快 |
I2在KI溶液中存在下列平衡:I2(aq)+I-(aq) I3-(aq), 某I2、KI混合溶液中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法正确的是( )
I3-(aq), 某I2、KI混合溶液中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法正确的是( ) 
A.反应 I2(aq)+I-(aq) I3-(aq)的 △H>0 I3-(aq)的 △H>0 |
| B.若温度为T1、T2时,反应平衡常数分别为K1、K2,则K2>K1 |
| C.若反应进行到状态D时,一定有v正>v逆 |
| D.状态A与状态B相比,状态A的c(I2)大 |
在一定温度条件下,甲、乙两个容积相等的恒容密闭容器中均发生如下反应:
3A(g)+B(g) xC(g)+D(s),向甲中通入6molA和2molB,向乙中通入1.5molA、0.5molB和3molC、2molD,反应一段时间后都达到平衡,此时测得甲、乙两容器中C的体积分数都为0.2,下列叙述中正确的是 ( )
A.若平衡时,甲、乙两容器中A的物质的量相等,则x=4
B.平衡时,甲、乙两容器中A、B的物质的量之比不相等
C.平衡时甲中A的体积分数为0.4
D.若平衡时两容器中的压强不相等,则两容器中压强之比8:5
可逆反应A(s)+B(g)
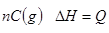 (n为正整数)在不同条件下反应混合物中C的百分含量和反应过程所需时间的关系曲线如右图所示。下列有关叙述中一定正确的是
(n为正整数)在不同条件下反应混合物中C的百分含量和反应过程所需时间的关系曲线如右图所示。下列有关叙述中一定正确的是
A.其他条件相同,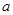 表示使用了催化剂, 表示使用了催化剂,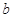 没有使用催化剂 没有使用催化剂 |
B.其他条件相同,若只改变压强,则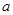 比 比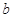 的压强大且 的压强大且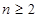 |
C.其他条件相同,若只改变温度,则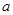 比 比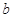 的温度高且Q>0 的温度高且Q>0 |
D.其他条件相同,若改变A的物质的量,则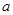 比 比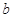 消耗A的物质的量少 消耗A的物质的量少 |
高温下,反应 2HBr(g) H2(g) + Br2(g) (正反应为吸热反应) 达到化学平衡时,要使混合气体的颜色加深,可采取的方法是( )
H2(g) + Br2(g) (正反应为吸热反应) 达到化学平衡时,要使混合气体的颜色加深,可采取的方法是( )
| A.减小压强 | B.缩小体积 |
| C.降低温度 | D.增大氢气的浓度 |
在一定条件下,反应A(g)+2B(g) 3C(g)达到平衡的标志是:( )
3C(g)达到平衡的标志是:( )
A.容器内压强不再变化
B.单位时间内生成nmolA同时生成2nmolB
C.A、B、C浓度不再变化
D.A、B、C的分子数之比为1:2:3
某温度下在密闭容器中发生如下反应:2M(g)+ N(g)  2G(g)若开始时只充入2molG(g),达平衡时,混合气体的压强比起始时增加20%,若开始时只充入2molM和1molN的混合气体,达平衡时M的转化率为
2G(g)若开始时只充入2molG(g),达平衡时,混合气体的压强比起始时增加20%,若开始时只充入2molM和1molN的混合气体,达平衡时M的转化率为
| A.20% | B.40% | C.60% | D.80% |
下列反应达到平衡后,加压或升温,平衡都向正反应方向移动的是( )
A.2NO2(g) N2O4(g) △H<0 N2O4(g) △H<0 |
B.3O2(g) 2O3(g)△H>0 2O3(g)△H>0 |
C.H2(g)+I2(g) 2HI(g)△H<0 2HI(g)△H<0 |
D.NH4HCO3(s) NH3(g)+H2O(g)+CO2(g) △H>0 NH3(g)+H2O(g)+CO2(g) △H>0 |
把在空气中久置的铝片 5.0 g投入盛有500mL0.5mol·L-1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率v与反应时间t可用如右的坐标曲线来表示,下列推论错误的是
| A.t由0→a段不产生氢气是因为表面的氧化物隔离了铝和硫酸溶液 |
| B.t由b→c段产生氢气的速率增加较快的主要原因之一是温度升高 |
| C.t=c时反应处平衡状态 |
| D.t>c产生氢气的速率降低主要是因为溶液中c(H+)降低 |
已知高锰酸钾与重铬酸钾(K2Cr2O7)都是化学中常用的强氧化剂,高锰酸钾溶液呈紫红色而重铬酸钾溶液中存在如下平衡:
2CrO42-(黄色)+2H+ Cr2O72-(橙色)+H2O
Cr2O72-(橙色)+H2O
若要使溶液的橙色加深,下列可采用的方法是
| A.加入适量稀盐酸 | B.加入适量稀硝酸 |
| C.加入适量烧碱固体 | D.加水稀释 |
金属卤化物跟卤素化合可生成多卤化物,如:KI+I2 KI3,有关KI3的叙述中不正确的是
KI3,有关KI3的叙述中不正确的是
| A.I2在KI溶液中溶解度增大是由于生成I3-离子 |
B.I3-在溶液中存在下列平衡I3- I2+I- I2+I- |
| C.KI3溶液遇淀粉不变蓝色 |
| D.将Cl2通入KI3溶液中,I3-浓度减小 |
在1100℃,一定容积的密闭容器中发生反应:FeO(s)+CO(g) Fe(s)+CO2(g) △H=a kJ/mol(a >0),该温度下K=0.263,下列有关该反应的说法正确的是
Fe(s)+CO2(g) △H=a kJ/mol(a >0),该温度下K=0.263,下列有关该反应的说法正确的是
| A.若生成1 mol Fe,则吸收的热量小于a kJ |
| B.若升高温度,正反应速率加快,逆反应速率减慢,则化学平衡正向移动 |
| C.若容器内压强不随时间变化,则可以判断该反应已达到化学平衡状态 |
| D.达到化学平衡状态时,若c(CO)="0.100" mol/L,则c(CO2)="0.0263" mol/L |
可逆反应A(g) + B(g)  2C(g)在固定容积的密闭容器中进行。若向容器中充入1molA和1molB,在T℃达平衡时,C的体积分数为m%;若向容器中充入2molC,T℃达平衡时,C的体积分数为n%;若向容器中充入1molC,T℃达平衡时,C的体积分数为p%。则m、n、p的关系是
2C(g)在固定容积的密闭容器中进行。若向容器中充入1molA和1molB,在T℃达平衡时,C的体积分数为m%;若向容器中充入2molC,T℃达平衡时,C的体积分数为n%;若向容器中充入1molC,T℃达平衡时,C的体积分数为p%。则m、n、p的关系是
| A.m =" n" = p | B.n > p >m | C.m =" n" > p | D.n > m >p |
已知某可逆反应aA(g) + bB(g)  cC(g) + dD(g)。反应过程中,当其它条件不变时,C的体积分数与温度(T)和压强(P)的关系如图。下列叙述正确的
cC(g) + dD(g)。反应过程中,当其它条件不变时,C的体积分数与温度(T)和压强(P)的关系如图。下列叙述正确的
| A.正反应为吸热反应 | B.降低温度,正反应速率增大 |
| C.a + b < c + d | D.增大压强,B转化率增大 |
试题篮
()