下列对各种平衡体系的叙述中,完全正确的一组是
① 在醋酸溶液中存在的电离平衡:CH3COOH CH3COO-+ H+,加水稀释后,溶液中所有离子浓度均减小
CH3COO-+ H+,加水稀释后,溶液中所有离子浓度均减小
② 常温下,在醋酸溶液中加入少量的CH3COONa固体,会使其电离平衡逆向移动
③ 某温度下,容积一定的密闭容器中进行可逆反应:X(g)+Y(g)  2Z(g) +W(s); △H>0平衡后,升高温度,该化学平衡正向移动
2Z(g) +W(s); △H>0平衡后,升高温度,该化学平衡正向移动
④在上述③的可逆反应中,当容器中气体压强不变时,反应达到平衡
⑤一定浓度的醋酸钠溶液可使酚酞试液变红,其原因是溶液中存在如下平衡
CH3COO-+ H2O CH3COOH + OH-使得溶液中的c (OH-)>c(H+)
CH3COOH + OH-使得溶液中的c (OH-)>c(H+)
⑥在碳酸钙的沉淀溶解平衡体系中,加入稀盐酸,平衡向溶解的方向移动
⑦在氯化银的沉淀溶解平衡体系中,加入碘化钾固体,氯化银沉淀可转化为碘化银沉淀
| A.①②③④⑤ | B.②③④⑤⑥ | C.②③⑤⑥⑦ | D.①②⑤⑥⑦ |
某温度下,在2L的密闭容器中,加入1molX(g)和2molY(g)发生反应:X(g)+m Y(g) 3Z(g),平衡时,X、Y、Z的体积分数分别为30%、60%、10%。在此平衡体系中再加入1molZ(g),再次达到平衡后,X、Y、Z的体积分数不变。下列叙述不正确的是( )
3Z(g),平衡时,X、Y、Z的体积分数分别为30%、60%、10%。在此平衡体系中再加入1molZ(g),再次达到平衡后,X、Y、Z的体积分数不变。下列叙述不正确的是( )
| A.m=2 |
| B.两次平衡的平衡常数相同 |
| C.第二次平衡时,Z的浓度为0.4 mol·L-1 |
| D.X与Y的平衡转化率之比为1:1 |
下列关于各图像的解释或结论正确的是

甲 乙 丙 丁
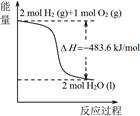
A.由甲可知:热化学方程式是H2(g) + O2(g) = H2O(g) △H=﹣241.8kJ/mol
O2(g) = H2O(g) △H=﹣241.8kJ/mol
B.由乙可知:对于恒温恒容条件下的反应2NO2(g) ⇌N2O4(g),A点为平衡状态
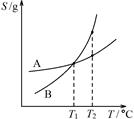
C.由丙可知:将A、B饱和溶液分别由T1℃升温至T2℃时,溶质的质量分数B>A
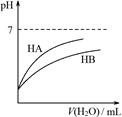
D.由丁可知:同温度、同浓度的NaA溶液与NaB溶液相比,其pH前者小于后者
T℃时,在2L的密闭容器中,A气体与B气体发生可逆反应生成C气体,反应过程中A、B、C物质的量变化如下图(Ⅰ)所示。若保持其它条件不变,温度分别为T1和T2时,B的物质的量分数与时间关系如下图(Ⅱ)所示。下列叙述正确的是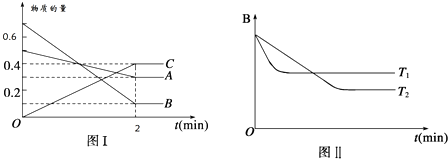
A.2min内A的化学反应速率为0.1 mol/(L•min)
B.在反应达平衡时,保持其他条件不变,增大压强,正逆反应速率都增大,且平衡向逆反应方向移动
C.在反应达平衡时,其他条件不变,升高温度,正逆反应速率都增大,且A的转化率增大
D.图(I)中,达平衡时,A的体积分数为37.5%
恒温恒容下,向2 L密闭容器中加入MgSO4(s)和CO(g),发生反应:
MgSO4(s)+CO(g) MgO(s)+CO2(g)+SO2(g)反应过程中测定的部分数据见下表:
MgO(s)+CO2(g)+SO2(g)反应过程中测定的部分数据见下表:
| 反应时间/min |
n(MgSO4)/mol |
n(CO)/mol |
n(SO2) / mol |
| 0 |
2.0 |
2.0 |
0 |
| 2 |
|
0.8 |
|
| 4 |
|
|
1.2 |
| 6 |
|
1.2 |
2.8 |
下列说法正确的是
A.0~2 min内的平均速率为υ(CO)=0.6 mol/(L·min)
B.4 min后,平衡移动的原因可能是向容器中加入了2.0 mol的SO2
C.若升高温度,反应的平衡常数变为1.0,则正反应为放热反应
D.其他条件不变,若起始时容器中MgSO4、CO均为1.0 mol,则平衡时n(SO2)="0.6" mol
可以充分说明反应P(g)+Q(g) R(g)+S(g)在恒温下已达到平衡的是( )
R(g)+S(g)在恒温下已达到平衡的是( )
| A.反应容器内的压强不随时间改变 |
| B.反应容器内P、Q、R、S四者浓度之比为1:1:1:1 |
| C.P的生成速率和S的生成速率相等 |
| D.反应容器内的气体总物质的量不随时间变化 |
在密闭容器中发生反应a X(气)+b Y(气) c W(气)+d Z(气),若反应达到平衡后,保持温度不变,将气体压缩到原来的1/2体积,再次达到平衡时,Z的浓度是原平衡的1.8倍,下列叙述中不正确的是( )
c W(气)+d Z(气),若反应达到平衡后,保持温度不变,将气体压缩到原来的1/2体积,再次达到平衡时,Z的浓度是原平衡的1.8倍,下列叙述中不正确的是( )
| A.平衡向逆反应方向移动 | B.a+b>c+d |
| C.W的体积分数减小 | D.X的转化率降低 |
298 K时,在2L固定体积的密闭容器中,发生可逆反应:2NO2(g)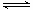 N2O4 (g) ΔH=-a kJ/mol (a>0) 。N2O4的物质的量浓度随时间变化如下图。达平衡时,N2O4的浓度为NO2的2倍,若反应在398K进行,某时刻测得n(NO2)="0.6" mol、n(N2O4)=1.2mol,则此时,下列大小关系正确的是
N2O4 (g) ΔH=-a kJ/mol (a>0) 。N2O4的物质的量浓度随时间变化如下图。达平衡时,N2O4的浓度为NO2的2倍,若反应在398K进行,某时刻测得n(NO2)="0.6" mol、n(N2O4)=1.2mol,则此时,下列大小关系正确的是

A. > >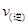 |
B. < <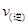 |
C. = =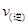 |
D. 、 、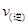 大小关系不确定 大小关系不确定 |
羰基硫(COS)可作为一种蚜虫熏蒸剂,能防止某些昆虫、线虫和蚜虫的危害。在恒容密闭容器中,将CO和H2S混合加热并达到下列平衡:CO(g)+H2S(g) COS(g)+H2(g) K=0.1,反应前CO的物质的量为10mol,平衡后CO物质的量为8mol,下列说法正确的是( )
COS(g)+H2(g) K=0.1,反应前CO的物质的量为10mol,平衡后CO物质的量为8mol,下列说法正确的是( )
| A.升高温度,H2S浓度增加,表明该反应是吸热反应 |
| B.通入CO后,正反应速率逐渐增大 |
| C.CO的平衡转化率为80% |
| D.反应前H2S物质的量为7mol |
在新制的氯水中存在平衡:Cl2+H2O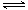 HCl+HClO。加入少量下列物质能使c(HClO)增大的是
HCl+HClO。加入少量下列物质能使c(HClO)增大的是
| A.CaCO3 | B.NaOH | C.CaSO3 | D.HCl |
对于已达到平衡状态的可逆反应:A+B C+D,若t1时增大压强,正、逆反应速率变化如图所示,下列有关A、B、C、D四种物质的状态叙述中正确的是( )
C+D,若t1时增大压强,正、逆反应速率变化如图所示,下列有关A、B、C、D四种物质的状态叙述中正确的是( )

A.A、B、C、D一定都是气体
B.A、B一定都是气体,C、D只有一种是气体
C.C、D一定都是气体,A、B只有一种是气体
D.C、D至少有一种是气体,A、B也至少有一种是气体
在温度、初始容积相同的两个密闭容器中,按不同方式投入反应物(如图所示),发生如下反应:3X(g)+Y(g)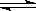 2Z(g)△H<0,保持温度不变,测得平衡时的有关数据如下:下列说法正确的是( )
2Z(g)△H<0,保持温度不变,测得平衡时的有关数据如下:下列说法正确的是( )
| |
恒容容器甲 |
恒压容器乙 |
| Y的物质的量/mol |
n1 |
n2 |
| Z的体积分数 |
φ1 |
φ2 |
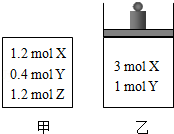
A.平衡时容器乙的容积一定比反应前大
B.平衡时容器甲的压强一定比反应前大
C.n2>n1
D.φ2>φ1
将0.5 mol SO2和0.2 mol O2置于密闭容器中发生反应:2SO2+O2 2SO3。下列关于该反应的说法正确的是
2SO3。下列关于该反应的说法正确的是
| A.最终可生成0.4 mol SO3 | B.当v正(O2)= v逆(SO2) = 0时一定达化学平衡 |
| C.升高温度反应速率减小 | D.缩小体积增大压强反应速率增大 |
某温度下,恒容密闭容器中发生如下可逆反应:2 E(g)  F(g) + x G(g)(正反应放热);若起始时E浓度为a mol/L,F、G浓度均为0,达平衡时E浓度为0.5amol/L,若E的起始浓度改为2amol/L,F、G 浓度仍为0,当达到新的平衡时,下列说法正确的是( )
F(g) + x G(g)(正反应放热);若起始时E浓度为a mol/L,F、G浓度均为0,达平衡时E浓度为0.5amol/L,若E的起始浓度改为2amol/L,F、G 浓度仍为0,当达到新的平衡时,下列说法正确的是( )
| A.升高温度时,正反应速率加快,逆反应速率减慢,平衡逆向移动 |
| B.若x=1,新平衡下E转化率为50% |
| C.若x=2,新平衡下F的平衡浓度为0.5a mol/L |
| D.若x=2,换成恒压容器,则达到平衡所需时间比恒容容器所需时间短 |
一定温度时,向容积为2L的密闭容器中充入一定量的SO2和O2,发生反应:2SO2(g)+O2(g) 2SO3(g) ∆H=−196kJ·moL−1,一段时间后达平衡,反应过程中测定的部分数据见下表:
2SO3(g) ∆H=−196kJ·moL−1,一段时间后达平衡,反应过程中测定的部分数据见下表:
| 反应时间/min |
n(SO2)/mol |
n(O2)/mol |
| 0 |
2 |
1 |
| 5 |
1.2 |
|
| 10 |
|
0.4 |
| 15 |
0.8 |
|
下列说法不正确的是
A.反应在前5min的平均速率为v (SO2)=0.08mol·L−1·min−1
B.保持温度不变,向平衡后的容器中再充入0.2molSO2和0.2mol SO3时,v (正)>v (逆)
C.保持其他条件不变,若起始时向容器中充入2molSO3,达平衡时吸收78.4kJ的热量
D.相同温度下,起始时向容器中充入1.5mol SO3,达平衡时SO3的转化率为40%
试题篮
()