相同温度下,容积相同的甲、乙、丙3个恒容密闭容器中发生可逆反应:2SO2(g)+O2(g) 2SO3(g);△H=-197kJ/mol。实验测得起始、平衡时的有关数据如下表:下列叙述正确的是
2SO3(g);△H=-197kJ/mol。实验测得起始、平衡时的有关数据如下表:下列叙述正确的是
| 器 |
起始各物质的物质的量/mol |
达到平衡时体系能量的变化 |
|||
| SO2 |
O2 |
SO3 |
Ar |
||
| 甲 |
2 |
1 |
0 |
0 |
放出热量:Q1 |
| 乙 |
1.8 |
0.9 |
0.2 |
0 |
放出热量:Q2 |
| 丙 |
1.8 |
0.9 |
0.2 |
0.1 |
放出热量:Q3 |
| 容器 |
起始各物质的物质的量/mol |
达到平衡时体系能量的变化 |
|||
| SO2 |
O2 |
SO3 |
Ar |
||
| 甲 |
2 |
1 |
0 |
0 |
放出热量:Q1 |
| 乙 |
1.8 |
0.9 |
0.2 |
0 |
放出热量:Q2 |
| 丙 |
1.8 |
0.9 |
0.2 |
0.1 |
放出热量:Q3 |
A.若在上述条件下反应生成2molSO3(s)的反应热为△H1,则△H1>-197 kJ·mol-1
B.Q1=Q2=Q3="197" kJ
C.甲、乙、丙3个容器中反应的平衡常数不相等
D.达到平衡时,丙容器中SO2的体积分数最大
一定条件下,在容积为10L的密闭容器中,将l mol X和1 mol Y进行如下反应:2X(g)+Y(g)  Z(g),经60 s达到平衡生成0.3 mol的Z,下列说法正确的是
Z(g),经60 s达到平衡生成0.3 mol的Z,下列说法正确的是
| A.60 s时Z的平衡浓度为0.03 mol/L |
| B.将容器容积变为20 L,Z的新平衡浓度将等于原平衡浓度的一半 |
| C.若温度和体积不变,往容器内增加1 mol Y,Y的转化率将增大 |
| D.若升高温度,X的体积分数增大,则正反应的△H>0 |
可逆反应2NO2 2NO+O2在体积固定的密闭容器中,达到平衡状态的标志是
2NO+O2在体积固定的密闭容器中,达到平衡状态的标志是
①单位时间内生成n mol O2的同时生成2n mol NO2
②单位时间内生成n mol O2的同时生成2n mol NO
③用NO2,NO,O2表示的反应速率的比为2:2:1的状态
④混合气体的颜色不再改变的状态
⑤混合气体的密度不再改变的状态
⑥混合气体的压强不再改变的状态
⑦混合气体的平均相对分子质量不再改变的状态
| A.①④⑥⑦ | B.②③⑤⑦ | C.①③④⑤ | D.全部 |
对平衡CO2(g) CO2(aq);△H =-19.75kJ/mol,为增大二氧化碳气体在水中的溶解度,应采用的方法是( )
CO2(aq);△H =-19.75kJ/mol,为增大二氧化碳气体在水中的溶解度,应采用的方法是( )
| A.升温增压 | B.降温减压 | C.升温减压 | D.降温增压 |
下面关于化学反应的限度的叙述中,正确的是
| A.化学反应的限度都相同 |
| B.可以通过改变温度控制化学反应的限度 |
| C.可以通过延长化学反应的时间改变化学反应的限度 |
| D.反应限度是无法改变的 |
密闭容器中,反应xA(g)+yB(g)  zC(g)达平衡时,A的浓度为0.5mol/L,若保持温度不变,将容器的容积扩大到原来的2倍,达新平衡时A的浓度降为0.3mol/L下列判断错误的是 ( )
zC(g)达平衡时,A的浓度为0.5mol/L,若保持温度不变,将容器的容积扩大到原来的2倍,达新平衡时A的浓度降为0.3mol/L下列判断错误的是 ( )
| A.x+y>z | B.平衡向正方向移动 |
| C.B的转化率降低 | D.C的体积分数下降 |
在一个不传热的固定容积的密闭容器中发生可逆反应:mA(g) + nB(g) ⇌pC(g) + qD(g) ,当m、n、p、q为任意整数(不为零)时,不能说明达到平衡状态的标志是
| A.D的质量不再改变 |
| B.各组分的浓度不再改变 |
| C.反应速率υA:υB:υC:υD=m:n:p:q |
| D.单位时间内m mol A断键发生反应,同时p mol C也断键发生反应 |
已知H2(g)+I2(g)  2HI(g) ΔH<0。有相同容积的定容密闭容器甲和乙,甲中加入H2和I2各0.1 mol,乙中加入HI 0.2 mol,在相同温度下分别达到平衡。现欲使甲中HI平衡时的百分含量大于乙中HI平衡时的百分含量,则应采取的措施是( )
2HI(g) ΔH<0。有相同容积的定容密闭容器甲和乙,甲中加入H2和I2各0.1 mol,乙中加入HI 0.2 mol,在相同温度下分别达到平衡。现欲使甲中HI平衡时的百分含量大于乙中HI平衡时的百分含量,则应采取的措施是( )
| A.甲中充入HI气体,乙中不变 | B.甲降低温度,乙增大压强 |
| C.甲中加入0.1 mol He,乙中不变 | D.甲增加0.1 mol H2,乙增加0.1 mol I2 |
在容积不变的密闭容器中,一定条件下发生反应:2A ⇌B(g)+2C(g),且达到平衡。当升高温度时气体的密度增大,则下列叙述中正确的是
| A.升高温度,正反应速率增大,逆反应速率减小 |
| B.若正反应是放热反应,则A为气态 |
| C.若向容器中充入惰性气体,则平衡向右移动 |
| D.物质A一定为非气态,且正反应是吸热反应 |
在2000K时,反应CO(g)+1/2O2(g)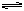 CO2(g)的平衡常数为K1,则相同温度下反
CO2(g)的平衡常数为K1,则相同温度下反
应2CO2(g)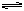 2CO(g)+O2(g)的平衡常数K2为( )
2CO(g)+O2(g)的平衡常数K2为( )
| A.1/K12 | B.K12 | C.1/K1 | D.K1-1/2 |
已知反应:2NO2(g)+4CO(g) N2(g)+4CO2(g) ΔH<0。将一定量的NO2与CO充入装有催化剂的注射器中后封口。右图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小)。下列说法不正确的是
N2(g)+4CO2(g) ΔH<0。将一定量的NO2与CO充入装有催化剂的注射器中后封口。右图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小)。下列说法不正确的是
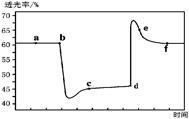
| A.b点的操作是快速压缩注射器 |
| B.c点与a点相比,c(NO2)、c(N2)都增大 |
C.e点: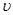 (正) < (正) <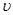 (逆) (逆) |
| D.若考虑体系温度变化,且没有能量损失,则平衡常数K(c) >K(f) |
一定温度下,反应2SO2+O2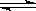 2SO3,达到平衡时,n (SO2):n(O2):n(SO3)=2:3:4。缩小体积,反应再次达到平衡时,n(O2)="0.8" mol,n(SO3)="1.4" mol,此时SO2的物质的量应是
2SO3,达到平衡时,n (SO2):n(O2):n(SO3)=2:3:4。缩小体积,反应再次达到平衡时,n(O2)="0.8" mol,n(SO3)="1.4" mol,此时SO2的物质的量应是
| A.1.2 mol | B.0.8 mol | C.0.6 mol | D.0.4 mol |
下列变化不能用勒夏特列原理解释的是
| A.红棕色的NO2气体加压后颜色先变深再变浅 |
| B.H2、I2、HI混合气体加压后颜色变深 |
| C.二氧化硫转化为三氧化硫时增加空气的量以提高二氧化硫的转化率 |
| D.打开汽水瓶,看到有大量的气泡逸出 |
某温度时,在一个容积为2 L的密闭容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示,根据图中数据,下列有关说法错误的是( )
| A.该反应的化学方程式为3X+Y===2ZA |
| B.2 min时,反应达最大限度,但化学反应仍在进行 |
| C.反应开始至2 min,Z的反应速率为0.10 mol·L-1·min-1 |
| D.反应达到平衡时,压强是开始时的0.9倍 |
试题篮
()