下列说法不正确的是
甲 乙 丙 丁
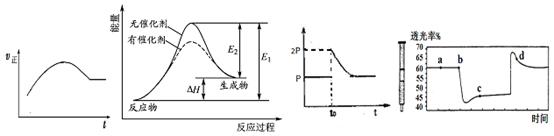
A.绝热恒容密闭容器中通入A和B,发生反应:2A (g)+B (g)  2C(g),图甲为其正反应速率随时间变化的示意图,则该反应为放热反应。 2C(g),图甲为其正反应速率随时间变化的示意图,则该反应为放热反应。 |
| B.催化剂能降低反应的活化能,提高活化分子的百分含量,从而加快化学反应速率。图乙显示的是催化反应与无催化反应过程中的能量关系。 |
C.将BaO2放入密闭真空容器中,反应2BaO2(s)  2BaO(s)+O2(g)达到平衡时体系压强为P,保持温度不变,t0时刻将容器体积缩小为原来的1/2,体系重新达到平衡,体系压强变化如图丙所示。 2BaO(s)+O2(g)达到平衡时体系压强为P,保持温度不变,t0时刻将容器体积缩小为原来的1/2,体系重新达到平衡,体系压强变化如图丙所示。 |
D.将一定量的NO2充入针筒中后封口,发生反应2NO2 (g) N2O4(g),图丁表示在拉伸和压缩针筒活塞的过程中气体透光率随时间的变化(气体颜色越深,透光率越小)。则c点与a点相比,c(NO2)增大,c(N2O4)减小。 N2O4(g),图丁表示在拉伸和压缩针筒活塞的过程中气体透光率随时间的变化(气体颜色越深,透光率越小)。则c点与a点相比,c(NO2)增大,c(N2O4)减小。 |
2.0molPCl3和1.0molCl2充入体积不变的密闭容器中,在一定条件下发生下述反应:
PCl3(g)+Cl2(g)= PCl5(g);反应达到平衡时,PCl5为0.4mol;如果此时移走1.0molPCl3和0.5molCl2,在相同的温度下再达到平衡时,PCl5的物质的量为( )
| A.0.4mol |
| B.0.2mol |
| C.小于0.2mol |
| D.大于0.2mol,小于0.4mol |
在一密闭容器中加入A、B、C三种气体,保持一定温度,在t1~t4时刻测得各物质的浓度如下表.据此判断下列结论正确的是
| 测定时刻/s |
t1 |
t2 |
t3 |
t4 |
| c(A)/(mol/L) |
6 |
3 |
2 |
2 |
| c(B)/(mol/L) |
5 |
3.5 |
3 |
3 |
| c(C)/(mol/L) |
1 |
2.5 |
3 |
3 |
A.在t3时刻反应已经停止
B.A的转化率比B的转化率低
C.在容器中发生的反应为:2A+B⇌2C
D.在t2~t3内A的平均反应速率为:[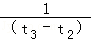 ]mol/(L•s)
]mol/(L•s)
在一定的温度下, 向一密闭容器中放入 1 mol A 和 1 mol B, 发生下列反应:A(g) + B(g)  C(g) + 2D(g),达到平衡状态时,C的含量为 m%,保持温度和体积不变,若按照下列配比在上述容器放入起始物质,达到平衡状态时C的含量仍然为m%的是
C(g) + 2D(g),达到平衡状态时,C的含量为 m%,保持温度和体积不变,若按照下列配比在上述容器放入起始物质,达到平衡状态时C的含量仍然为m%的是
| A.2mol A + 1mol B |
| B.1mol C + 1mol D |
| C.2mol C + 2mol D |
| D.0.5mol A +0.5mol B +0.5mol C +1mol D |
某恒温密闭容器发生可逆反应:Z(?)+W(?) X(g)+Y(?)ΔH,在t1时刻反应达到平衡,在t2时刻缩小容器体积,t3时刻再次达到平衡状态后未再改变条件。下列有关说法中正确的是( )
X(g)+Y(?)ΔH,在t1时刻反应达到平衡,在t2时刻缩小容器体积,t3时刻再次达到平衡状态后未再改变条件。下列有关说法中正确的是( )

| A.Z和W在该条件下均为非气态 |
| B.t1~t2时间段与t3时刻后,两时间段反应体系中气体的 平均摩尔质量不可能相等 |
| C.若在该温度下此反应平衡常数表达式为K=c(X),则 t1~t2时间段与t3时刻后的X浓度不相等 |
| D.若该反应只在某温度T以上自发进行,则该反应的平衡常数K随温度升高而减小 |
有下列五个化学方程式(X、Y、Z均为正值):
①C2H2(g)+H2(g) C2H4(g)
C2H4(g)
②CH4(g) H2(g)+
H2(g)+ C2H4(g)
C2H4(g)
③C(s)+2H2(g) CH4(g);△H=-X kJ·mol—1
CH4(g);△H=-X kJ·mol—1
④C(s)+ H2(g)
H2(g)
 C2H2(g);△H=-Y kJ·mol—1
C2H2(g);△H=-Y kJ·mol—1
⑤C(s)+H2(g)
 C2H4(g);△H=-Z kJ·mol—1
C2H4(g);△H=-Z kJ·mol—1
当温度下降时①式平衡向右移动,②式平衡向左移动。据此判定③—⑤式中关于X、Y、Z的大小顺序排列正确的是
| A.X>y>Z | B.X>Z>Y | C.Y>X>Z | D.Z>X>Y |
相同温度下,体积均为1.5 L的两个恒容容器中发生可逆反应:X2 (g)+3Y2(g)  2XY3(g) ΔH=-92.6 kJ·mol-1,实验测得有关数据如下表:
2XY3(g) ΔH=-92.6 kJ·mol-1,实验测得有关数据如下表:
| 容器编号 |
起始时各物质物质的量/mol |
达平衡时体系能量的变化 |
||
| X2 |
Y2 |
XY3 |
||
| ① |
1 |
3 |
0 |
放热46.3 kJ |
| ② |
0.8 |
2.4 |
0.4 |
Q(Q>0) |
下列叙述不正确的是( )
A、容器①中达到平衡时,Y2的转化率为50%
B、Q="27.78" kJ
C、相同温度下;起始时向容器中充入1.0 X2 mol 、3.0 mol Y2和2 mol XY3;反应达到平衡前v(正)>v(逆)
D、容器①、②中反应的平衡常数相等,K=
密闭容器中,反应xA(g)+yB(g) zC(g)达到平衡时,A的浓度为0.5mol·L-1,若保持温度不变,将容器的容积扩大原来的2倍,达到新平衡时,测得A气体的浓度为0.3mol/L,则下列叙述中正确的是( )
zC(g)达到平衡时,A的浓度为0.5mol·L-1,若保持温度不变,将容器的容积扩大原来的2倍,达到新平衡时,测得A气体的浓度为0.3mol/L,则下列叙述中正确的是( )
| A.x+y<n | B.该化学平衡向正方向移动 |
| C.B的转化率增大 | D.C的体积分数减小 |
Cr2O72-可通过下列反应转化成铬黄(PbCrO4):
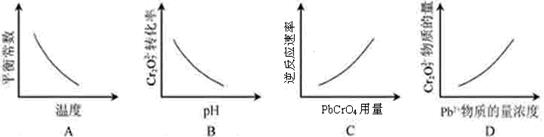
Cr2O72-(aq)+2Pb2+(aq)+H2O(l) 2 PbCrO4(s)+2H+(aq) ΔH< 0
2 PbCrO4(s)+2H+(aq) ΔH< 0
该反应达平衡后,改变横坐标表示的反应条件,下列示意图正确的是( )
T °C时,在容积为2 L的3个恒容密闭容器中发生反应:3A(g)+B(g) XC(g),按不同方式投入反应物,测得反应达到平衡时的有关数据如下:
XC(g),按不同方式投入反应物,测得反应达到平衡时的有关数据如下:
| 容器 |
甲 |
乙 |
丙 |
| 反应物的投入量 |
3molA、2mol B |
6molA、4molB |
2molC |
| 达到平衡的时间/ min |
5 |
|
8 |
| A的浓度/mol • L-1 |
C1 |
C2 |
|
| C的体积分数/% |
 |
|
 |
| 混合气体的密度/g • L-1 |
 |
 |
|
下列说法正确的是
A.若 x <4,,2C1<C2
B.若 x = 4,则 =
=
C.无论x的值是多少贝均有 =
=
D.容器甲达到平衡所需的时间比容器乙达到平衡所需的时间短
在相同温度下,有相同体积的甲、乙两容器,容器体积固定不变。甲容器中充入1gSO2和1gO2;乙容器中充入2g SO2和2g O2.下列叙述错误的是( )
| A.化学反应速率:乙>甲 | B.平衡后SO3的浓度:乙>甲 |
| C.O2的转化率:乙>甲 | D.平衡后O2的体积分数:乙>甲 |
工业上制备纯硅反应的热化学方程式如下:SiCl4(g)+2H2(g) Si(s)+4HCl(g);△H=+Q kJ·mol-1(Q>0)。某温度、压强下,将一定量的反应物通入密闭容器进行以上反应(此条件下为可逆反应),下列叙述正确的是
Si(s)+4HCl(g);△H=+Q kJ·mol-1(Q>0)。某温度、压强下,将一定量的反应物通入密闭容器进行以上反应(此条件下为可逆反应),下列叙述正确的是
| A.反应达平衡后,若压缩容器的体积,则SiCl4的转化率增大 |
| B.若反应开始时投入1mol SiCl4、2mol H2,则达到平衡时吸收热量为Q kJ |
| C.若反应4min HCl的浓度为0.12mol·L-1,则H2的反应速率为0.03mol·(L·min)-1 |
| D.当反应吸收热量为0.025 Q kJ时,则生成的HCl全部通入100mL1mol·L-1的NaOH溶液中恰好反应 |
体积相同的甲、乙两个容器中,分别充有等物质的量的SO2和O2,在相同温度下发生反应2SO2(g)+O2(g) 2SO3(g)并达到平衡。在这个过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为p%,则乙容器中SO2的转化率为( )
2SO3(g)并达到平衡。在这个过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为p%,则乙容器中SO2的转化率为( )
| A.等于p% | B.大于p% | C.小于p% | D.无法判断 |
试题篮
()