设NA表示阿伏加得罗常数,下列叙述正确的是
| A.标准状况下,11.2L氦气所含的原子数为NA |
| B.1.6gNH2-离子中所含的电子数为NA |
| C.常温常压下,44g二氧化碳分子中所形成的共用电子对数为2NA |
| D.NA个氮分子和NA个氢分子的体积比是1︰1 |
设NA为阿伏伽德罗常数的数值,则下列说法中正确的是
①2.24L氨气含有NA个电子,②1.4g乙烯与丙烯的混合气体含有NA个碳原子,③精炼铜, 若阳极失去2NA个电子,则阴极增重64g,④标准状况下,22.4L空气含有NA个分子,⑤过氧化钠与水反应,若电子转移4NA,则产生的氧气为32 g,⑥将1L 2mol/L 的FeCl3溶液加入到沸水中,加热使之完全反应,所得氢氧化铁胶体粒子数为2NA,⑦在1L 0.1mol/L的碳酸钠溶液中,阴离子总数大于0.1NA
| A.②③④⑦ | B.①③④⑦ | C.②③④⑤⑦ | D.②④⑤⑦ |
设NA表示阿伏加德罗常数,下列说法错误的是( )
| A.一定量的Fe与含1 mol HNO3的稀硝酸恰好反应,则被还原的氮原子数小于NA |
| B.1 L 1 mol/L的FeCl3溶液中含有NA个Fe3+ |
| C.常温常压下,等质量的SO2、S2含有相同的分子数 |
| D.125 g CuSO4·5H2O晶体中含有0.5NA个Cu2+ |
NA表示阿伏加德罗常数,下列判断正确的是( )
| A.标准状况下,22.4 L CCl4中含有氯原子数目为4NA |
| B.0.05 mol硫酸氢钠晶体中含离子总数为0.15NA |
| C.常温下,16 g O2与O3的混合气体中含氧原子数为NA |
| D.一定条件下,2 mol二氧化硫和1 mol氧气混合,反应时转移的电子数为4NA |
阿伏加德罗常数约为6.02×1023mol-1,下列说法正确的是( )
| A.1.0 L 1 mol·L-1氨水中,NH3·H2O的分子数为6.02×1023 |
| B.当有7.1 g Cl2和水完全反应时转移的电子数为0.1×6.02×1023 |
| C.白磷分子(P4)呈正四面体结构,31 g白磷中含有P—P键个数为6×6.02×1023 |
| D.20 g重水(2H216O)中含有的中子数为8×6.02×1023 |
设NA为阿伏加德罗常数,下列说法正确的是( )
| A.常温常压下,0.2NA个NH3分子的质子数NA |
| B.1 mol NaCl中,所有Na+的最外层电子总数为8NA |
| C.7.1g Cl2变为氯离子时,得到的电子数一定为0.1NA |
D.1L 0.2 mol/L硫酸铁溶液中含有的SO 离子数目为0.2NA 离子数目为0.2NA |
设NA表示阿伏加德罗常数的值,下列说法错误的是( )
| A.标准状况下,4.48L氦气和重氢气(D2)的混合物中所含中子数为0.4NA |
| B.常温下,0.1molCl2与过量稀NaOH溶液反应,转移的电子总数为0.2NA |
C.10.6gNa2CO3固体中,所含CO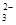 的数目为0.1NA 的数目为0.1NA |
| D.足量铜与0.1L18.4mol·L-1”浓硫酸反应,生成SO2的分子数一定小于0.92NA |
NA为阿伏加德罗常数的数值,下列说法中正确的是
| A.0.5molO3与11.2LO2所含的分子数一定相等 |
| B.在密闭容器中加入1.5 mol H2和0.5 molN2,充分反应后可得到NH3分子数为NA |
| C.常温常压下,7.0g乙烯与丁烯的混合物中含有氢原子的数目为NA |
| D.标准状况下,22.4 L氯气与足量铁粉充分反应,转移的电子数为3 NA |
设NA为阿伏加德罗常数的数值,下列说法不正确的是( )
| A.常温下,1 L pH=1的硫酸溶液中含有的H+为0.1NA |
| B.常温下,14g C2H4和C3H6的混合气体中含有2NA个氢原子 |
| C.2.3 g Na和足量的O2完全反应,在常温和燃烧时,转移电子数均为0.1NA |
| D.1mol甲醇中含有C—H键的数目为4NA |
设nA为阿伏加德罗常数的数值,下列说法正确的是( )
| A.16 g CH4中含有4 nA个C—H键 |
| B.1 mol/L NaCl溶液含有nA个Na+ |
| C.1 mol Cu和足量稀硝酸反应产生nA个NO分子 |
| D.标准状况下,22.4 L己烯中含有nA个CO2分子 |
设NA代表阿伏加德罗常数的数值,下列说法中正确的是( )
①常温常压下,17 g甲基(-14CH3)所含的中子数为9NA
②常温常压下,22.4 L NO气体的分子数小于NA ③64 g铜发生氧化还原反应,一定失去2NA个电子 ④常温常压下,100 mL 0.5 mol/L的乙酸溶液中,乙酸的分子数目小于0.05NA ⑤标准状况下,22.4 L二氯甲烷所含有的分子数为NA ⑥常温常压下,1 mol氦气含有的核外电子数为4NA
| A.①② | B.③④ | C.②④ | D.⑤⑥ |
向m g镁和铝的混合物中加入适量的稀硫酸,恰好完全反应生成标准状况下的气体b L。向反应后的溶液中加入c mol/L氢氧化钾溶液V mL,使金属离子刚好沉淀完全,得到的沉淀质量为n g。再将得到的沉淀灼烧至质量不再改变为止,得到固体p g。则下列关系不正确的是
A. |
B. |
C.n=m+17Vc | D. m<p< m<p< |
用NA表示阿伏加德罗常数的值,则下列叙述正确的是
| A.标准状况下,2.24LSO3含有的分子数等于0.1NA |
| B.常温下,1.0L 1.0 mol·L-1NaAlO2溶液中含有的氧原子数为2NA |
| C.7.8 g Na2S和Na2O2的混合物中含有的阴离子数等于0.1NA |
| D.0.1 mol Fe参加氧化还原反应,转移的电子数目一定是0.2 NA |
用NA表示阿伏加德罗常数的值。下列叙述正确的是
| A.标况下,11.2L的戊烷含有分子数为0.5NA个 |
| B.常温下,14g乙烯和丙烯的混合物中总原子数为3NA个 |
| C.1L浓度为1mol·L-1的Na2CO3溶液中含有NA个CO32- |
| D. 1L 1mol/L的盐酸溶液中,所含氯化氢分子数为NA |
试题篮
()