利用碳棒、锌片和200ml稀硫酸组成原电池,将化学能转化为电能,当碳棒上共产生3.36L(标准状况)气体时,硫酸恰好全部被消耗。试计算:
(1)锌片的质量减少了多少?
(2)原稀硫酸溶液的物质的量浓度。
(3)有多少个电子通过了导线。
把a、b、c、d 四块金属片浸泡在盐酸中,用导线两两相连可以组成各种原电池:若a、b相连时,a为负极;c、d相连时,电子从 c流向d;a、c相连时,c极发生还原反应;b、d相连时,b极产生大量气泡。则这四种金属的活动性顺序由大到小为:
| A.a>b>c>d | B.b>d>c>a | C.c>a>b>d | D.a>c>d>b |
锌和足量的稀HCl反应时,加入少量CuSO4固体,下列叙述正确的是:
| A.反应速率减慢,产生H2的量不变 |
| B.反应速率加快,产生H2的量不变 |
| C.反应速率不变,产生H2的量增加 |
| D.反应速率加快,产生H2的量减少 |
在理论上可用于设计原电池的化学反应是
| A.2Al(s)十2NaOH(aq)+2H2O(1)=2NaAlO2(aq)+3H2(g);△H <O |
| B.Ba(OH)2·8H2O(s)+2NH4Cl(s)=BaCl2(aq)+2NH3·H2O(aq)+8H2O(1);△H >0 |
| C.CaC2(s)+2H2O(1)→Ca(OH)2(s)+C2H2(g);△H <0 |
D.FeCl3(aq)十3H2O(1) Fe(OH)3(s)+3HCl(aq);△H >0 Fe(OH)3(s)+3HCl(aq);△H >0 |
右图装置中,所用电极均为惰性电极,通电一段时间后,b极附近溶液呈红色,下列说法中正确的是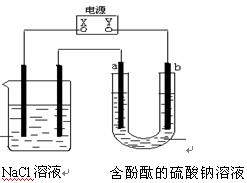
| A.X是正极,Y是负极 | B.a是正极,b是负极 |
| C.NaCl溶液的pH保持不变 | D.NaCl溶液的pH减小 |
已知可逆反应:AsO43-+2I-+2H+ AsO33-+I2+H2O 据此设计出如右图所示的实验装置(装置中盐桥的作用是使整个装置形成一个闭合回路).向(B)烧杯中逐滴加入浓盐酸,发现微安表指针偏转
AsO33-+I2+H2O 据此设计出如右图所示的实验装置(装置中盐桥的作用是使整个装置形成一个闭合回路).向(B)烧杯中逐滴加入浓盐酸,发现微安表指针偏转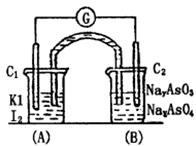
试回答下列问题:
(1)C1棒的电极为 极;发生的电极反应为____________________________.
(2)C2棒的电极为 极;发生的电极反应为____________________________.
如右图所示,将两烧杯中电极用导线相连,四个电极分别为Mg、Al、Pt、C。当闭合开关S后,电流表指针发生偏转,以下表述不正确的是
A.甲池发生了原电池反应
B.Mg是正极
C.乙烧杯中可以用乙醇代替氢氧化钠溶液,电流表仍会偏转
D.甲池pH逐渐减小
A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸,如下图所示:
(1)A中反应的离子方程式是 。
(2)B中Sn极的电极反应式为____________________,Sn极附近溶液的pH__________(填“增大”“减小”或“不变”)。
(3)C中被腐蚀的金属是__________,总反应离子方程式是____________________,比较A、B、C中铁被腐蚀的速率由快到慢的顺序是__________。
a、b的活动性均比氢强,a还可以从b的硝酸盐中置换出b。将a、b用导线相连放入CuSO4溶液中,下列叙述中不正确的是 ( )
| A.导线上有电流,电流方向由a到b | B.a极质量减少,b极质量增加 |
| C.b棒上析出氢气 | D.a棒发生氧化反应,b棒发生还原反应 |
下列各组材料中,不能组成原电池的是 ( )
| |
A |
B |
C |
D |
| 两极材料 |
Zn片、石墨 |
Cu片、Ag片 |
Zn片、Cu片 |
Fe片、Cu片 |
| 插入溶液 |
硫酸溶液 |
硝酸银溶液 |
蔗糖溶液 |
稀盐酸 |
关于如右图所示装置的叙述,正确的是
| A.铜是阳极,铜片上有气泡产生 |
| B.铜片质量逐渐减少 |
| C.电流从锌片经导线流向铜片 |
| D.铜离子在铜片表面被还原 |
关于如图所示的装置的叙述,正确的是:
| A.电流从锌片经导线流向铜片 |
| B.一段时间后,电解质溶液中的硫酸根浓度减少 |
| C.铜是正极,铜片上有气泡产生,锌片质量减少 |
| D.一段时间后,电解质溶液的酸碱性保持不变 |
(1)写出一个能证明还原性Fe比Cu强的离子方程式:
;
(2)根据上述反应设计一个原电池,画出简易装置图(标出电极名称、电极材料、电解质溶液)
;
(3)若该电池中两电极的总质量为60 g,工作一段时间后,取出两电极洗净干燥后称量,总质量为46 g,则反应过程中转移电子的数目为 。
如图
|
甲把锌片和铜片用导线相连后插入稀硫酸溶液构成原电池。某实验兴趣小组做完实验后,在读书卡上的记录如图乙所示,则卡片上的描述合理的是( )
 卡片号:2009.3
卡片号:2009.3
 实验后的记录:
实验后的记录:
①Cu为阳极,Zn为阴极
②Cu极上有气泡产生
③SO42-向Cu极移动
④若有0.5mol电子流经导线,则可产生0.25mol气体
 ⑤电子流向是:Cu Zn
⑤电子流向是:Cu Zn
⑥正极反应式:Cu + 2e- = Cu2+
图甲 图乙
| A.①②③ | B.②④ | C.④⑤⑥ | D.③④⑤ |
试题篮
()