甲、乙两池电极材料都是铁棒与碳棒,两池中均为饱和NaCl溶液。请回答下列问题:
(1)甲池属于 (填装置名),其中正极材料为 ,其电极反应式是_____________ 。
(2)乙池属于 (填装置名),铁极上电极反应属于____________(填“氧化反应”或“还原反应”),写出乙池中总反应的离子方程式___________。
(4) 若乙池转移0.01 mol e-后停止实验,池中溶液体积是100 mL,则溶液混匀后的[OH‾]=________。(溶液体积变化忽略)
依据氧化还原反应: 2Ag+(aq) + Cu(s) ="==" Cu2+(aq) + 2Ag(s)设计的原电池如图所示。请回答下列问题:
2Ag+(aq) + Cu(s) ="==" Cu2+(aq) + 2Ag(s)设计的原电池如图所示。请回答下列问题:
(1)电极X的材料是 ;电解质溶液Y是 。
(2)外电路中的电子是从 电极流向 电极。
(3)银电极上发生的电极反应式为
(5分)已知电极材料:铁、铜、银、石墨、锌、铝;电解质溶液:CuCl 溶液、Fe
溶液、Fe (SO
(SO )
) 溶液、盐酸。按要求回答下列问题:若电极材料选铜和石墨,电解质溶液选硫酸铁溶液,外加导线,能否构成原电池? (填“能”或“不能”)。若能,请写出电极反应式:负极 ,正极 。若不能,请说明原因 。
溶液、盐酸。按要求回答下列问题:若电极材料选铜和石墨,电解质溶液选硫酸铁溶液,外加导线,能否构成原电池? (填“能”或“不能”)。若能,请写出电极反应式:负极 ,正极 。若不能,请说明原因 。
有铜片、锌片、若干小烧杯、导线、、盐桥(含琼胶的KCl饱和溶液)、电流计、ZnSO4溶液、CuSO4溶液,试画出原电池的装置图,并说明其工作原理。
⑴原电池装置图; ⑵工作原理;
(8分)燃煤废气中的氮氧化物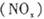 、二氧化碳等气体,常用下列方法处理,以实现节能减排、废物利用等。
、二氧化碳等气体,常用下列方法处理,以实现节能减排、废物利用等。
(1)对燃煤废气进行脱硝处理时,常利用甲烷催化还原氮氧化物。如: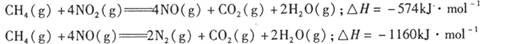
则CH4 ( g)将NO2 (g)还原为N2(g)等的热化学方程式是________________________________
(2)将燃煤废气中的CO2转化为甲醚的化学方程式为: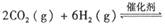
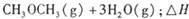 。已知在一定压强下,该反应随温度的升高而CO2的转化率降低。则该反应的
。已知在一定压强下,该反应随温度的升高而CO2的转化率降低。则该反应的 ________ 0(填“ >”或“ <”);若用以甲醚、空气、氢氧化钾溶液为原料,石墨为电极构成燃料电池,则该电池中负极的电极反应式是________________________________,放电过程中溶液的PH________ (填“增大”、“减小”或“不变”)。
________ 0(填“ >”或“ <”);若用以甲醚、空气、氢氧化钾溶液为原料,石墨为电极构成燃料电池,则该电池中负极的电极反应式是________________________________,放电过程中溶液的PH________ (填“增大”、“减小”或“不变”)。
某兴趣小组同学利用氧化还原反应:2KMnO4+10FeSO4+8H2SO4===2MnSO4+5Fe2(SO4)3+K2SO4+8H2O设计如下原电池,其中甲、乙两烧杯中各物质的物质的量浓度均为1 mol·L-1,盐桥中装有饱和K2SO4溶液.回答下列问题: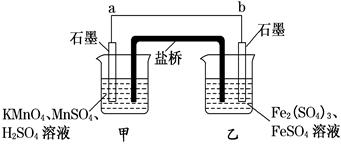
(1)发生氧化反应的烧杯是________(填“甲”或“乙”).
(2)外电路的电流方向为:从________到________.(填“a”或“b”)
(3)电池工作时,盐桥中的SO移向________(填“甲”或“乙”)烧杯.
(4)甲烧杯中发生的电极反应为______________________________________________.
(1)A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸。
①B中Sn极的电极反应式为__________________,Sn极附近溶液的pH(填“增大”、“减小”或“不变”)__________。
②A中总反应离子方程式为__________。比较A、B、C中铁被腐蚀的速率,由快到慢 的顺序是________。
的顺序是________。
(2)如图是甲烷燃料电池原理示意图,回答下列问题:
①电池的负极是__________(填“a”或“b”),该极的电极反应是:__________。
②电池工作一过程中正极pH______,负极pH值_______,一段时间后电解质溶液的pH__________(填“增大”、“减小”或“不变”)。
人们已经研制出以丙烷为燃料的新型燃料电池,电解质为熔融酸盐,电池

(2)该电池的正极通入O2和CO2,负极通入丙烷,则正极的电极反应式为__________________________________,电池工作时CO32—移向_____________极。
(3)用该电池电解1L 1 mol·L—1的AgNO3溶 液,此电解池反应的化学方程式为_________________________________________________;当该电池消耗0.005molC3H8时,所得溶液的pH为__________(溶液体积变化忽略不计)
液,此电解池反应的化学方程式为_________________________________________________;当该电池消耗0.005molC3H8时,所得溶液的pH为__________(溶液体积变化忽略不计)
糖类物质为很多生物生命活动提供能量。
(1)已知 45g葡萄糖在人体内完全氧化为二氧化碳和水,放出701KJ的热量,该反应的热化学方程式 。
(2)以葡萄糖为燃料的微生物燃料电池结构如图所示,其负极反应为: .
电池工作过程中溶液中氢离子移动方向从 极区
移向 极区(填“正”或“负”)
(3)常温下,用上述电池惰性电极电解100L某浓的硫酸铜溶液,当溶液PH=1时停止电解,则理论上需要葡萄糖的质量为 。(假设溶液体积不变)
将洁净的金属片A、B 、C、D 分别放置在浸有盐溶液的滤纸上面并压紧(如图所示)。在每次实验时,记录电压指针的移动方向和电压表的读数如右表所示:
已知构成原电池两电极的金属活动性相差越大,电压表读数越大。请判断:
(1) A、B、C、D四种金属中活泼性最强的是_____________(用字母表示)
(2) 若滤纸改用NaOH溶液浸润一段时间后,则在滤纸上能看到有白色物质析出,后迅速变为灰绿色,最后变成褐色。则滤纸上方的金属片为___________(A、B、C、D中哪一种),此时对应的电极反应式为:正极___________________________________________
Li-SOCl2电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解液是LiAlCl4—SOCl2。电池的总反应可表示为:4Li+2SOCl2 =" 4LiCl" +S +SO2。 请回答下列问题:
请回答下列问题: (1)电池的负极材料为 ,该极的电极反应
(1)电池的负极材料为 ,该极的电极反应 式为 ;
式为 ; (2)电池正极的电极反应式为 ;
(2)电池正极的电极反应式为 ; (3)SOCl2易挥发,实验室中常用NaOH溶液吸收SOCl2,有Na2SO3和NaCl生成。 如果把少量水滴到SOCl2中,实验现象是 ,反应的化学方程式为 ;
(3)SOCl2易挥发,实验室中常用NaOH溶液吸收SOCl2,有Na2SO3和NaCl生成。 如果把少量水滴到SOCl2中,实验现象是 ,反应的化学方程式为 ; (4)组装该电池必须在无水、无氧的条件下进行,原因是 。
(4)组装该电池必须在无水、无氧的条件下进行,原因是 。
(共18分)I写出下列热化学反应方程式
(1)N2 (g)与H2(g)反应生成1molNH3(g),放出46.1KJ热量。
(2)1molC2H5OH(l)完全燃烧生成CO2(g)和H2O(l),放出1366.8KJ热量。
(3)1molC(石墨)与适量H2O(g)反应吸收131.3KJ热量
II.(1)化学反应中均伴随着能量的变化,化学键的断裂和形成是发生能量变化的主要原因。生成物中化学键形成时会__________能量(填“放出”或“吸收”);如果一个化学反应,化学键断裂时的能量变化大于化学键形成时的能量变化,则该反应属于_________反应; 如果一个化学反应,反应物的总能量和生成物的总能量有如图所示的关系,则该反应属于__________反应。
如果一个化学反应,反应物的总能量和生成物的总能量有如图所示的关系,则该反应属于__________反应。
(2)不同形式的能量可以相互转换,如:化学能和电能、热能之间的相互转换。如图是一个原电池工作原理的示意图。试回答:
①从能量角度看,它属于____________能转化为____________能;
②装置中Zn为____________极。
(1)依据氧化还原反应:2Ag+(aq) + Cu(s) ="=" Cu2+(aq) + 2Ag(s)设计的原电池如图所示。请回答下列问题:
①电极X的材料是  ;电解质溶液Y是 ;
;电解质溶液Y是 ;
②银电极为电池的 极,发生 的电极反应式为 ;X电极上发生的电极反应式为 ;
的电极反应式为 ;X电极上发生的电极反应式为 ;
③外电路中的电子是从 电极流向 电极。
(2)物质Z是中学化学中的常见物质,X既能与稀硫酸反应,又能与氢氧化钠溶液反应。
①若Z为氧化物,X的化学式是___________________________。
②若Z为单质,Z与NaOH溶液反应的离子方程式为___________________________________。
③若Z与稀硫酸反应生成无色没有气味的气体A,与氢氧化钠溶液加热反应生成气体B。等物质的量的A和B在水溶液中反应又生成X。
Z与稀硫酸反应的离子方程式是______________________________________;
Z与足量氢氧化钠溶液加热的离子方程式是__________________________。
(1)实事证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是 。
A.C(s)+H2O(g)=CO(g)+H2(g) △H>0
B.NaOH(aq)+HC1(aq)=NaC1(aq)+H2O(1) △H<0
C.2H2(g)+O2(g)=2H2 O(1) △H<0
O(1) △H<0
(2)以KOH溶液为电解质溶液,依据所选反应设计一个原电池,其负极反应的电极反应式为 。
(3)电解原理在化学工业中有着广泛的应用。
现将你设计的原电池通过导线与下图中电解池相连,其中,a为电解液,X和Y是两块电极板,则:
① 若X和Y均为惰性 电极,a为CuSO4溶液
电极,a为CuSO4溶液
则阳极的电极反应式为 ,电解时的化学反应方程式为 ,通过一段时间后,向所得溶液中加入0.2molCuO粉末,恰好恢复到电解前的浓度和pH,则电解过程中转移的电子的物质的量为 。
②若X、Y分别为铁和铜,a仍为CuSO4溶液,则Y极的电 极反应式为
极反应式为
③若用此装置电解精炼铜, 做阳极,电解液CuSO4的浓度 (填“增大”、“减小”或“不变”)。
④若用此装置在铁制品上镀铜,铁制品做 ,电镀液的浓度 (填“增大”、“减小”或“不变”)。
试题篮
()