某化学兴趣小组设计了下图所示实验装置,其中c为石墨电极,d为银电极。
(1)甲池中OH-移向 极(填电极的字母序号),f为 (填电极名称)。
(2)a极上的电极反应式是 。
(3)乙池中放出气体的电极为 极(填“c”或“d”),写出此电极反应式: 。
(4)乙池中总反应的离子方程式是 。
(5)当乙池中阴极质量增加5.40 g时,丙池某电极析出1.60 g金属,则丙池的溶液中溶质可能是 (填序号)。
| A.MgSO4 | B.CuSO4 | C.NaCl | D.AgNO3 |
某兴趣小组为研究原电池原理设计了如下图装置,盐桥中装有含琼胶的KCl饱和溶液。
(1)Cu极为原电池的 极(填“正”或“负”),电极反应式是 ;Zn极发生 (填“氧化”或“还原”)反应。
(2)盐桥中K+移向 (填“甲”或“乙”)烧杯的溶液。取出盐桥,电流计指针 (填“偏转”或“不偏转”)。
(3)若将锌电极换为石墨,甲烧杯中盛装等物质的量浓度的Fe2(SO4)3和FeSO4混合溶液,则两烧杯中的电极反应式分别为:甲 ,乙 。
如下图所示,烧杯中都盛有稀硫酸。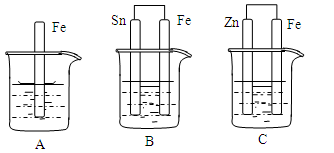
(1)A中反应的离子方程式为 ;
(2)B中的电极反应:Fe: .Sn: Sn极附近溶液的pH(填增大、减小或不变) ;
(3)C中被腐蚀的金属是 。其电极反应式为 。比较A、B、C中纯铁被腐蚀的速率由快到慢的顺序是 。
依据氧化还原反应:2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池如图所示。请回答下列问题: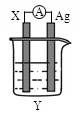
(1)电极X的材料是______;电解质溶液Y是________;
(2)银电极为电池的 极,发生的电极反应为 ;X电极上发生的电极反应为_______反应;(填“氧化”或“还原”)
(3)外电路中的电子 (填“流出”或“流向”)Ag电极。
(4)当有1.6 g铜溶解时,银棒增重______ g。
由铜、锌和稀硫酸组成的原电池中:
(1)锌是 极,电极反应式是 。
(2)铜是 极,电极反应式是 。
(3)在铜极上可以观察到有 (填实验现象)
根据下图所示回答有关问题:
(1)甲池为 (选填“原电池”或“电解池”),石墨A上发生的电极反应式为: 。
(2)乙池中Zn棒为 极, Zn棒上发生反应的电极反应式为: 。
(3)石墨B上刚好有9.6克物质析出时,则反应过程中转移的电子数为 。
电子表和电子计算器中所用的是钮扣式的微型银锌电池,其电极分别为Ag2O和Zn,电解液为KOH溶液。工作时电池总反应为:Ag2O+Zn+H2O=2Ag+Zn(OH)2。
(1)工作时电流从 极流向 极(两空均选填“Ag2O”或“Zn”);
(2)负极的电极反应式为: ;
(3)工作时电池正极区的pH (选填“增大”“减小”或“不变”);
(4)外电路中每通过0.2 mol电子,锌的质量理论上减少 g。
(1)将锌、铜用导线连接后浸入2mol/L的稀硫酸中,正极电极反应式为_______________________,发生 反应(填氧化或还原);电子从 经外电路到____ (填锌或铜),溶液中H+ 向 移动(填正极或负极),放电一段时间后,正极区pH值 (填变大、变小或不变)。
(2)将铜片和铁片用导线连接后插入三氯化铁溶液中,也有电流通过电流表,负极电极反应式为_________________,总反应的离子方程式为______ 。
可以将氧化还原反应2H2+O2=2H2O设计成原电池。(每空2分)
(1)利用H2、O2、HCl溶液构成燃料电池,则正极的电极反应式为_______________;负极的电极反 应式为________________。
(2)把H2改成CH4,KOH溶液作电解质,则负极的电极反应式为_______________,当导线中通过4 mol电子时,需消耗______mol的KOH;将4 mol CH4完全与Cl2发生取代反应,并生成等物质的量的四种氯代物,则理论上需要消耗Cl2的物质的量为_______mol。
(9分)将反应IO3-+5I-+6H+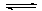 3I2+3H2O设计成如图所示的原电池。
3I2+3H2O设计成如图所示的原电池。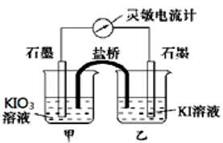
(1)开始时向甲烧杯中加入少量浓硫酸,电流计指针向右偏转,此时甲池中发生的电极反应式为____________,工作过程中关于电流计的读数,下列说法正确的是_______(填编号)
a.电流计读数逐渐减小 b.电流计读数有可能变为0
c.电流计读数一直不变 d.电流计的读数逐渐增大
(2)如果在加浓硫酸前,甲、乙烧杯中都加入淀粉溶液,则溶液变蓝的烧杯是_______(填“甲”、“乙”)。
(3)工作一段时间后,如果再向甲烧杯滴入浓NaOH溶液,此时乙池中发生的电极反应式为____________,电流计指针向_____(填“左”、“右”)偏转。
(7分)下图是铜锌原电池装置。其电池的总反应是:Zn(s) + CuSO4(aq)="=" ZnSO4(aq) + Cu(s)。
请回答以下问题:
(1)R的名称是____________,其作用是_____________。R中的阳离子移向_______(填A或B)中的溶液。
(2)电极Y的材料是________,B中的电解质溶液是______________。
(3)X为原电池的______极,其电极反应式是______________________。
有A、B、C、D四种短周期元素,其原子序数依次增大。A、B可形成A2B和A2B2两种化合物,B、C同主族且可形成CB2和CB3两种化合物。回答下列问题。
(1)B在周期表中的位置______________。
(2)CB2通入A2B2溶液中可被氧化为W,方程式为____________。用W的溶液(体积为1L,假设变化前后溶液体积变化忽略不计)组装成原电池(如图所示)
电池总反应可表示为:PbO2 +Pb+ 2W= 2PbSO4 + 2H2O 。若电池中转移0.1 mol电子时,则W的浓度由质量分数39 % (密度1.3 g·cm-3)变为____________mol·L-1。
(3)金属元素E是中学化学常见元素,位于元素周期表的第四周期。该元素可与D形成ED2和ED3两种化合物。将E的单质浸入ED3溶液中(如下图甲所示),溶液由黄色逐渐变为浅绿色,该反应的离子方程式为_________________________。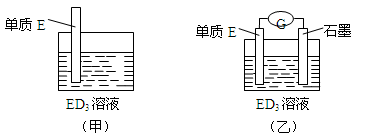
(4)依据(3)中的反应,可用单质E和石墨为电极设计一个原电池,则在该原电池工作时,石墨一极发生的反应可以表示为________________。比较甲、乙两图,说明石墨除形成闭合回路外所起的作用是 。
将纯锌片和纯铜片按下图方式插入100mL相同浓度的稀硫酸中一段时间,回答下列问题:
(1)上图两装置中能构成原电池的是 (填甲或乙)。
(2)当甲中产生1.12L(标准状况)气体时,理论上通过导线的电子的物质的量为 。
(3)现有如下两个反应:A:NaOH+HCl=NaCl+H2O ;B:Fe+2Fe3+= 3Fe2+,根据两反应的本质,判断 不能设计成为原电池(填A或B),不能的原因是 。
A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸。
(1)分别写出B、C装置中铁片表面发生的电极反应:
B:________________________________________
C:________________________________________
(2)A、B、C中铁被腐蚀的速率,由快到慢的顺序是_____________
(3)科学工作者为心脏病人设计的心脏起搏器的电池是以Pt和Zn为电极材料,依靠人体内液体中含有一定浓度的溶解氧、H+和Zn2+进行工作。该电池的正极反应: 。
(12分)
(一)大气中的部分碘源于O3对海水中I-的氧化。将O3持续通入NaI溶液中进行模拟研究.
(1)O3将I-氧化成I2的过程由3步反应组成:
①I-(aq)+ O3(g)= IO-(aq)+O2(g) △H1
②IO-(aq)+H+(aq) HOI(aq) △H2
HOI(aq) △H2
③HOI(aq) + I-(aq) + H+(aq) I2(aq) + H2O(l) △H3
I2(aq) + H2O(l) △H3
总反应的化学方程式为______,其反应△H=______。
(2)在溶液中存在化学平衡:I2(aq)+I-(aq) I3-(aq),其平衡常数表达式为 。
I3-(aq),其平衡常数表达式为 。
(二)能量之间可以相互转化:原电池可将化学能转化为电能。
(1)下列反应能设计成原电池的是: 。
①2FeCl3+Fe=3FeCl2.C
②AlCl3+3NH3·H2O= Al(OH)3↓+3NH4Cl
③NaOH+HC1=NaC1+H2O
(2)根据(1)所选的反应设计成原电池如图,请在图中完成并作相应标注。
写出该电池的正极反应式: ,电池工作的时候,盐桥中的阴离子移向 (填“负极”,“正极”或“不移动”)。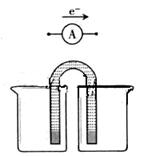
(3)用FeCl3溶液腐蚀印刷电路铜板的化学方程式为: ;
若将该反应设计成下图的原电池,请在图中完成电极材料及电解质溶液的标注。
试题篮
()