下表列出了3种燃煤烟气脱硫方法的原理。
| 方法I |
用氨水将 转化为 转化为 ,再氧化成 ,再氧化成 。 。 |
| 方法II |
用生物质热结气(主要成分: 、 、 、 、 )将 )将 在高温下还原成单质硫 在高温下还原成单质硫 |
| 方法III |
用 溶液吸收 溶液吸收 ,再经电解转化为 ,再经电解转化为 。 。 |
(1)光谱研究表明, 易溶于水的
易溶于水的 所形成的溶液中存在着下列平衡:
所形成的溶液中存在着下列平衡:
据此,下列判断中正确的是______________。
A. 该溶液中存在着 分子
分子
B. 该溶液中 浓度是
浓度是 浓度的2倍
浓度的2倍
C. 向该溶液中加入任何足量的强酸都能放出 气体
气体
D. 向该溶液中加入过 量
量 可得到
可得到 、
、 的混合溶液
的混合溶液
(2)方法I中用氨水 吸收燃煤烟气中
吸收燃煤烟气中 的离子方程式为______________。能提高燃煤烟气中
的离子方程式为______________。能提高燃煤烟气中 去除率的措施有______________(填字母)
去除率的措施有______________(填字母)
A. 增大氨水浓度 B. 升高反应温度
C. 使燃煤烟气与氨水充分接触 D. 通入空气使 转化为
转化为
采用方法I脱硫,并不需要先除去燃煤烟气中大量的 ,原因是(用离子方程式表示)________________________________________________________。
,原因是(用离子方程式表示)________________________________________________________。
(3)方法II主要发生了下列反应:







 反应生成
反应生成 的热化学方程式为___________________。
的热化学方程式为___________________。
(4)方法III中用惰性电极电解 溶液的装置如下图所示(阴离子交换膜只允许阴离子通过)。阳极区放出的气体的成分为_____________(填化学式)。
溶液的装置如下图所示(阴离子交换膜只允许阴离子通过)。阳极区放出的气体的成分为_____________(填化学式)。
Ⅰ.(8分)利用下图装置作电解50mL 0.5 mol·L-1的CuCl2溶液实验。

实验记录:
A.阳极上有黄绿色气体产生,该气体使湿润的淀粉碘化钾试纸先变蓝后褪色(提示:Cl2氧化性大于IO3-);
B.电解一段时间以后,阴极表面除有铜吸附外,还出现了少量气泡和浅蓝色固体。
(1)分析实验记录A中试纸颜色变化,用离子方程式解释:① ;
② 。
(2)分析实验记录B中浅蓝色固体可能是 (写化学式),
试分析生成该物质的原因 。
Ⅱ.(10分)A、B、C、D、E、F六种元素的原子序数依次递增,A+核外无电子,B元素的一种单质是自然界中最硬的物质,C、D、E的简单离子具有相同的核外电子排布,舍勒是D元素单质的发现者之一,戴维最早制得了E元素的单质,F元素的单质历史上曾作为流通货币,A、C、D、F四种元素形成的化合物W可用于制镜工业。
(1)D、E两元素通常可形成两种离子化合物,其中一种化合物X可用做供氧剂,X与A2D反应会产生大量气体,该气体能使带火星的木条复燃。请写出X与A2D反应的化学方程式 。
(2)A、B、D、E四种元素形成的某化合物,摩尔质量为68 g·mol-1,请用离子方程式解释其水溶液呈碱性的原因 。
(3)B、C的氧化物是汽车尾气中的主要有害物质,通过钯碳催化剂,两者能反应生成无毒物质,请写出该反应的化学方程式 。
(4)W的水溶液久置会析出一种沉淀物Z,Z由C、F两元素形成且两元素原子个数比为1:3,Z极易爆炸分解生成两种单质。请写出Z分解的化学方程式 。请从化学反应原理的角度解释Z能发生分解反应的原因 。
氯碱工业中电解饱和食盐水的原理示意图,如图所示:
(1)溶液A的溶质是 ;
(2)电解饱和食盐水的离子方程式是 ;
(3)电解时用盐酸控制阳极区溶液的pH在2~3,用化学平衡移动原理解释盐酸的作用 ;
(4)电解所用的盐水需精制。
去除有影响的Ca2+、Mg2+、N H4+、SO42-[c(SO42-)>c(Ca2+)]。
H4+、SO42-[c(SO42-)>c(Ca2+)]。
精致流程如下(淡盐水和溶液A来电解池):
①盐泥a除泥沙外,还含有的物质是 。
②过程Ⅰ中将NH4+转化为N2的离子方程式是
③BaSO4的溶解度比BaCO3的小,过程Ⅱ中除去的离子有
④经过程Ⅲ处理,要求盐水中c 中剩余Na2SO3的含量小于5mg /L,若盐水b中NaClO的含量是7.45 mg /L ,则处理10m3盐水b ,至多添加10% Na2SO3溶液 kg(溶液体积变化忽略不计)。
高锰酸钾是强氧化剂,它的用途遍布各个行业。
(1)工业上由软锰矿(主要成分为MnO2)生产髙锰酸钾分为两个步骤:
①步骤一将软锰矿与过量的固体KOH和空气在高温下反应,生成锰酸钾(K2MnO4),该反应的化学方程式是 。
②步骤二以石墨为阳极,铁为阴极,电解锰酸钾(K2MnO4)溶液,在 (填“阴极区”或“阳极区”)得到高锰酸钾。阴极反应的电极反应式是 。
(2)某研究小组用工业生产高锰酸钾产生的废渣——锰泥(含K2MnO4、MnO2及Pb、Ca等元素)和乳钢废酸液制取工业级碳酸锰(MnCO3),其流程如下:
③轧钢废酸中Fe2+的作用是 。
④操作I、操作Ⅱ、操作Ⅲ的名称是 。
⑤溶液C中除含有Ca2+、Mn2+、H+外,还含有的阳离子是 。
⑥若固体C中不含CaCO3,则溶液C中 < (已知:Ksp(MnCO3)=1×10-11,Ksp(CaCO3)=5×10-9)。
< (已知:Ksp(MnCO3)=1×10-11,Ksp(CaCO3)=5×10-9)。
氢气是一种清洁能源,可以通过多种方法制得。
(1) 工业上用水煤气法制氢气,有关化学方程式是:
反应一:C( s) + H2O(g)
s) + H2O(g)  CO(g) + H2(g) △H> 0
CO(g) + H2(g) △H> 0
反应二:CO(g) + H2O(g)  CO2(g) + H2(g) △H < 0
CO2(g) + H2(g) △H < 0
①若反应一在t℃时达到化学平衡状态,则此温度下该反应的的平衡常数表达式
K = ;
②在427℃时将CO 和H2O(g)各0.01mol通入体积为2升的密闭容器中反应,5分钟时达到平衡状态,该反应的平衡常数是9,则CO的转化率是 ,用CO的浓度变化表示的反应率速v(CO)是 mol /(L·min)。
(2)利用电解饱和食盐水也可制得氢气,下图为电解食盐水的示意图:
请回答:
① C1电极是 极(填“阴”或“阳”),C2电极的电极反应式是 。
②该电解反应的离子方程式是 ,
(3)通过下列方法也可以得到氢气。
已知: CH4(g)+H2O(g)=CO(g)+3H2(g) △H=+206.2kJ·mol-1
CH4(g)+CO2(g)=2CO(g)+2H2(g) △H=-247.4 kJ·mol-1
1molCH4(g)与H2O(g)反应生成CO2(g)和H2(g)的反应热是 kJ·mol-1。
尿素 [CO(NH2)2 ]是首个由无机物人工合成的有机物。
(1)工业上尿素由CO2和NH3,在一定条件下合成,其反应方程式为 。
(2)当氨碳比 =4,CO2的转化率随时间的变化关系如图所示.
=4,CO2的转化率随时间的变化关系如图所示.
①A点的逆反应速率v逆(CO2)  点的正反应
点的正反应
速率为v正(CO2)(填“大于”、“小于”或“等于”)
②NH3的平衡转化率为 。
(3)人工肾脏可用间接电化学方法除去代谢产物中的尿素,原理如图
①电源的负极为 (填“A”或“B”).
②阳极室中发生的化学反应用方程式表示,依次为 、 。
③电解结束后,阴极室溶液的pH与电解前相比将 ;若两极共收集到气体13.44L(标准状况),则除去的尿素为 g(忽略气体的溶解).
铬化学丰富多彩,由于铬光泽度好,常将铬镀在其他金属表面,同铁、镍组成各 种性能的不锈钢,CrO3 大量地用于电镀工业中。
(1)在下图装置中,观察到图 1 装置铜电极上产生大量的无色气泡,而图 2 装置中铜电 极上无气体产生,铬电极上产生大量有色气体。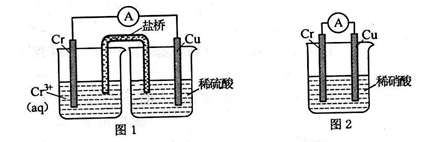
图 2 装置中铬电极的电极反应式______________________
(2)最近赣州酒驾检查特别严,利用 CrO3具有强氧化性,有机物(如酒精)遇到 CrO3时,猛烈反应,CrO3被还原成绿色的硫酸铬[Cr2(SO4)3],另该过程中乙醇被氧化成乙酸, 从而增强导电性,根据电流大小可自动换算出酒精含量。写出该反应的化学方程式为_________________________
(3)虽然铬加到铁中可将铁做成不锈钢可减少金属腐蚀,但 生产成本高,生活中很多情况下还是直接使用钢铁,但易腐蚀, 利用右图装置,可以模拟铁的电化学防护。若 X 为碳棒,为 减缓铁的腐蚀,开关 K 应置于________处。若 X 为锌,开关K 置于________处。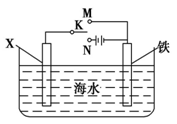
(4)CrO3 和 K2Cr2O7 均易溶于水,这是工业上造成铬污染的 主要原因。净化处理方法之一是将含+6 价 Cr 的废水放入电解槽内,用铁作阳极,加入 适量的 NaCl 进行电解:阳极区生成的 Fe2+和 Cr2O72-发生反应,生成的 Fe3+和 Cr3+在阴极 区与OH-结合生成 Fe(OH)3和 Cr(OH)3沉淀除去【已知某条件下的KspFe (OH)3 = 3.0×10-31, KspCr(OH)3 = 6.0×10-38】。已知电解后的溶液中 c(Fe3+)为 2.0×10-6 mol·L1,则溶液中c(Cr3+)为______________mol·L-1。
工业废水随意排放会造成严重污染,根据成分不同可采用不同的处理方法。
(1)电池生产工业废水中常含有Cu2+等重金属离子,常用FeS等难溶物质作为沉淀剂除去。已知室温下Ksp(FeS)=6.3×10-18mol2·L-2,Ksp(CuS)=1.3×10-36mol2·L-2。
①请用离子方程式说明上述除杂的原理______________________。
②FeS高温煅烧产生的SO2气体通入下列溶液中,能够产生沉淀的是_________(填序号)
A.Ba(NO3)2 B.BaCl2
C.Ba(OH)2 D.溶有NH3的BaCl2溶液
③已知元素在高价态时常表现氧化性,若在酸性CuSO4溶液中加入一定量的Na2SO3和NaCl溶液,加热,生成CuCl沉淀,则生成CuCl的离子方程式是___________。
(2)电解法处理酸性含铬废水(主要含有Cr2O72-)时,在废水中加入适量NaCl,以铁板作阴、阳极,处理过程中存在如下反应Cr2O72+6Fe2++14H+═2Cr3++6Fe3++7H2O,最后Cr3+ 以Cr(OH)3形式除去,下列说法不正确的是______(填序号)
A.阳极反应为Fe-2e-═Fe2+
B.电解过程中溶液pH减小
C.过程中有Fe(OH)3沉淀生成
D.电路中每转移12 mol电子,最多有2mol Cr2O72-被还原
(3)废氨水可以转化成氨,氨再设计成碱性燃料电池。右图是该燃料电池示意图,产生的X气体可直接排放到大气中,a电极作_________极(填“正”“负”“阴”或“阳”),其电极反应式为___________。

I.炒过菜的铁锅未及时洗净,不久便会因腐蚀而出现红色锈斑。请回答:
写出铁锅腐蚀时正极的电极反应式: 。
II.氯碱工业中电解饱和食盐水的原理示意图如下图所示:

(1)溶液A的溶质是 ;
(2)电解饱和食盐水的离子方程式是 ;
(3)电解时用盐酸控制阳极区溶液的pH在2~3,用平衡移动移动原理解释盐酸的作用: 。
Ⅲ.(1)按右图电解氯化钠的稀溶液可制得漂白液,写出该电解池中发生反应的总反应方程式: ;

(2)将充分电解后所得溶液逐滴加入到酚酞试液中,观察到的(3)现象是 。
如图所示的电解装置中,乙池盛有200mL饱和CuSO4溶液,丙池盛有200mL饱和NaCl溶液.通电一段时间后,C极增重0.64g,则:

(1)P是电源的_________极。甲池中,A极的质量_________g。电解一段时间,甲池溶液的pH为_________。(2)D极的电极反应式为 ,丙池电解反应的总离子方程式为 。
相同状况下,D电极与E电极产生的气体体积比为_______________。
(3)若乙池溶液通电一段时间后,向所得的溶液中加入0.1mol的Cu(OH)2后恰好恢复到电解前的浓度。则电解过程中转移电子的数目为__________________。(用NA表示)
NH4NO3主要用作肥料、军用炸药、冷冻剂、制造笑气等。
(1)铵态氮肥NH4NO3________(填“能”或“不能”)与草木灰混合施用,用盐类水解的知识简述原因__________。
(2)NH4NO3受热分解温度不同,分解产物也不同。在185~200°C时,NH4NO3分解生成笑气(N2O)和水,分解生成的氧化产物与还原产物的质量比为__________。超过400°C,NH4NO3剧烈分解生成N2、NO2和H2O,并发生爆炸,若32g NH4NO3爆炸放出12.3 kJ的热量,则NH4NO3分解爆炸的热化学方程式为______________。
(3)电解NO制备 NH4NO3,其工作原理如图所示,阴极反应式为___________________;电解反应的总方程式为___________________;为使电解产物全部转化为NH4NO3,需补充物质A,A是__________。
电解原理在化学工业中有着广泛的应用。现将你设计的原电池通过导线与右图中电解池相连,其中,a为电解液,X和Y是两块电极板,则:

(1)若X、Y依次为铜和铁,a仍为CuSO4溶液,且反应过程中未生成Fe3+,则Y极的电极反应式为
(2)若用此装置电解精炼铜, 做阳极,电解液CuSO4的浓度 (填“增大”、“减小”或“不变”)。
(3)PbO2可以通过石墨为电极,Pb(NO3)2和Cu(NO3)2的混合溶液为电解液电解制取。阳极发生反应的电极反应式为 ;若电解液中不加入Cu(NO3)2,阴极发生的电极反应式为 。
(4)如图:A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸。

比较A、B、C中铁被腐蚀的速率,由快到慢的顺序为 (填字母序号)。
(18分)(1)某催化剂可将汽车尾气中的CO、NO转化为无毒气体。已知:
②可以利用反应: (n可以为零)将NO2变成无害N2,若要求X必须为无污染的物质,则G可以是_________(填写字母)。
(n可以为零)将NO2变成无害N2,若要求X必须为无污染的物质,则G可以是_________(填写字母)。
a.NH3 b.CO2 c.SO2 d.CH3CH2OH
当反应中转移1.2mol电子时,消耗NO2____________L(标准状况)。
③用NaOH溶液吸收工业尾气中的SO2最终制得石膏(CaSO4.2H2O)。为节约资源减少排放实现物质的循环利用,生产过程中还需要加入的固体物质是____________(填化学式)。
(2)工业上通过电解含NH4F的无水熔融物生产NF3气体,其电解原理如图所示。则a极为___________极,该极的电极反应式________________________________________
(3)用电镀法在铁板表面镀锌或锡可防腐,这种防止金属腐蚀的方法从原理上属于_______法。
碳及其化合物应用广泛。
I 工业上利用CO和水蒸汽反应制氢气,存在以下平衡:
CO(g)+H2O(g)  CO2(g)+H2(g)△H>0
CO2(g)+H2(g)△H>0
(1)向1L恒容密闭容器中注入CO(g)和H2O(g),830℃时测得部分数据如下表。则该温度下反应的平衡常数K=______________。
(2)相同条件下,向1L恒容密闭容器中,同时注入2mol CO、2mol H2O(g),1molCO2和1mo1H2,此时v(正 ) __________v(逆)(填“>”“=”或“<”)
(3)上述反应达到平衡时,要提高CO的转化率,可采取的措施是_______(填字母代号)。
| A.升高温度 |
| B.加入催化剂 |
| C.增大压强 |
| D.增加CO的浓度 |
E.及时分离出CO2
II 已知CO(g)+1/2 O2(g)=CO2(g) △H=一141 kJ·mol-1
2H2(g)+ O2(g)=2H2O(g) △H=一484 kJ·mol-1
CH3OH(1)+3/2O2(g)=CO2(g)+2H2O(g) △H=一726 kJ·mol-1
(4)用CO(g)、H2(g)化合制得液态甲醇的热化学方程式为___________________________。
III某同学设计了一个甲醇燃料电池,并用该电池电解100mL一定浓度NaCl与CuSO4混合溶液,其装置如图:
(5)写出甲中通入甲醇这一极的电极反应式__________________________________ 。
(6)理论上乙中两极所得气体的体积随时间变化的关系如丙图所示(气体体积已换算成标准状况下的体积),写出在t1后,石墨电极上的电极反应式____________,原混合溶液中CuSO4的物质的量浓度____________mol/L。(假设溶液体积不变)
(7)将在t2时所得的溶液稀释至200mL,该溶液的pH约为___________。
下图所示装置中,甲、乙、丙三个烧杯依次分别盛放100g 5.00%的NaOH溶液、足量的CuSO4溶液和100g 10.00%的K2SO4溶液,电极均为石墨电极。
(1) 接通电源,经过一段时间后,测得丙中K2SO4浓度为10.47%,乙中c电极质量增加。据此回答问题:
①电源的N端为  极;
极;
②电极b上发生的电极反应为 ;
③计算电极b上生成的气体在标准状态下的体积: ;
④电极c的质量变化是 g;
⑤电解前后各溶液的PH大小是否发生变化(填变大、变小、不变):
甲溶液 ; 乙溶液  ;丙溶液
;丙溶液
(2)如果电解过程中铜全部析出,此时电解能否继续进行,为什么?

试题篮
()