有机合成中常用的钯/活性炭催化剂若长期使用,会被铁、有机化合物等杂质污染而失去活性,成为废催化剂。一种由废催化剂制取PdCl2的工艺流程如下:
(1)“焙烧1”通入空气的目的是 。
(2)甲酸在反应中被氧化为二氧化碳,写出甲酸与PdO反应的化学方程式 。
(3)加入浓氨水的过程中,需要控制溶液的pH为8~9,实验室中检测溶液pH的简单方法是 。
(4)写出“焙烧2”发生反应的化学方程式: 。
(5)Pd中加入王水的反应可以表示为:Pd+HCl+HNO3 → A+B↑+H2O(未配平)。其中B为无色有毒气体,该气体在空气中不能稳定存在;A中含有三种元素,其中Pd元素的质量分数为42.4%,H元素的质量分数为0.8%。则A的化学式为: 。
大家知道葡萄糖在乳酸菌的催化作用下,可以生成乳酸,其分子式是C3H6O3。无色透明的乳酸溶液能使紫色石蕊溶液变红色;能够在加热、浓硫酸做催化剂的条件下与乙酸进行酯化反应,则
(1)①乳酸中含有官能团的名称是__________、__________:
②若乳酸中还含有一个甲基(—CH3),则乳酸的结构简式为 ___________________。
(2)写出足量的钠与乳酸反应的化学方程式____________________________________________,
(3)写出乳酸在加热、浓硫酸做催化剂的条件下与乙酸反应的化学方程式_________________。
尼泊金酯是国际上公认的广谱性高效防腐剂,被广泛应用于食品、医药和化妆品的防腐等领域。某尼泊金酯W在酸性条件下水解,可生成分子式为C7H6O3的有机物A和分子式为C3H8O的醇B。A的红外光谱表征到了羧基、羟基和苯环的存在,核磁共振氢谱表明其有4种不同化学环境的氢原子,且峰面积比为1∶2∶2∶1。
(1)W的分子式为 。
(2)B的结构简式可能为 、 。为确定B的结构,可采用下列方法中的 (填序号)。
a.检验能否与金属Na反应生成H2
b.核磁共振氢谱法
c.检验被氧气催化氧化的产物能否发生银镜反应
(3)写出A与足量NaOH溶液反应的化学方程式 。
(4)写出同时满足下列条件的W的一种同分异构体结构简式 。
a.分子中不含甲基且苯环上有两个对位取代基
b.属于酯类
c.遇FeCl3溶液显紫色
某有机物A的结构简式为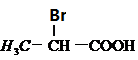 ,请回答下列问题。
,请回答下列问题。
(1)A中所含官能团的名称是___________、___________;
(2)A可能发生的反应有___________(填序号);
①取代反应②消去反应③水解反应④酯化反应
(3)将A与氢氧化钠的乙醇溶液混合并加热,再让得到的主要产物发生加聚反应,生成了某聚合物,该聚合物的结构简式是_____________________________。
(14分,每空2分)某有机物A能与NaOH溶液反应,其分子中含有苯环,相对分子质量为136,其中含碳的质量分数为70.6%,氢的质量分数为5.9%,其余为氧。
(1)A的分子式是 。
若A能与NaHCO3溶液反应放出CO2气体,其结构有 种。
(3)若A与NaOH溶液在加热时才能反应,且1mol A消耗1mol NaOH,则A的结构简式可能是 或者是 。
(4)若A与NaOH溶液在加热时才能反应,且1mol A消耗2mol NaOH,则符合条件的A的结构可能有 种,其中能发生银镜反应的有 种,不能发生银镜反应的物质的结构简式是 。
(本题共15分)在实验室可以在试管A中加入3 mL 乙醇,然后边振荡试管边慢慢加入2 mL浓硫酸和2 mL 乙酸,按下图所示(挟持和加热仪器略去)连接好装置进行实验,以制取乙酸乙酯。回答下列问题:
(1)浓硫酸的主要作用是①________,②________。
(2)试管B中盛放的溶液是________,B中通蒸气的导管不能插入溶液中目的是_______。
(3)做此实验时,有时还向A试管里加入几块碎瓷片,其目的是________。
(4)制取乙酸乙酯的反应方程式是_____________,反应类型_ 。
(5)长的玻璃导管的作用是_ 。
(6)实验完成后,观察到试管B的液面上有透明的不溶于水的油状液体产生。可通过________(填操作名称)的方法进行分离。
(7)若要分离沸点不同且互溶的液体,该操作名称________。
(8)实验室可用乙醇来制取乙烯,将生成的乙烯通入溴的四氯化碳溶液,反应后生成物的结构简式是_______________,反应类型是_________,请写出由乙醇制取乙烯的化学方程式 。
(7分)在下列物质中选择相应的序号填空:
①甲烷 ②乙烯 ③乙炔 ④甲苯 ⑤1-丁醇 ⑥乙酸乙酯 ⑦甘氨酸
Ⅰ.分子结构为正四面体的是 ;
Ⅱ.分子中中心原子采取sp杂化的是 ;
Ⅲ.能发生水解反应的是 ;
Ⅳ.能与溴水反应并使其褪色的是 ;
Ⅴ.分子与分子之间存在氢键的是 ;
Ⅵ.能发生消去反应的是
Ⅶ.与酸或碱都能反应生成盐的是 。
有机物A常用于食品行业。已知9.0 g A在足量O2中充分燃烧,混合气体依次通过足量的浓硫酸和碱石灰,分别增重5.4 g和13.2 g,经检验剩余气体为O2。
(1)A分子的质谱图如下图所示,从图中可知其相对分子质量为_____,则A的分子式是______________________。
(2)A能与NaHCO3溶液发生反应,A一定含有的官能团名称是______________。
(3)A分子的核磁共振氢谱有4个峰,峰面积之比是1:1:1:3,则A的结构简式是_________________________________。
(4)0.1 mol A与足量Na反应,在标准状况下产生H2的体积是__________L。
(5)A在一定条件下可聚合得到一种聚酯,用于制造手术缝合线,其反应的化学方程式是_______________________________________________________________。
(7分)某有机物的结构简式为HOOC—CH=CHCH2OH。
①请你写出该有机物官能团的名称: 、 、 。
②验证该有机物中含有-COOH官能团常采用的方法 ,产生的现象为 。
③请你写出该有机物与氢气反应的化学方程式:
回答下列问题:
(1)用乙炔制备聚氯乙烯(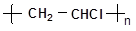 )(自行选择无机原料),
)(自行选择无机原料),
请书写化学反应方程式:_____ __;____ ____。
(2实验室用乙醇制乙烯的反应方程式为________。其反应类型为________。检验生成的乙烯要将导管先后通入______、_________。(填试剂名称)
(3)由溴乙烷为原料合成1,2-二溴乙烷(自行选择无机原料),
请书写化学反应方程式:____ ___;____ ____。
(4) 能发生反应生成一种含五元环的化合物,请书写化学反应方程式_______。
能发生反应生成一种含五元环的化合物,请书写化学反应方程式_______。
第(1)小题每空1分第(2)小题每空3分
(1)用工业酒精制造的假酒中通常含有 ;福尔马林溶液的溶质是 ;非典型肺炎流行期间,为了杀灭空气中病菌人们常通过熏_ (某种酸)作为家庭预防手段之一。(写出物质的结构简式)
(2)在某有机物A的分子中,具有酚羟基、醇羟基、 羟基等官能团,其结构简式如下图。
A跟NaOH溶液反应的化学方程式是
②A跟NaHCO3溶液反应的化学方程式是
③A在一定条件下跟Na反应的化学方程式是:
目前世界上已证明“达菲”是治疗禽流感和甲型H1N1流感的良方。“达菲”的主要合成原料是我国盛产的莽草酸。从八角茴香中提取的莽草酸经过多次反应和其他工艺制成“达菲”颗粒。下图是莽草酸和“达菲”有效成分的键线式结构(楔形实线、虚线表示基团的立体结构)。
(1)“达菲”的相对分子质量为410.4,扣除H3PO4后的部分称为“自由基奥司他韦”。试求“自由基奥司他韦”的相对分子质量________;“自由基奥司他韦”能与磷酸结合,说明氨基具有________性。
(2)莽草酸中含有的官能团有__________________________(写名称)。
(3)下列有关莽草酸的说法中正确的是____________________________。
①分子式为C7H10O5
②能使FeCl3溶液显紫色
③能使溴的四氯化碳溶液褪色
④l mol莽草酸与分别足量的Na和NaOH反应,消耗的Na和NaOH的物质的量之比为4:l
(4)莽草酸与C2H5OH发生酯化反应的化学方程式是_________________。
(5)莽草酸在浓硫酸作用下加热可得到B(C7H6O3),B的同分异构体中既含有酚羟基又含有酯基的共有______种,写出其中一种同分异构体的结构简式 。
A、B、C、D四种有机物具有支链的化合物A的结构简式为 ,A可以使Br2的四氯化碳溶液褪色,也能与乙醇反应。
,A可以使Br2的四氯化碳溶液褪色,也能与乙醇反应。
(1)写出A与Br2的四氯化碳溶液反应的类型 ;A与乙醇反应的条件 。
(2)写出与A具有相同官能团的同分异构体的结构简式:
、 。
(3)已知碳碳双键的碳原子上连接羟基是不稳定的,请写出两种下列要求的A的同分异构体的结构简式(①能发生银镜反应、也能与金属钠反应产生气体 ②能发生银镜反应、但不能与金属钠反应产生气体):
、 。
“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯。回答下列问题:
(1)写出制取乙酸乙酯的化学反应方程式 。
(2)浓硫酸的作用是:① ;② 。
(3)饱和碳酸钠溶液的主要作用是 。
(4)装置中通蒸气的导管要插在饱和碳酸钠溶液的液面上,不能插入溶液中,目的是 。
(5)若要把制得的乙酸乙酯分离出来,应采用的实验操作是 。
试题篮
()