下列离子方程式的书写正确的是( )
| A.实验室用大理石和稀盐酸制取CO2:2H++CO32-=CO2↑+H2O |
| B.向氯化亚铁溶液滴加新制氯水:2Fe2++Cl2=2Fe3++2Cl- |
| C.向AlCl3溶液中加入过量的NaOH溶液:Al3++3OH-=Al(OH)3↓ |
| D.铁和稀盐酸反应:2Fe+6H+=3H2↑+2Fe3+ |
用NA表示阿伏伽德罗常数的值,下列叙述正确的是( )
| A.18g水中所含的电子数为8NA |
| B.常温常压下,28g氮气所含的原子数为2NA |
| C.0.5molCuO的摩尔质量为40g/mol |
| D.22.4L甲烷(CH4)所含的原子数为5NA |
下列反应不能观察到“既有沉淀析出,又有气体产生”现象的是( )
| A.金属钠和硫酸铜溶液 | B.过氧化钠和氯化镁溶液 |
| C.氧化钠和氯化铵溶液 | D.硫酸铵和氢氧化钡混合加热 |
当光束通过下列分散系时,能观察到丁达尔效应的是( )
| A.泥水 | B.盐酸 | C.Fe(OH)3胶体 | D.NaCl溶液 |
光纤通信是一种现代化的通信手段,制造光纤的主要原料是( )
| A.CaCO3 | B.CaO | C.Na2CO3 | D.SiO2 |
利用右图装置进行下列实验,不能得出相关实验现象的是
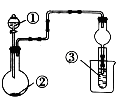
| 选项 |
① |
② |
③ |
④ |
| A |
浓盐酸 |
Na2SO3 |
BaCl2溶液 |
出现浑浊 |
| B |
稀盐酸 |
石灰石 |
饱和Na2CO3溶液 |
出现浑浊 |
| C |
浓氨水 |
生石灰 |
酚酞溶液 |
出现红色 |
| D |
醋酸 |
贝壳 |
澄清石灰水 |
先浑浊后澄清 |
为检验某溶液中的离子,下列操作方法及结论正确的是
| A.加入氯水,再加入KSCN溶液,溶液显红色,则溶液中一定含有Fe2+ |
| B.加入盐酸,产生无色无味且能使澄清石灰水变浑浊的气体,则溶液中一定含有CO32- |
| C.加入Ba(NO3)2溶液,再加入稀盐酸,产生白色沉淀,则溶液中一定含有SO42- |
| D.加入NaOH溶液并加热,产生使湿润的红色石蕊试纸变蓝的气体,则溶液中一定含有NH4+ |
下列事实与胶体性质无关的是
| A.豆浆中加入CaSO4制豆腐 |
| B.清晨在茂密的森林里看到缕缕阳光穿过林木枝叶 |
| C.FeCl3溶液中加入NaOH溶液产生红褐色沉淀 |
| D.使用钢笔时不宜将不同品牌的墨水混用 |
实验室里需储存在棕色试剂瓶中的是
A.金属钠 B浓硝酸 C.FeSO4溶液 D.浓硫酸
a为乙二胺四乙酸(EDTA),易与金属离子形成螯合物。b为EDTA与Ca2+形成的螯合物。下列叙述正确的是( )

A.a和b中的N原子均为sp3杂化
B.b中Ca2+的配位数为4
C.b含有分子内氢键
D.b含有共价键、离子键和配位键
PCl5和AlCl3形成的加合物PCl5·AlCl3由[PCl4]+和[AlCl4]-构成。下列有关该加合物的叙述正确的是( )
| A.属于分子晶体 | B.[PCl4]+空间构型为正四面体 |
| C.阴阳离子均含有配位键 | D.固态可导电 |
下表是A、B、C、D、E、F六种短周期元素的部分化合价、电负性和原子半径数据。下列说法正确的是( )
| |
A |
B |
C |
D |
E |
F |
| 化合价 |
+1 |
-2 |
-1 |
-2 |
-1 |
+1 |
| 电负性 |
2.1 |
2.5 |
3.0 |
3.5 |
4.0 |
0.9 |
| 原子半径/nm |
0.037 |
0.102 |
0.099 |
0.073 |
0.071 |
0.154 |
A.A的单质中含有金属键 B.F2D2含有非极性共价键
C.沸点:A2D<AE D.最高价氧化物对应水化物的酸性:B>C
乙烯通过一步反应不能制取的物质是( )
| A.CH3CH2OH | B.CH3CH2Cl | C.CH2BrCH2Br | D.CH2=CHCl |
徐光宪在《分子共和国》一书中介绍了许多明星分子,如H2O2、CO2、BF3、CH3COOH等。下列说法正确的是( )
| A.H2O2分子的空间构型为直线形 | B.CO2分子为非极性分子 |
| C.BF3分子中的B原子满足8电子稳定结构 | D.CH3COOH分子中C原子均为sp2杂化 |
两种金属粉末的混合物9g与足量的稀硫酸反应收集到标准状况下的氢气6.72L,则这种混合物的可能组成是( )
| A.Mg和Al | B.Fe和Zn | C.Fe和Cu | D.Fe和Al |
试题篮
()