为除去铜粉中混有的少量铝粉,下列试剂不可行的是
| A.CuCl2溶液 | B.稀硝酸 | C.NaOH溶液 | D.稀盐酸 |
下列电离方程式书写正确的是
| A.Na3PO4═3Na++P5++4O2﹣ | B.H2SO4═H++SO42﹣ |
| C.NH3•H2O⇌NH4++O2﹣+H+ | D.NH4NO3═NH4++NO3﹣ |
下列变化过程中,没有发生化学变化的是
| A.铝的钝化 | B.光合作用 | C.碘的升华 | D.海水提溴 |
硅酸钠的水溶液俗称“水玻璃”,是建筑行业经常使用的一种黏合剂.硅酸钠属于
| A.盐 | B.氧化物 | C.碱 | D.酸 |
相等物质的量的KClO3分别发生下述反应:①有MnO2催化剂存在时,受热分解得到氧气;②若不使用催化剂,加热至470℃左右,得到KClO4(高氯酸钾)和KCl.下列关于①和②的说法不正确的是
| A.都属于氧化还原反应 | B.发生还原反应的元素相同 |
| C.发生氧化反应的元素不同 | D.生成KCl的物质的量为2:1 |
已知2Fe3++2I﹣=I2+2Fe2+、Br2+2Fe2+=2Fe3++2Br﹣.现向含有FeBr2、FeI2的某溶液中通入一定量的氯气,再向反应后的溶液中滴加少量的KSCN溶液,结果溶液变为红色,则下列叙述中正确的是
①按Br2、Fe3+、I2的顺序氧化性逐渐减弱
②原溶液中Br﹣一定被氧化
③通入氯气后原溶液中的Fe2+一定被氧化
④不能确定通入氯气后的溶液中是否还存在Fe2+
⑤若取少量所得溶液,加入CCI4后静置,向上层溶液中加入足量的AgNO3溶液,只产生白色沉淀,说明原溶液中Fe2+、Br﹣均被完全氧化.
| A.①②③④ | B.①③④⑤ | C.②④⑤ | D.①②③④⑤ |
现有常温下的四份溶液:①0.01mol•L﹣1 CH3COOH溶液;②0.01mol•L﹣1盐酸;③pH=12的氨水;④pH=12的NaOH溶液.下列说法正确的是
| A.①中水的电离程度最小,③中水的电离程度最大 |
| B.等体积的①、②、④溶液分别与足量铝粉反应,生成H2的量:④最大 |
| C.将四份溶液稀释相同倍数后,溶液的pH:③>④,②>① |
| D.将②、③混合,若pH=7,则消耗溶液的体积:②<③ |
设NA表示阿伏加德罗常数的值,下列说法正确的是
| A.5.6 g Fe和足量的盐酸完全反应失去电子数为0.3 NA |
| B.64g SO2含有NA个SO2分子 |
| C.16g CH4所含的电子数为NA |
| D.标况下,4.48L的水中含有H2O分子的数目为0.2NA |
下列说法正确的是
| A.金属在反应中只能作还原剂,非金属在反应中只能作氧化剂 |
| B.氧化剂在反应中失去电子,还原剂在反应中得到电子 |
| C.氧化剂具有氧化性,还原剂具有还原性 |
| D.阳离子只有氧化性,阴离子只有还原性 |
丁香油酚的结构简式为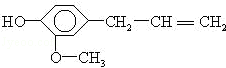 据此结构分析,下列说法正确的是
据此结构分析,下列说法正确的是
| A.可以燃烧,只能与溴水发生加成反应 |
| B.可与NaOH溶液反应,也可与FeCl3溶液反应 |
| C.不能与金属钠反应放出H2 |
| D.可以与小苏打溶液反应放出CO2气体 |
关于海水综合利用问题,下列说法错误的是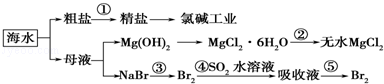
| A.从能量转换角度来看,氯碱工业中的电解饱和食盐水是一个将电能转化为化学能的过程 |
| B.在过程②中若要获得无水MgCl2不可直接蒸干灼烧 |
| C.除去粗盐中杂质(Mg2+、SO42﹣、Ca2+),加入的药品顺序为:NaOH溶液→Na2CO3溶液→BaCl2溶液→过滤后加盐酸 |
| D.第③④步的目的是为了浓缩富集溴 |
在标准状况下,将wgA气体(摩尔质量为Mg/mol)溶于1L水中,所得溶液密度为dg/mL,则此溶液的物质的量浓度为mol/L.
A.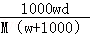 |
B.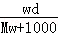 |
C.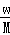 |
D.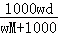 |
试题篮
()