除去下表内各物质中含有的少量杂质,写出除杂试剂,并填写分离方法。
| 序号 |
物质 |
杂质 |
所加试剂 |
分离方法 |
| (1) |
NO |
NO2 |
|
|
| (2) |
Fe粉 |
Al粉 |
|
|
| (3) |
氯化钠固体 |
氯化铵固体 |
|
|
有下列物质:①H2SO4;②金属铜;③Al2O3;④漂白粉;⑤蔗糖;⑥醋酸;⑦NO;⑧SiO2。
(1)请用序号填写空白:以上物质中属于混合物的是____________;能导电的是____________;属于弱电解质的是____________;能引起光化学烟雾的是____________;属于两性氧化物的是 ;可用作光导纤维原料的是 。
(2)写出H2SO4在水中的电离方程式: 。
(3)写出Al2O3溶于NaOH溶液的离子方程式:____________。
为确定SO2、CO2、Cl2的混合气体的各种成分,小龙同学做了如下探究。
(1)三种气体都具有的性质是___________(填字母);
A.漂白性和氧化性 B.水溶液显酸性 C.能与碳酸钠溶液反应 D.能与非金属单质反应
(2)通过观察颜色,可以确定混合气体中含有_________,为了检验另两种气体,可以将混合气体通过下列试剂中的_____________________(填字母)洗去该气体;
A.氢氧化钠溶液 B.饱和食盐水 C.硫化氢溶液 D.四氯化碳
(3)确定另外两种气体的成分时,需要依次通过A、B、C、D四个洗气瓶:
A.品红溶液 B.酸性高锰酸钾溶液 C.品红溶液 D.澄清石灰水
①能说明混合气体中含有CO2的实验现象是_______________________________;
②B中溶液紫红色褪去产生Mn2+和SO42-写出此反应的离子反应方程式_______________________。
用化学方程式解释下列问题
(1)久置氯水不能使有色布条褪色:_____________________________;
(2)被SO2漂白的品红溶液中通入氯气后先复色再褪色,解释“复色”的原因:______________;
(3)氢氟酸不能用玻璃瓶储存:_________________________________;
(4)饱和亚硫酸钠溶液能吸收SO2________________________________;
(5)氯化铁溶液能吸收硫化氢___________________________________。
H1N1病毒是一种没有超常抵抗力的病毒。研究证明,许多常用消毒药物如漂粉精、漂白粉、高锰酸钾等,可以将H1N1病毒杀灭。
(1)工业上制取漂白粉的反应方程式为__________________________;
(2)将漂白粉溶于适量水中,呈白色浊状物,静置沉降.取少许上层清液,滴加碳酸钠溶液出现白色沉淀,写出其中反应的离子方程式____________________;另取少许上层清液,滴加适量的_____________(填化学式)即可检验Cl-的存在,发生反应的化学方程式为___________________;
(3)漂白粉在空气中长期放置,会失效,用化学方程式解释其原因_______________________。
亚氯酸钠(NaClO2)一种高效氯化剂、漂白剂,在NaOH溶液中ClO2与H2O2反应可以得到亚氯酸钠。
(1)ClO2中氯元素的化合价是_____________;在制备亚氯酸钠的反应中ClO2做_____________(填“氧化剂”或“还原剂”);若反应中生成1molNaClO2,转移电子物质的量为___________mol;
(2)写出该反应的化学方程式为_____________;
(3)科学家经研究发现NaClO2也可用于制取自来水消毒剂ClO2。2NaClO2+Cl2═2ClO2+2NaCl,还原产物为___________,用单线桥法标出电子转移的方向和数目。
将29g混合均匀的铁粉和硫粉置于密闭容器中加热,充分反应后冷却至室温,再跟足量稀盐酸反应,产生气体在标准状况下为8.4L,则混合物中铁和硫的物质的量之比为________。若使上述气体充分燃烧,可消耗标准状况下氧气的体积为___________。
在25 ℃时,用石墨电极电解2.0 L 0.5mol·L-1 CuSO4溶液。5min后,在一个石墨电极上有6.4 g Cu生成。试回答下列问题。
(1)发生氧化反应的是__________极,电极反应式为____________。
(2)若电解后溶液的体积不变,则电解后溶液的pH为____________。
(3)若将溶液恢复到与电解前一样,则需加入________mol的_______。
(1)写出下列化合物的结构简式
2,2,3,3,-四甲基戊烷:__________________________。
(2)①写出Na2CO3溶液与AlCl3溶液反应的离子方程__________________________。
②写出由甲苯制备TNT的化学方程式:__________________________。
③Na2CO3溶液显碱性,用离子方程式表示原因___________,其溶液中离子浓度大小顺序为___________。
(3)除去括号中的杂质,填上适宜的试剂和提纯方法
乙醇(水):__________、_________。
(4)甲烷燃料电池(在KOH环境中)的负极的电极反应式:___________________。
(5)将煤转化为煤气的主要化学反应为:C(s)+H2O(g)===CO(g)+H2(g)
C(s)、CO(g)和H2(g)完全燃烧的热化学方程式为:
C(s)+O2(g)===CO2(g) ΔH=-393.5 kJ/mol
H2(g)+ O2(g)===H2O(g) ΔH=-242.0 kJ/mol
O2(g)===H2O(g) ΔH=-242.0 kJ/mol
CO(g)+ O2(g)===CO2(g) ΔH=-283.0 kJ/mol
O2(g)===CO2(g) ΔH=-283.0 kJ/mol
根据以上数据,写出C(s)与水蒸气反应的热化学方程______________________。
工业制纯碱广泛采用的两种生产流程可以用以下示意图简要表示。
完成下列填空:
(1)用甲流程生产纯碱的方法称为_________________法。
(2)沉淀池中发生反应的化学方程式为_______________________________。
(3)T是________; W中除Ca(OH)2外,溶质的主要成分是_________(均填化学式)。
(4)甲流程中设计循环I的目的是________________;乙流程中设计循环I的目的是_____________。
(5)在乙流程中,若通入NH3 44.8 L(已折合成标准状况下)可以得到纯碱100.0 g,则NH3的利用率为__________。
(6)若制碱厂欲利用产生的氯化钙废液制取硝酸钙(Ca(NO3)2·4H2O),设计一个经济可行的方案,用流程图表示。
(1)合理膳食,保持营养均衡,是青少年学生健康成长的重要保证。
①维生素C能增强人体对疾病的抵抗能力,促进人体生长发育,中学生每天要补充60mg的维生素C。下列物质含有丰富维生素C的是 (填字母)。
A.牛肉 B.辣椒 C.鸡蛋
②青少年及成人缺乏某种微量元素将导致甲状腺肿大,而且会造成智力损害,该微量元素是 (填字母)
A.碘 B.铁 C.钙
③蛋白质是人体必需的营养物质,它在人体内最终分解为 (填字母)。
A.葡萄糖 B.氨基酸 C.脂肪酸
(2)材料是人类生存和发展的物质基础,合理使用材料可以改善我们的生活。
①居室装修所使的人造板材会释放出一种挥发性物质,长期接触会引起过敏性皮炎,免疫功能异常,该挥发性物质是 。
②玻璃是重要的硅酸盐产品。生产玻璃时,石灰石与石英反应的化学方程式为 。
③铁是人们生活中常用的金属材料,请列举两种防止铁制品被腐蚀的方法: , 。
(3)保持洁净安全的生存环境已成为全人类的共识,人与自然要和谐相处。
①pH< 的雨水称为酸雨;向煤中加入适量的 ,可以大大减少燃物产物中SO2的量。
②对汽车加装尾气催化净化装置,可以使其中的NO、CO相互反应转化成无毒的气体,其原理可以用化学方程式表示为 。
③天然水中杂质较多,常需加入明矾,ClO2等物质处理后才能饮用。加入ClO2的作用是 ;加入明矾后, 水解的离子方程式是 。
水解的离子方程式是 。
实验室里常用浓盐酸与二氧化锰反应来制取少量的氯气,现取一定量的浓盐酸使其与二氧化锰发生反应,产生的氯气在标准状况下的体积为22.4 L。
请回答下列问题:
(1)写出该反应的离子反应方程式______________________。
(2)参加反应的二氧化锰的质量为____________。
(3)反应中被氧化的HCl的物质的量为 ____________。
有关物质间转化关系如下图,试回答:
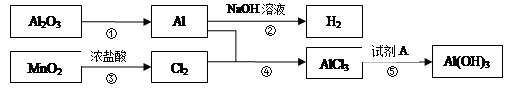
据此判断:
(1)转化①的反应条件为 。
(2)转化②的化学方程式为 。
(3)若转化⑤用于实验室制Al(OH)3,则试剂A宜选择 填名称)。
(4)转化⑤的离子方程式为 。
某合作学习小组讨论辨析以下说法中正确的是
①硅是光导纤维的主要成分 ②CO2气体通入CaCl2溶液中会出现混浊
③冰和干冰既是纯净物又是化合物 ④某气体能使品红溶液褪色,该气体是SO2
⑤盐酸和食醋既是化合物又是酸 ⑥鉴别MgCl2、AlCl3、FeCl3溶液可用NaOH试剂
⑦豆浆、雾都是胶体 ⑧利用丁达尔效应可以区分溶液和胶体
试题篮
()