(1)由于SiH4具有易提纯的特点,因此硅烷热分解法是制备高纯硅很有发展潜力的方法。制备硅烷整个过程必须严格控制无水,否则生成的硅烷将发生变质,其化学方程式为 ,整个系统还必须与氧隔绝,其原因是 (用化学方程式表示)
(2)无机非金属材料是日常生活中不可缺少的物质,它们往往具有高强度、耐高温、耐腐蚀的特点。Si3N4就是一种重要的精细陶瓷,合成氮化硅的方法之一为: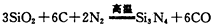 ,Si3N4属于原子晶体,在上述反应中氧化剂为
,Si3N4属于原子晶体,在上述反应中氧化剂为
(3)硅酸盐中,SiO44-四面体通过共用顶角氧离子可形成链状、层状、空间网状等结构型式。下图为一种无限长双链结构的多硅酸根,其中Si原子的杂化形式为 ,该多硅酸根化学式为

苯乙烯是重要的基础有机原料。工业中用乙苯(C6 H5- CH2 CH3)为原料,采用催化脱氢的方法制取苯乙烯(C6 H5- CH= CH2)的反应方程式为:

(1)向体积为VL的密闭容器中充入a mol乙苯,反应达到平衡状态时,平衡体系组成(物质的量分数)与温度的关系如图所示:

由图可知:在600℃时,平衡体系中苯乙烯的物质的量分数为25%,则:
①氢气的物质的量分数为 ;
②乙苯的平衡转化率为 ;
③计算此温度下该反应的平衡常数 。
(2)已知某温度下,当压强为101.3kPa时,该反应中乙苯的平衡转化率为30%;在相同温度下,若反应体系中加入稀释剂水蒸气并保持体系总压为101.3kPa,则乙苯的平衡转化率 30%(填“>、=、<” )。
(3)已知:

计算上述反应的ΔH= kJ/mol。
(1)某小组分析二氧化铅分解产物的组成,取478g的PbO2加热,PbO2在加热过程发生分解的失重曲线如下图所示,已知失重曲线上的a为96.66%,则a点固体的分子式为
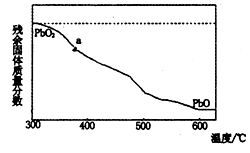
已知PbO2与硝酸不反应且氧化性强于硝酸,而PbO是碱性氧化物,能和酸反应,写出上述分解产物与硝酸反应的化学方程式
(2)①另一实验小组也取一定量的PbO2加热得到了一些固体,为探究该固体的组成,取一定质量该固体加入到30 mLCH3COOH一CH3COONa溶液中,再加入足量KI固体,摇荡锥瓶使固体中的PbO2与KI全部反应而溶解,得到棕色溶液。写出PbO2参与该反应的化学方程式 ,用淀粉指示剂,0.2 mol/L的Na2S2O3标准溶液滴定至溶液蓝色刚消失为止,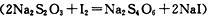 ,Na2S2O3标准溶液的消耗量为20 mL。
,Na2S2O3标准溶液的消耗量为20 mL。
②固体加入到醋酸而非盐酸中是因为会产生有毒气体,写出反应的化学方程式
用CH3COOH一CH3COONa的混合液而不用CH3COOH可以控制pH不至于过低,否则会产生浑浊和气体,请写出该反应的化学方程式
③取相同质量的上述固体与硝酸混合,过滤出的滤液加入足量的铬酸钾溶液得到铬酸铅(PbCrO2相对分子质量323)沉淀,然后 ,得固体质量为0.969g,依据上述数据,该固体的分子式 。
短周期元素形成的常见非金属固体单质A与常见金属单质B,在加热条件下反应生成化合物C,C与水反应生成白色沉淀D和气体E,D既能溶于强酸,也能溶于强碱。E在足量空气中燃烧产生刺激性气体G,G在大气中能导致酸雨的形成。E被足量氢氧化钠溶液吸收得到无色溶液F。溶液F空气中长期放置发生反应,生成物之一为H。H与过氧化钠的结构和化学性质相似,其溶液显黄色。
(1)单质A是一种黄色固体,组成单质A的元素在周期表中的位置是________________。用物理方法洗去试管内壁的A,应选择的试剂是_______________;化学方法洗去试管内壁的A是发生歧化反应生成两种盐,但这两种盐在强酸性条件下不能大量共存,请写出化学方法洗去试管内壁的A时发生的化学反应方程式______________________________。
(2)工业上获得B时常使用电解法,请写出阳极反应的电极反应_________________。
(3)FeCl3溶液中的Fe3+可以催化G与氧气在溶液中的反应,此催化过程分两步进行,请写出Fe3+参与的第一步反应的离子反应方程式_____________________________。
(4)工业上吸收E常用氨水,先生成正盐最终产物为酸式盐。E与该正盐反应的化学方程式___________________________.
(5)将D溶于稀硫酸,向恰好完全反应后所得的溶液中加入过量氢氧化钡溶液,则加入氢氧化钡溶液的过程中的现象是_____________________________。
(6)G与氯酸钠在酸性条件下反应可生成消毒杀菌剂二氧化氯。该反应的氧化产物为__________,当生成2mol二氧化氯时,转移电子___________mol。
(7)H的溶液与稀硫酸反应的化学方程式______________________________。
当前我国环境状况不容乐观,其中PM2.5、CO、S02、NOx等污染物对空气质量的影响非常显著,其主要来源为燃煤、机动车尾气等,因此,对其进行研究具有重要意义。
(1)对某地PM2.5样本用蒸馏水处理后,测得该试样中的化学组分及其平均浓度如下表:

根据表中数据计算该试样的pH=
(2)NOx是汽车尾气的主要污染物之一。汽车发动机工作时会引发N2和O2反应,其能量变化如图1所示。
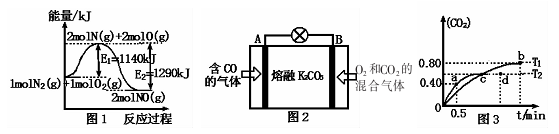
①写出N2和02反应的热化学方程式:________。
②有人设想将C0按下列反应除去:2CO(g)= 2C(s)+02(g)△H>O,请你分析该设想能否实现? (填“是”或“否”),依据是
③用图2所示原电池原理也可以除去CO,则其负极反应式为:________。
(3)有人设想利用反应NaOH+S02=NaHS03将SO2吸收除去,然后用石灰水又可使NaOH再生。再生的离子方程式为: 。
(4)利用I205消除CO污染的反应为:5CO(g)+I205(s)—兰5CO2(g)+I2(s),不同温度下,测得CO2的体积分数随时间t变化曲线如图3.则:
①该反应的化学平衡常数表达式为K=____ 。
②T1与T2化学平衡常数大小关系:K(T1)__________K(T2)(填“>”、“<”或“=”)
某硅铁矿中主要含Si02、Fe304、Al203、Cu0。某工厂用它为原料进行综合应用来制取硅胶、铁红、铝、胆矾晶体,设计如下工业流程图:
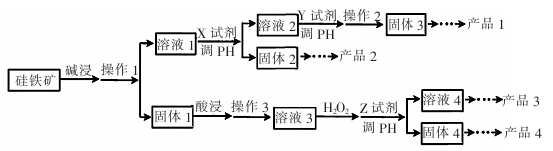
已知:Fe(OH)2、Fe(OH)3、Cu(OH)2完全沉淀的PH分别为9.6、3.7、9.4。
(1)碱浸时发生的离子反应方程式为:_
(2)为提高碱浸的浸出率,可采取的方法有 。(填两种即可)
(3)溶液3中加H2O2的目的是 。 对应的离子反应方程式为:________。
(4)Z试剂可以选用下列的 (填字母)
a. Cu b.CuO c.Cu(OH)2 d.CuCO3
(5)由溶液4制取产品3还要先加热到____(填字母)时,停止加热、冷却结晶。
| A.沸腾 |
| B.液体表面出现晶膜 |
| C.析出大量晶体 |
| D.快蒸干,还有少量液体 |
(6)判断固体4对应的元素沉淀完全的方法是:________________。
短周期主族元素A、B、C、D、E、F的原子序数依次递增,A、B两元素相邻,B、C、E原子的最外层电子数之和为13,C原子最外层电子数是E原子最外层电子数的3倍,B、F原子最外层电子数之和等于C、E原子最外层电子数之和.请回答下列问题:
(1)B元素在元素周期表中的位置为 .
(2)元素C和D可形成两种化合物D2C、D2C2,其中均含有的化学键类型是 ;元素E、F形成的最高价氧化物对应水化物的碱性强弱关系为 > (填化学式).
(3)E的单质能与A的最高价氧化物发生置换反应,反应的化学方程式为 ;
(4)F的单质加入到D的最高价氧化物对应水化物的溶液中,发生反应的离子方程式为 .
空气质量日报中有一项重要检测指标是SO2的含量,结合所学知识回答下列问题。工业制硫酸的过程中,SO2催化氧化的原理:
2SO2(g)+O2(g)  2SO3(g) △H<0
2SO3(g) △H<0

(1)某温度下,测得SO2(g)的平衡转化率(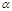 )与体系总压强( p )的关系如上图所示。a、b两点对应的平衡常数K(a) K(b) (填“>”“<”或“=”,下同)SO3浓度c(a) c(b)c点,反应速率υ(正) υ(逆)。
)与体系总压强( p )的关系如上图所示。a、b两点对应的平衡常数K(a) K(b) (填“>”“<”或“=”,下同)SO3浓度c(a) c(b)c点,反应速率υ(正) υ(逆)。
(2)将一定量的SO2(g)和O2(g)分别通入到体积为2L的恒容密闭容器中,在不同温度下进行,反应得到如下表中的两组数据:
| 实验编号 |
温度/℃ |
起始量/mol |
平衡量/mol |
||
| SO2 |
O2 |
SO2 |
O2 |
||
| 1 |
T1 |
4 |
2 |
x |
0.8 |
| 2 |
T2 |
4 |
2 |
0.4 |
y |
实验1从开始到反应达到化学平衡时,用去时间t 分钟,则υ(SO2)表示的反应速率为 ,温度T1大于T2的理由是 。
高锰酸钾(KMnO4)和过氧化氢(H2O2)是两种典型的氧化剂。
(1)H2O2的结构式为________________。
(2)下列物质中能使酸性KMnO4溶液褪色的是________(填选项字母)。
| A.臭碱(Na2S) | B.小苏打(NaHCO3) | C.水玻璃(Na2SiO3) | D.酒精(C2H5OH) |
(3)高锰酸钾、双氧水、活性炭常用于饮用水的处理,但三者联合作用时必须有先后顺序。
①在稀硫酸中,KMnO4和H2O2能发生氧化还原反应:
氧化反应:H2O2-2e-→2H++O2↑
还原反应:MnO4-+5e-+8H+→Mn2++4H2O
写出该氧化还原反应的离子方程式________________________________________。
②在处理饮用水时,活性炭应在高锰酸钾反应结束后投加,否则会发生反应:
4KMnO4+3C+H2O=4MnO2+2X+K2CO3,其中X的化学式为________。
二甲醚是一种重要的清洁燃料,也可替代氟利昂作制冷剂等,对臭氧层无破坏作用。工业上可利用煤的气化产物(水煤气)合成二甲醚。请回答下列问题:
(1)煤的气化过程中产生的有害气体H2S用Na2CO3溶液吸收,生成两种酸式盐,该反应的化学方程式为: 。
(2)利用水煤气合成二甲醚的三步反应如下:
① 2H2(g) + CO(g) CH3OH(g);ΔH =-90.8 kJ·mol-1
CH3OH(g);ΔH =-90.8 kJ·mol-1
② 2CH3OH(g) CH3OCH3(g) + H2O(g);ΔH=-23.5 kJ·mol-1
CH3OCH3(g) + H2O(g);ΔH=-23.5 kJ·mol-1
③ CO(g) + H2O(g) CO2(g) + H2(g);ΔH=-41.3 kJ·mol-1
CO2(g) + H2(g);ΔH=-41.3 kJ·mol-1
总反应:3H2(g) + 3CO(g) CH3OCH3(g) + CO2(g)的ΔH= ;一定条件下的密闭容器中,该总反应达到平衡,要提高CO的转化率,可以采取的措施是 (填字母代号)。
CH3OCH3(g) + CO2(g)的ΔH= ;一定条件下的密闭容器中,该总反应达到平衡,要提高CO的转化率,可以采取的措施是 (填字母代号)。
a.压缩体积 b.加入催化剂 c.减少CO2的浓度 d.增加CO的浓度 e.分离出二甲醚
(3)已知反应②2CH3OH(g) CH3OCH3(g) + H2O(g)某温度下的平衡常数为400。此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
CH3OCH3(g) + H2O(g)某温度下的平衡常数为400。此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:

① 比较此时正、逆反应速率的大小:v正 v逆 (填“>”、“<”或“=”)。
② 温度升高,该反应的平衡常数K (填“增大”、“减小”或“不变”)
如图所示装置,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极。将直流电源接通后,F极附近溶液呈红色。请回答:
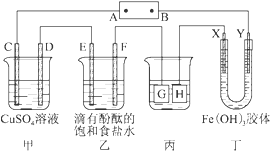
(1)B极是电源的 极。C电极上的电极反应式: 。
(2)若甲、乙装置中的C、D、E、F电极均只有一种单质生成时,对应单质的物质的量之比为 。
(3)现用丙装置给铜件镀银,则H应该是 (填“镀层金属”或“镀件”),电镀液是 溶液。当乙中溶液的pH=13时(此时乙溶液体积为500 mL),丙中镀件上析出银的质量为 。
(4)丁中X极附近的颜色逐渐变浅,Y极附近的颜色逐渐变深,这表明 ,在电场作用下向Y极移动。
某二元酸(化学式用H2B表示)在水中的电离方程式是:H2B = H++HB-,HB-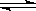 H++B2-
H++B2-
回答下列问题:
(1)Na2B溶液显 (填“酸性”“中性”或“碱性”),理由是 。(用离子方程式表示)
(2)在0.1 mol·L-1 Na2B溶液中,下列粒子浓度关系式正确的是 。
| A.c(Na+)+(OH-)=c(H+)+c(HB-) |
| B.c(Na+)+c(H+)=c(OH-)+c(HB-)+2c(B2-) |
| C.c(Na+)=2c(B2-)+2c(HB-) |
| D.c(B2-)+ c(HB-)=0.1mol·L-1 |
(3)已知0.1 mol·L-1 NaHB溶液的pH=2,则0.1mol·L-1 H2B溶液中氢离子的物质的量浓度可能是 0.11 mol·L-1(填“<”“>”或”=”),理由是 。
(4)0.1 mol·L-1 NaHB溶液中各种离子浓度由大到小的顺序是 。
明矾石经处理后得到明矾[KAl(SO4)2·12H2O]。从明矾制备Al、K2SO4和H2SO4的工艺过程如下所示:
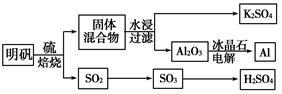
焙烧明矾的化学方程式为:4KAl(SO4)2·12H2O+3S 2K2SO4+2Al2O3+9SO2↑+48H2O
2K2SO4+2Al2O3+9SO2↑+48H2O
请回答下列问题:
(1)在焙烧明矾的反应中,还原剂是 。
(2)从水浸后的滤液中得到K2SO4晶体的方法是 。
(3)以Al和NiO(OH)为电极,NaOH溶液为电解液组成一种新型电池,放电时NiO(OH)转化为Ni(OH)2,该电池反应的化学方程式是 。
利用氮气、氢气在一定条件下生成氨气这一可逆反应来合成氨,是一个重要的化工反应。常用来生产液氨和氨水。
完成下列填空:
(1)右图表示合成氨时生成1mol生成物时的能量变化,E的单位为kJ。请写出合成氨的热化学方程式 (热量用E1、E2或E3表示)。

该图中的实线与虚线部分是什么反应条件发生了变化? 。
(2)在一定温度下,若将4amol H2和2amol N2放入VL的定容密闭容器中,2分钟后测得N2的转化率为50%,则该段时间用H2表示的反应速率为 摩尔/(升–秒)。若此时再向该容器中投入a mol H2、amol N2和2amol NH3,判断平衡移动的方向是 (填“正向移动”“逆向移动”或“不移动”)。
(3)液氨和水类似,也能电离:2NH3 NH4++ NH2-,某温度时,其离子积K=2×l0-30。该温度下:①将少量NH4Cl固体加入液氨中,K 2×10-30(填“<”、“>”或“=”);
NH4++ NH2-,某温度时,其离子积K=2×l0-30。该温度下:①将少量NH4Cl固体加入液氨中,K 2×10-30(填“<”、“>”或“=”);
②将少量金属钠投入液氨中,完全反应后所得溶液中各微粒物质的量大小排列为:
(4)工厂生产的氨水作肥料时需要稀释。用水稀释0.1mol/L稀氨水时,溶液中随着水量的增加而减少的是 。
a.c(NH4+)/c(NH3•H2O) b.c(NH3•H2O)/c(OH-)
c.c(OH-)/c(H+) d.c(H+)/c(NH4+)
硫化钠是一种重要的化工原料。工业上用硫酸钠与碳反应得到硫化钠。反应方程式如下:
Na2SO4 + 2C Na2S + CO2↑
Na2S + CO2↑
完成下列填空:
(1)上述反应的元素中,原子半径最小的元素的原子有 种能级不同的电子。
(2)下列可以证明二氧化碳是非极性分子的事实是 (填编号)
a.二氧化碳密度比空气大
b.二氧化碳能溶于水
c.二氧化碳在电场中通过不偏向
d.二氧化碳常温常压下为气态
(3)硫化钠在一定条件下会与硫单质反应生成多硫化钠(Na2SX)。在碱性溶液中,Na2SX与NaBrO3反应生成Na2SO4与NaBr。若Na2SX与NaBrO3反应的物质的量之比为3:16,则 x = 。
(4)写出硫氢化钠与少量硫酸铜溶液反应的离子方程式 。能否用硫酸铜溶液来鉴别硫化钠溶液和硫氢化钠溶液?请简述实验操作和现象并说明自己的观点: 。
(5)已知:H2S Ki1 = 9.1×10-8 Ki2 = 1.1×10-12 HF Ki = 3.5×10-4
H2SO3 Ki1 = 1.5×10-2 Ki2 = 1.0×10-7 HAc Ki = 1.75×10-5
若用右图的装置,用硫化钠固体和下列溶液制取硫化氢气体,可选用的试剂是 。

a.硝酸 b.亚硫酸氢钠 c.氢氟酸 d.醋酸
试题篮
()