有一包粉末状的混合物,可能含有MgCl2、FeCl3、NaOH、CuSO4、Al2(SO4)3、KNO3、CaCO3、NaCl中的两种或多种。将混合物置于水中搅拌,得无色透明溶液;再将所得无色透明溶液分为两份:一份中通入CO2,有白色沉淀出现,滴入稀盐酸沉淀消失;另一份中加入BaCl2溶液,同样有白色沉淀出现,此沉淀不溶于稀硝酸。完成下列问题:
(1)原混合物中肯定含有的物质是____________(写化学式)
(2)混合物置于水中,所得无色透明溶液中一定含有的物质是______________(写化学式)。
(3)常温下所得无色透明溶液的pH7(填“>”或“<”)。
(4)在所得无色透明溶液中有关离子方程式为___________________________________。
有A、B、C三种元素,已知5.75 g A单质跟盐酸完全反应,在标准状况下,可产生2.8 L(标准状况下)H2和0.25 mol ACln;B的气态氢化物的分子式是H2B,其相对分子质量与B的最高价氧化物的水化物相对分子质量比为1∶2.88,B核内质子数与中子数相等;C和B可形成CB2液态化合物,并能溶解B的单质,试完成下列问题:
(1)A、B、C的名称;A离子的结构示意图;B在周期表中的位置;CB2的分子式。
(2)用电子式表示A与B形成化合物的过程。
(8分)我国规定饮用水质量标准必须符合下列要求:pH为6.5—8.5,Ca2+和Mg2+总浓度小于0.004 5 mol·L-1,细菌总数小于100个每毫升。下图是源水处理成自来水的工艺流程示意图。

(1)源水中含Ca2+、Mg2+、 、Cl-等,加入石灰后,生成Ca(OH)2,进而发生多个复分解反应,请写出其中三个反应的离子方程式:①__________________;②__________________;③_________________________________。
、Cl-等,加入石灰后,生成Ca(OH)2,进而发生多个复分解反应,请写出其中三个反应的离子方程式:①__________________;②__________________;③_________________________________。
(2)凝聚剂除去悬浮固体颗粒的过程是______________________ (填序号)。
A.只是物理过程 B.只是化学过程 C.是物理和化学过程
(3)绿矾在水中最终生成______________________沉淀。
(14分)a、b、c、d、e、f、g为七种由短期周期元素构成的粒子,它们都有10个电子,其结构特点如下:
| 粒子代码 |
a |
b |
c |
d |
e |
f |
g |
| 原子核数 |
单核 |
单核 |
双核 |
多核 |
单核 |
多核 |
多核 |
| 电荷数(单位电荷) |
0 |
1+ |
1- |
0 |
2+ |
1+ |
0 |
其中b的离子半径大于e的离子半径;d是由极性键构成的四原子极性分子;c与f可形成两个共价型g分子。
试写出:
(1)a粒子的核外电子排布式 __________________________________________。
(2)b与e相应元素的最高价氧化物对应水化物的碱性强弱比较为:_______>_______ (用化学式表示)。
(3)d溶于水的电离方程式______________。
(4)g粒子所构成的晶体类型属______________。
(5)c粒子是___________,f粒子是___________ (用化学式表示)。
重庆开县的天然气矿“井喷”事故对人畜造成了极大的伤害。主要原因是喷发出的天然气中含有浓度较大的硫化氢气体,这种气体具有臭鸡蛋气味,有剧毒,其毒性原理为阻断机体细胞的内呼吸导致全身缺氧。由于中枢系统对缺氧敏感,因而首先受到损害。其爆炸极限为4.3%~45.5%,着火点为292℃。其相对分子质量为34,与空气的相对密度为1.2。
针对这次“井喷”事故,有专家提出如下现场处理措施:
(一)在井架入口、井架上、钻台边上、循环系统等处设置风向标,一旦发生紧急情况,作业人员可向1方向疏散。
(二)在含硫钻井地区的生产班当班人员每人配一套空气呼吸器2,另配一定数量的公用呼吸器,并做到人人会用、会维护、会检查。
(三)加强对钻井液中硫化氢浓度的测量,充分发挥除硫剂和除气器的功能,保持钻井液中硫化氢含量在15mg﹒m-3以下。当硫化氢含量超过20mg﹒m-3安全临界浓度3时,工作人员应佩戴空气呼吸器,不允许单独行动,派专人监护现场。
(四)钻井队在现场条件下不能实施井控作业,决定放喷时,放出天然气烧掉4。
放喷点火应派专人进行……
(1)如果你负责疏散群众,那么,受灾人员的疏散方向时
A.顺风向 B.逆风向 C.地势高的方向 D.地势低的方向
(2)空气呼吸器中可盛放的物质是
A.氢氧化钠 B.碱石灰 C.氯化钠 D.氨水
(3)检测人员从现场取出500mL,含H2S 0.01mol,则此时工作人员
A.可安全生产 B.必须佩戴空气呼吸器
C.迅速离开现场 D.无法确定
(4)①点燃天然气时应注意什么问题?
②点燃天然气实属无奈之举,因为此法并不能完全消除环境污染,为什么?
用氯气消毒的饮用水,会使水中的有机物发生氯化反应,生成有机含氯化合物,对人体有害,世界环保联盟建议推广采用高效氧化剂二氧化氯(ClO2)消毒。
(1)使用ClO2作饮用水消毒剂的优点是_____________________________。
(2)目前国外多用NaClO3与浓HCl反应制取ClO2,同时有Cl2生成,且体积为ClO2的一半,写出反应的化学方程式。__________________________________________________
(3)上述反应中产生0.1 mol Cl2,转移的电子的物质的量为_________ mol。
(4)在H2SO4酸性条件下,用Na2SO3还原NaClO3可制得ClO2,反应为:2NaClO3+Na2SO3 +H2SO4====2ClO2↑+2Na2SO4+H2O
这种方法的优点是____________________________________________________________。
甘蔗糖厂在生产过程中需要使用SO2气体,为此,需要在燃烧炉中燃烧硫磺(沸点为445℃)。在生产中发现如下情况:当液态硫表面上方3 mm左右空间的温度为360℃~380℃时,燃烧硫磺的火焰呈蓝色;当温度超过450℃,火焰呈白色,此时硫磺消耗的速度加快,但SO2产率明显降低,在输送SO2的管道中也随之出现较严重的堵塞。试解释其原因。
A、B、C是三种短周期元素,它们的原子序数依次增大。已知A是地壳中含量最多的元素;B元素原子的最外层只有一个电子;C元素的单质在常温下是黄绿色的气体。
(1)写出A、B的元素符号:A_________,B_________。
(2)写出C元素最高价氧化物对应水化物的化学式 。
已知:(X代表卤素原子,R代表烃基)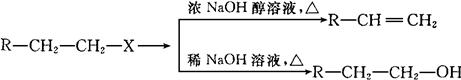
利用上述信息,按以下步骤从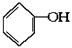 合成
合成 。(部分试剂和反应条件已略去)
。(部分试剂和反应条件已略去)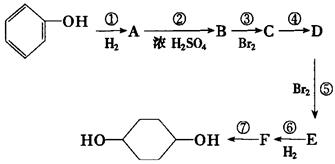
请回答下列问题:
(1)分别写出B、D的结构简式:B_________、D_________。
(2)反应①~⑦中属于消去反应的是____ _____。(填数字代号)
(3)如果不考虑⑥、⑦反应,对于反应⑤,得到的E可能的结构简式为:_________ 。
(4)试写出C D反应的化学方程式(有机物写结构简式,并注明反应条件)
D反应的化学方程式(有机物写结构简式,并注明反应条件)
。
已知:①A、B、C、D四种物质均含有元素X,可能还含有元素Y或Z。元素Y、X、Z的原子序数依次递增且都不超过20。② X在A、B、C、D中的化合价分别为0、-1、+1、+5。③室温下单质A与某种常见一元强碱溶液反应,可得到B和C。④化合物D在二氧化锰催化下受热分解,可制得元素Y的单质。请完成下列问题:
(1)写出元素X、Y、Z的元素符号:X___________,Y___________,Z___________。
(2)写出A、B、C、D的化学式:A___________,B___________,C___________,D___________。
(3)写出③中反应的化学方程式:
__________________________________________________。
(4)写出④中反应的化学方程式:
___________________________________________________。
m、n、x、y四种主族元素在周期表里的相对位置如下所示,已知它们的原子序数总和为46。
| m |
n |
|
|
| |
|
x |
y |
(1)m与y形成的化合物中含 键,属 分子(填“极性”或“非极性”)。
(2)由n、y的氢化物相互作用所生成的物质的电子式为 。
(3)写出m单质与x元素最高价氧化物对应的水化物反应的化学方程式为
。
(4)核电荷数比x元素少8的元素可形成多种粒子,按要求填入空格中:
| 质子数 |
16 |
16 |
16 |
| 电子数 |
16 |
17 |
18 |
| 化学式 |
|
|
|
环境保护已成为当前和未来的一项全球性重大课题之一。为消除目前燃料使用过程中的环境污染问题,并缓解能源危机,有的专家提供利用太阳能促进燃料循环使用的构想。
这种构想或方案可用如下反应表示:
①2CO2 2CO+O2
2CO+O2
②H2O _______________
_______________
③N2+H2O _______________
_______________
④CO2+_______________ CH3OH+_______________
CH3OH+_______________
⑤_______________+H2O CH4+_______________
CH4+_______________
(1)请完成上述化学方程式;
(2)要实现上述的一些构想,目前和今后要解决的关键问题是_________________________
______________________________________________________________________________;
试题篮
()