学习化学应正确认识物质及其变化。下列说法正确的是( )
| A. |
催化剂在化学反应后质量会减小 |
| B. |
铝在空气中会生成氧化铝膜 |
| C. |
硬水煮沸后导电能力通常会增强 |
| D. |
空气液化主要发生化学变化 |
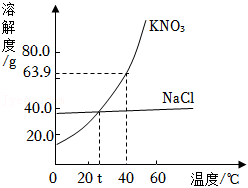
硝酸钾、氯化钠的溶解度曲线如图所示,下列说法正确的是( )
| A. |
用搅拌或加热的方法能增大氯化钠在水中的溶解度 |
| B. |
40℃时,100g硝酸钾饱和溶液中含有硝酸钾63.9g |
| C. |
t℃时,硝酸钾饱和溶液和氯化钠饱和溶液的溶质质量相等 |
| D. |
将硝酸钾溶液由40℃降温至20℃,不一定有硝酸钾晶体析出 |
化学就在我们身边。下列做法合理的是( )
| A. |
用熟石灰改良酸性土壤 |
| B. |
用氢氧化钠溶液治疗胃酸过多 |
| C. |
用浓硫酸作食品干燥剂 |
| D. |
用自来水除去铁制品表面的铁锈 |
在化学实验中要特别注意观察和记录实验现象。下列实验现象的记录正确的是( )
| A. |
硫粉燃烧生成无色无味的气体 |
| B. |
镁条在空气中燃烧生成黑色氧化镁 |
| C. |
干冰放置在空气中有白雾出现 |
| D. |
铜片加入稀硫酸中有大量气泡出现 |
化学在人类社会的发展历程中起着重要作用。下列认识错误的是( )
| A. |
我国科学家首次利用二氧化碳合成淀粉,该技术有助于推进“碳中和” |
| B. |
北京冬奥会火炬“飞扬”采用氢气作为燃料,燃烧产物无污染 |
| C. |
建造潜水器外壳所使用的钛合金,具有强度高、硬度大等特点 |
| D. |
加大化石燃料的开采与利用,以满足不断增长的能源需求 |
氢是实现碳中和的能源载体。
(1)煤制氢的原理可表示为 。
① 中肯定含有的元素是 。
②煤制氢的不足是 (写出一点)。
(2)甲烷制氢包括重整、转化和分离等过程。甲烷制氢过程中产生的 和 的混合气分离得到 的过程如下:
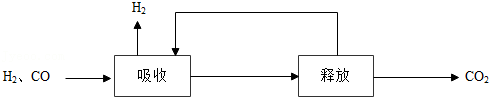
①海水作为吸收剂时,下列措施有利于海水吸收二氧化碳的是 (填序号)。
a.升高海水的温度
b.加快混合气的流速
c.增大气体的压强
②利用 溶液吸收 ,将其转化为 , 在加热条件下即可分解生成 。比较 和 分解反应的不同,可推知 的稳定性 (填“>”或“<”) 的稳定性。
③使用氢氧化钠溶液吸收二氧化碳并分离出氢气。补充完整氢氧化钠循环使用的方案。
步骤1:将氢气和二氧化碳的混合气通入足量的氢氧化钠溶液中。
步骤2:向步骤1所得的溶液中 。
步骤3:过滤,得滤渣和氢氧化钠溶液。
(3)某种利用太阳能制氢的过程如图1所示。
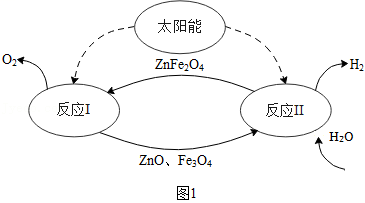
①反应I的基本类型为 。
②写出反应Ⅱ的化学方程式: 。
(4)我国2030~2050年各种能源使用预期情况如图2所示。
①图2所涉及的能源中,属于不可再生能源的是 。
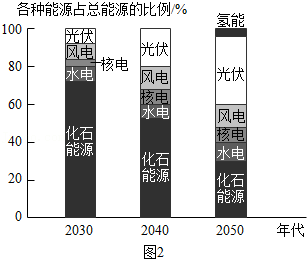
②2030~2050年,预期我国能源结构的变化趋势是 。
化学兴趣小组对实验室制取氧气进行了如下探究。
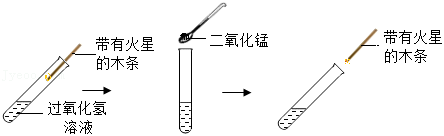
I、探究二氧化锰在过氧化氢分解反应中的作用
实验1:在试管中加入5mL5%过氧化氢溶液,把带火星的木条伸入试管,观察现象。(如图)
实验2:向上述试管中加入二氧化锰粉末,把带火星的木条伸入试管,有大量气泡冒出,带火星的木条复燃。
实验3:待上述试管中没有现象发生时,重新加入过氧化氢溶液,把带火星的木条伸入试管,观察现象。
实验4:探究催化剂的用量对过氧化氢分解速率的影响。每次实验均用30mL10%的 溶液,采用不同质量 粉末做催化剂,测定收集到500mL氧气所用的时间,结果如下:
|
实验序号 |
① |
② |
③ |
④ |
⑤ |
⑥ |
⑦ |
⑧ |
|
粉末用量/g |
0.1 |
0.2 |
0.3 |
0.4 |
0.5 |
0.6 |
0.7 |
0.8 |
|
所用时间/s |
17 |
8 |
6 |
3 |
2 |
2 |
2 |
2 |
(1)实验1中,观察到有气泡产生,带火星的小木条未复燃。实验结论是 。
(2)写出实验2发生反应的化学方程式 。
(3)实验3的实验目的是 。
(4)由实验4的实验结果可得出的结论是 。
Ⅱ、探究高锰酸钾分解制取氧气的得氧率
高锰酸钾在用酒精灯加热分解的过程中,可能发生如下三个反应:
①
②
③
(5)根据反应①,计算 完全分解生成氧气的质量(写出计算过程) 。
(6)已知: 。在反应①、②、③中,相同质量的高锰酸钾加热完全分解,理论上得氧率最高的是 (填反应序号)。
阅读下列短文,回答相关问题。
飞行的金属
现代先进的飞机与飞行器要飞得高、快、远、省,就必须靠轻、强、美的材料。铝、镁、锂、钛这些金属及其合金被称之为“飞行的金属”。铝、镁、锂、钛等金属在自然界中以化合物的形式存在,铝土矿含有 ,光卤石含有 ,锂辉石含有 ,金红石含有 。元素的存在形态与环境条件有关,铝元素在pH<4的溶液中以 存在,在pH为4~7时以 的形态沉淀,在pH>7的溶液中以 存在。
铝、镁、锂、钛的冶炼有电解法和还原法等。冶炼钛的部分生产流程如图1所示。

金属及其合金的性质决定其用途。钛在盐酸、硫酸、硝酸溶液中耐腐蚀,在碱性溶液中可稳定存在。将1mm厚的不锈钢、钛浸在海水中,不锈钢4年后完全腐蚀,钛几十年不腐蚀。钛合金、铝合金、铜合金的耐海水腐蚀性能试验结果如图2所示。航空航天材料的选择,既要轻又要有足够的强度。铝、镁、锂、钛、铁的密度( )的值分别为2.7、1.74、0.54、4.51和7.87。比强度( )越大,材料的性能越好。不锈钢、铝合金和钛合金的比强度分别为79、167和218。
铝,姗姗来迟,给世界带来勃勃生机。镁、锂让飞行器变得更快更省。钛,力大无比的巨人,“全能”的钛帮助人类飞出地球,飞向太空!
(1) 合金属于 。
| A. |
a.金属材料 |
| B. |
b.合成材料 |
| C. |
c.复合材料 |
(2)铝制品在空气中耐腐蚀的原因是 。
(3)锂和镁、铝相比,能让飞行器变得更快的原因是 ;钛、铜镍合金、铝黄铜中耐腐蚀性最好的是 。
(4)写出由 转化为 的化学反应方程式: 。
(5)下列叙述正确的是 (填序号)。
| A. |
a.自然界中,在酸性条件下,铝元素的存在形式有 或 |
| B. |
b.作为航空航天材料,与铝相比,钛在密度和强度方面都具有明显优势 |
| C. |
c.金属的冶炼与金属活动性、金属矿物的储量等因素有关 |
燃煤电厂产生的脱硫废水(含有 、 、 等物质)软化的一种工艺流程如下:
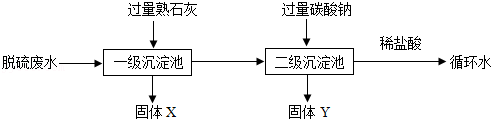
(1)“脱硫”过程中发生反应的化学方程式为: 。R的化学式为 。
(2)“沉淀”步骤需要不断搅拌,目的是 。
(3)写出“一级沉淀”中生成氢氧化镁的化学方程式: (任写一个)。
(4)“二级沉淀”中固体Y的化学式为 ;加入稀盐酸的目的是 。
(5)软化处理过程中,碳酸钠和熟石灰的添加顺序不能颠倒,原因是 。
化学兴趣小组同学对稀盐酸和氢氧化钠溶液反应的发生进行了探究。
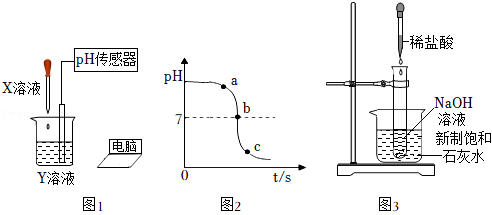
(1)利用如图1所示的装置进行实验探究。用pH传感器测得烧杯中溶液的pH随滴加液体体积变化的曲线如图2所示。
①反应前烧杯中盛放的液体Y是 。
②图中b点所示溶液中的溶质是 。
③写出盐酸和氢氧化钠反应的化学方程式: 。
(2)利用如图3所示装置进行实验:烧杯中放入新制饱和石灰水,向试管中加入氢氧化钠溶液,将稀盐酸滴入试管。一段时间后,试管外壁附近溶液中出现浑浊,原因是 。
暖宝宝可用于“暖”宝宝。
(1)利用铁粉、活性炭、水和食盐可自制暖宝宝。暖宝宝发热的原因是铁与空气中的 和水反应放热。
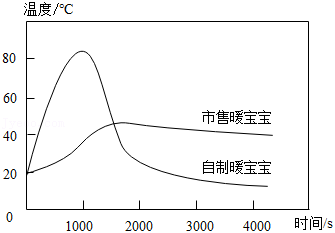
(2)利用温度传感器测得两种不同暖宝宝使用时温度变化的曲线如图所示。与市售暖宝宝相比,自制暖宝宝用来取暖的不足有:① ;② 。
(3)利用暖宝宝可从空气中分离出氮气。氮气可用作食品保护气,理由是 。
海水淡化常用蒸馏和膜分离等多种方法。
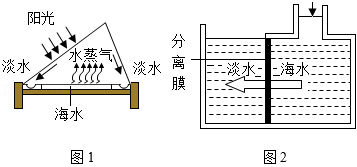
(1)蒸馏的原理示意图如图1所示。蒸馏属于 (填“物理”或“化学”)变化。
(2)膜分离的原理如图2所示。将海水加压一段时间后,水分子能透过分离膜, 和 却不能透过,右侧海水中氯化钠的质量分数 (填“变大”“变小”或“不变”)。
(3)膜分离的原理与化学实验中物质分离的 操作相似。
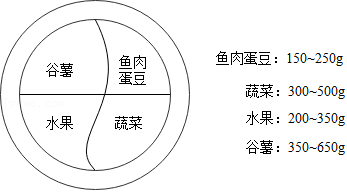
中国居民平衡膳食餐盘及每天摄入量建议如图所示。
(1)下列食物中富含蛋白质的是 (填序号)。
| A. |
a.谷薯类 |
| B. |
b.鱼肉类 |
| C. |
c.蔬菜类 |
(2)青少年缺少钙元素会患 。
| A. |
a.佝偻病 |
| B. |
b.夜盲症 |
| C. |
c.甲状腺肿大 |
(3)平衡膳食要注意两点:①膳食中有多样化的食物;② 。
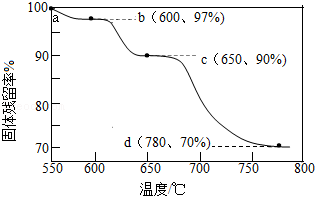
、 还原 的过程相似,大致分为三个阶段。向 中不断通入 ,不断加热,实验测得固体残留率(固体残留率 )随温度的变化曲线如图所示。下列叙述错误的是( )
| A. |
d点对应固体为 ,其质量为3.36g |
| B. |
从a到d点,固体中的含氧量逐渐变小 |
| C. |
从a到d点,固体减少的质量等于生成的水的质量 |
| D. |
bc段发生反应的方程式为 |
试题篮
()