碳酸钠、碳酸氢钠是中学常见的化合物。
探究一:碳酸钠、碳酸氢钠与酸反应
如图所示,将两气球内的NaHCO3和Na2CO3同时倒入试管中。已知盐酸足量,且装置气密性良好。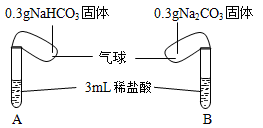
回答下列问题:
(1)碳酸钠俗名是。
(2)实验过程中观察到的现象是: 。
(3)NaHCO3和Na2CO3都能与盐酸反应产生二氧化碳、水和氯化钠。任写出其中一个反应的化学方程式。
(4)已知NaHCO3、Na2CO3的相对分子质量分别为84、106,通过计算:实验结束后,(填“A”或“B”)试管的气球更大。
探究二:碳酸氢钠、碳酸钠固体与酸反应的热效应
【发现问题】在探究一实验过程中用手触摸试管,发现盛NaHCO3的试管温度降低,而盛Na2CO3的试管温度升高。
【猜想与推测】甲同学由此推测:NaHCO3和盐酸反应为吸热反应,Na2CO3和盐酸反应为放热反应。
【实验与数据】乙同学认为甲同学推测不妥,通过以下多次实验后取平均值数据记录如下:
| 步骤① |
步骤② |
步骤③ |
步骤④ |
步骤⑤ |
| 测量10mL水温/℃ |
加入物质0.5 g |
溶解后测量溶液温度t1/℃ |
静置一段时间后测量溶液温度t2/℃ |
加入20%盐酸10 mL反应后测量溶液温度t3/℃ |
| 20 |
NaHCO3 |
18.5 |
20.0 |
20.8 |
| 20 |
Na2CO3 |
23.3 |
20.0 |
23.7 |
【分析与结论】
(1)由步骤①~③比较得到的结论是。
(2)由步骤④~⑤比较得到的结论是:。
(3)结合上面探究活动,你认为甲同学推测的不妥之处是。
(13分)某校化学兴趣小组用下图装置探究铁生锈的条件。
(1)气体发生装置的选择
A装置用双氧水和二氧化锰制取氧气,为了控制反应速率,得到平稳的氧气流,应选择下图中的(填“甲”、“乙”或“丙”)装置,该反应的化学方程式为。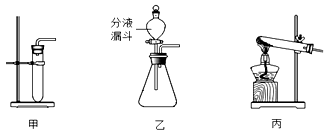
(2)铁生锈条件的探究
①上图C装置中浓硫酸的作用是。
②打开K1、K2、K3,通入氧气,检验氧气已充满整个装置的方法是。
关闭K1、K2、K3,2天后观察到:B处铁丝表面布满铁锈,D处铁丝依然光亮,E中铁丝表面有部分铁锈。
实验结论:铁生锈主要是铁与和 发生反应。
③B、E处实验现象对比说明:影响铁生锈快慢的一种因素是。
将氢氧化钠和氯化钠的混合物19.3g,放入80.7g水中使其完全溶解,再加入100g溶质质量分数为7.3%的稀盐酸,恰好完全反应。试计算:
(1)将上述浓度的稀盐酸100克稀释为溶质质量分数为4%的稀盐酸,需要加入水的质量;
(2)原混合物中氢氧化钠的质量;
(3)反应后所得溶液中溶质的质量。
实验室中有一瓶部分变质了的NaOH溶液,小丽为了测定溶液中溶质的Na2CO3的质量分数,现取20g待测溶液,向其中逐滴加入CaCl2溶液,产生沉淀质量与所加CaCl2质量的关系如图所示。
(1)B点处所得溶液中溶质有。
(2)若加入的CaCl2溶液的质量分数为11.1%则需该溶液的质量为________
(3)求待测溶液中Na2CO3的质量分数。(写出计算过程)
A、B、C、D、E是初中化学中常见的五种物质,它们都含有一种相同的元素,右图表示各物质之间的转化关系。其中,A为食盐的主要成分, B中含钡元素,D为有颜色溶液,E为蓝色溶液,其它物质的溶液都为无色;反应⑤和⑥为置换反应,其它均为复分解反应。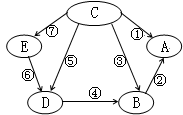
(1)写出物质C的化学式。
(2)反应②的现象为。
(3)反应⑥的化学方程式为。
下列是四种实验操作中各量变化关系的图像,能正确反映其对应操作的图像有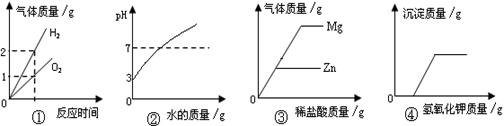
①电解水
②向一定量pH=3的盐酸溶液中不断加水稀释
③向等质量的镁和锌中分别加入溶质质量分数相同的稀盐酸至过量
④向盐酸和氯化铜的混合溶液中不断滴加氢氧化钾溶液
| A.4个 | B.3个 | C.2个 | D.1个 |
金属氧化物陶瓷着色,有时测定金属氧化物中的金属含量。现将Fe2O3、CuO、Al2O3的混合物16克,与109.5克20%的稀盐酸混合后恰好完全反应,则此金属氧化物着色剂中金属元素的含量是
| A.20% | B.70% | C.73.5% | D.80% |
如图是某胃药标签上的部分内容,兴趣小组欲测定该药品中碳酸氢钠(NaHCO3)的质量分数,取10片该药品研碎放入烧杯中,再向烧杯中滴加稀盐酸至恰好完全反应(杂质不溶于水也不参加反应),共消耗稀盐酸23g,测得反应后烧杯内物质的总质量为25.8g。请计算:
(1)10片药品的质量为g,反应共生成气体的质量为g;
(2)药品中碳酸氢钠的质量分数.
(3)反应后所得溶液中溶质的质量分数.(计算结果保留到0.1%)
某工厂废料中含有铜、氧化铜和碳中的一种或几种,按如下流程进行反应,请回答:
① A、C、D、E四种物质中,属于氧化物的是(13)(填字母)。
② 蓝色溶液B中含有溶质的化学式(14),产生气体E的化学方程式(15)。
③ 由此可以确定废料的成分是(16)。
梧州市某中学化学兴趣小组的同学发现,熟鸡蛋在常温下放置一、两天后就会变臭了。富有营养而鲜美的鸡蛋,怎么会散发出臭味呢?同学们旋即对此进行了研究。
【提出问题】这种散发出刺激性臭味的无色气体是什么?它有怎样的性质?
【猜想假设】大家按照查阅到的鸡蛋中主要含有的元素是C、H、O、N、S的信息,及相应元素的化合价,列出了气体的可能存在形式分别有以下几组:
甲组—含碳化合物:CH4、CO、CO2
乙组—含氮化合物:NH3、NO、NO2
丙组—含硫化合物:SO2、SO3
虽然列出了上述可能,但大家都一致提议排除甲组的可能性,大家提出的理由是:__________________。
【查阅资料】
| 物质 |
NH3 |
NO |
NO2 |
SO2 |
SO3 |
| 一些特性 |
碱性 |
在空气中会迅速变成NO2 |
红棕色 |
酸性,有刺激性气味,能使KMnO4溶液褪色 |
沸点44.8℃ |
根据所查阅的资料,大家进一步排除了NO、NO2,理由是___________________;
也排除了SO3的可能,理由是_____________________________________________。
【实验验证】
毫无头绪的同学们向老师请教,老师笑而不语,拿出了两集气瓶的气体M,告诉大家这就是该刺激性臭味气体的主要成分,具有可燃性,至于还有什么性质,让大家在注意防护和试验安全的条件下进行探究。
(1)小吴同学用针筒抽取了部分气体M,注入盛有石蕊试液的试管中,结果没有看到溶液变_________的现象,证明该气体不是NH3;
(2)小周同学设法点燃了气体M,并拿一个干冷的小烧杯罩在火焰的上方,看到烧杯内壁有小水珠出现,说明了M气体中含有_______元素;燃烧后的气体带有刺激性,并能使另一个内壁沾有KMnO4溶液的小烧杯,出现红色褪去的现象,说明M气体中还含有_______元素。
(3)为了进一步探究M气体的组成,小施将3.4g的M气体完全燃烧后,设法将燃烧后所得气体,全部通入如下装置进行中。(注:碱石灰为固体NaOH和CaO的混合物)
经充分吸收后称重,发现A装置增重1.8g,C装置增重6.4g。通过计算可知,除了上述小周确定的两种元素外,M气体中________(填“含”或“不含”)其他元素;并确定了M的化学式为___________。而上图中B装置的作用是___________________;D装置的作用是__________________。经过严谨的思考与细致的实验,同学们终于揭开了这种气体的组成。
春节期间,小颖你妈妈去医院打点滴,发现护士往输液管上放了一个纸包,经询问得知它是输液恒温贴。可以温暖输入人体中的液体。小颖对包里的东西能产生热量感到很奇,于是,他向护士要了一只输液恒温贴,带回来进行了如下探究。
撕开真空包装封口,解开内衣包装袋,倒出其中的粉末,发现成黑色。
【提出问题】黑色粉末可能含有哪些物质呢?
【猜想与假设】该黑色粉末可能含有碳粉、铁粉、二氧化锰、氧化铜、四氧化三铁中的一种或几种。
【初步认证】将磁铁靠近黑色粉末,部分被吸引。
【查阅资料】四氧化三铁能被磁铁吸引。四氧化三铁与盐酸反应生成氯化亚铁,氯化铁和水
【初步结论】黑色粉末可能含有。
【进行实验】
| 实验编号 |
实验操作 |
实验现象 |
| ① |
取少量黑色粉末于试管中,加足量稀硫酸 |
固体部分溶解,有气泡产生,溶液变为浅绿色, |
| ② |
将实验①试管中的物质过滤,向滤液中加入足量铁粉 |
有气泡产生,无红色物质析出 |
| ③ |
取实验②滤渣灼烧,将内壁涂有澄清石灰水的小烧杯罩在上方 |
澄清石灰水变浑浊 |
由上述实验可知,该黑色粉末肯定含有,肯定不含;写出实验①中产生气体的化学方程式.
【交流讨论】
①输液恒温贴真空包装的原因:铁粉在空气中会与发生缓慢氧化转化成铁锈
并放出热量。
②输液恒温贴中炭粉的作用是。
下列有关物质鉴别方案正确的一组是
| A.MgCl2溶液、NaOH溶液、H2SO4溶液、CuSO4溶液,不加任何试剂即可鉴别 |
| B.可用Ba(OH)2溶液鉴别(NH4)2CO3、(NH4)2SO4、NH4NO3三种氮肥 |
| C.Na2CO3溶液、Ca(OH)2溶液、盐酸、BaCl2溶液,不加任何试剂即可鉴别 |
| D.CuO粉末、炭粉、铁粉,三种黑色粉末用一种试剂就可鉴别 |
有A~F六种无色的液体,其中E溶液有咸味,其溶质可作为调味品,其余分别是稀盐酸、碳酸钠溶液、氢氧化钠溶液、氢氧化钙溶液、水中的某一种,请根据下面实验现象回答问题。
(1)将少量A分别滴入适量的B、C、D、F中,均没有明显现象。
(2)将少量B分别滴入适量的A、C、D、F中,C中有气泡出现,其余均没有明显现象。
(3)将少量D分别滴入适量的A、B、C、F中,均没有明显现象。
①溶液E中的溶质是。
②写出B滴入C中发生反应的化学方程式。
③根据实验现象能判断出的:B是C是F是
④对还没有确定的溶液(或液体),下列几种鉴别方法中,正确的是(填序号)。
A.分别滴加硫酸铜溶液B.分别滴加澄清石灰水
C.分别滴加石蕊溶液 D.分别滴加稀盐酸
氢化钙固体是登山运动员常用的能源提供剂。某探究小组的同学通过查阅资料得知,氢化钙(CaH2)与水反应生成氢氧化钙和氢气。
请写出该反应的化学方程式:
探究小组的同学把一定量的CaH2加入碳酸钠溶液中,充分反应后过滤,得到滤渣和滤液,经检验滤渣的成分是碳酸钙。
【提出问题】滤液中溶质的成分是什么?
【猜想与假设】猜想一:氢氧化钠、碳酸钠、氢氧化钙
猜想二:氢氧化钠、碳酸钠
猜想三:
猜想四:氢氧化钠
经过讨论,大家一致认为猜想不合理,请用化学方程式说明原因:
【实验验证】
| 实验 |
现象 |
结论 |
| 实验一:取滤液,向其中滴入少量碳酸钠溶液 |
无明显现象 |
猜想不成立 |
| 实验二:另取滤液,向其中加入足量稀盐酸 |
猜想二成立 |
【反思与拓展】
①若向氯化铵的浓溶液中加一定量CaH2,充分反应,产生的气体是;
②登山运动员常用CaH2作为能源提供剂,与氢气相比,其优点是。
【定量分析】
探究小组的同学称取氢化钙样品的质量为10g,加入碳酸钠溶液中(假设氢化钙样品中的杂质不反应),充分反应后过滤、洗涤、烘干,得到滤渣质量为20g,试计算氢化钙样品中氢化钙的质量分数。(要求写出计算过程)
硫酸锌可作为食品锌强化剂的原料。工业上常用菱锌矿生产硫酸锌,菱锌矿的主要成分是ZnCO3,并含少量的Fe2O3、FeCO3、MgO等,工艺流程图如下:
【查阅资料】①一般情况下,难溶性碱受热易分解,生成对应的金属氧化物和水;
②Mg(OH)2和Zn(OH)2开始沉淀和沉淀完全时的pH如下表所示:
| Mg(OH)2 |
Zn(OH)2 |
|
| 开始沉淀的pH |
10.4 |
6.4 |
| 沉淀完全的pH |
12.4 |
8.0 |
| 开始溶解的pH |
—— |
10.5 |
根据上图回答下列问题:
(1)将菱锌矿研磨成粉的目的是;
(2)针铁矿的组成元素是Fe、O和H,相对分子质量是89,针铁矿中铁原子数︰氧原子数︰氢原子数=;(提示:氢原子数目小于氧原子数目)
(3)“滤液4”之前加入锌粉的目的是;
(4)工业上从“滤液3”制取MgO过程中,合适的反应物是(选填序号);
a.大理石粉 b.石灰乳 c.纯碱溶液 d.烧碱溶液
(5)完成这个流程中发生的化学反应方程式:
4Fe(OH)2+Ca(ClO)2+2=4Fe(OH)3+CaCl2,
试题篮
()