二氧化碳与二氧化硫均为非金属氧化物,某兴趣小组用类比法对SO 2进行如下探究:
探究一 二氧化硫和二氧化碳性质的比较
[查阅资料]二氧化硫具有漂白性,能与某些有色物质(如品红溶液)反应生成无色物质。

| 操作现象装置 |
实验Ⅰ:通入二氧化碳 |
实验Ⅱ:通入二氧化硫 |
| A |
紫色变成红色 |
? |
| B |
无明显变化 |
红色褪为无色 |
| C |
白色浑浊 |
白色浑浊 |
由实验可知:
(1)将SO 2通入装置A中的现象为 说明二氧化硫也能与水反应生成相应的酸。
(2)二氧化碳能与澄清石灰水反应,生成亚硫酸钙(CaSO 3)和水,写出该反应的化学方程式 。
(3)鉴别CO 2和SO 2的方法是 。
(4)从环保角度指出上述装置的不足之处: 。
探究二 测定工业废气中的SO 2含量
[查阅资料]①二氧化硫与溴水反应的化学方程式为:Br 2+SO 2+2H 2O=H 2SO 4+2HBr
②我省规定工业排放的废气中SO 2含量不得超0.4mg/m 3。
探究小组进行如下实验
测定步骤:
Ⅰ.向试管中加入10mL溶质的质量分数为0.1%的溴水(其密度可近视看做1g/cm 3)
Ⅱ.在指定地点抽取工业废气注入上述溴水中(如图2)。
Ⅲ.当注入溴水中的工业废气总量达5m 3时,溶液恰好由黄色变成无色。
(1)由实验可知该废气中SO 2含量为 mg/m 3, (填"符合"或"不符合")排放标准(SO 2、Br 2的相对分子质量分别为:64、160)
(2)排放到空气中的SO 2气体主要来自 的燃烧。
某固体粉末由Mg、MgO和Mg(OH)2中的一种或几种组成。某化学小组为了探究该固体粉末的成分,设计如图所示的装置(固定装置省略)
[信息资料]本实验条件下,氢气密度为0.09g/L。
[实验过程]
步骤Ⅰ:检查装置气密性,装入药品并连接仪器。
步骤Ⅱ:倾斜Y形管,使样品充分反应,测定生成气体的体积为55.6mL。
步骤Ⅲ:拆下装置,往Y形管内残余液中加入氢氧化钠溶液,至不再生产沉淀。经过滤、洗涤和干燥后,称得沉淀质量为2.90g。
[回答问题]
(1)该套装置气密性的检查方法是 。
(2)①使样品与硫酸充分反应的正确操作是 (填标号)。
A.硫酸溶液转移到样品中 B.样品转移到硫酸溶液中
②判断样品完全反应的现象是 。
(3)根据实验结果分析:
①通过步骤Ⅱ推断,样品中一定含有的物质是 。
通过步骤Ⅲ计算,样品中镁元素的总质量为 g。
②结论:该样品中的成分是 。
[反思]
(4)该化学小组同学经过讨论得到以下结论,正确的有 (填标号)。
A.利用该实验方案,能计算出样品中各物质的质量
B.实验前可通过样品的质量估算硫酸溶液的质量,确保样品完全反应
C.仅称量步骤Ⅱ中Y形管内药品减轻的质量,即能计算出样品中各物质的质量。

有一固体物质可能含有硫酸钾、硝酸铵、氯化钡中的一种或几种。现需要对此物质成分进行检测。甲同学向固体中加入足量的水,形成无色溶液;乙同学向固体中加入足量氢氧化钡溶液,产生白色沉淀,放出刺激性气体。
(1)该气体为 (写化学式)。
(2)根据两同学的实验现象可推定此物质的组成是 。
有一包白色固体可能含有碳酸钠、硫酸钠、硝酸钡、氢氧化钠中的一种或几种,某科学兴趣小组为探究其成分做了以下实验:
①取少量固体于烧杯中,加足量的水溶解,烧杯内有固体残留并得到无色溶液甲;
②取少量无色溶液甲于试管中,滴加酚酞溶液,溶液不变色;
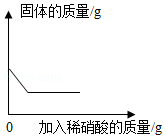
③继续向①的烧杯中滴加稀硝酸并不断搅拌,烧杯内固体的质量随加入稀硝酸质量的变化如图所示。
(1)仅通过①可以得出的结论是:原白色固体中一定有 ;
(2)无色溶液甲中一定不存在的物质是 (填字母)
A.碳酸钠 B.硫酸钠 C.硝酸钡 D.氢氧化钠
有一固体物质可能含有硫酸钾、硝酸铵、氯化钡中的一种或几种。现需要对此物质成分进行检测。甲同学向固体中加入足量的水,形成无色溶液;乙同学向固体中加入足量氢氧化钡溶液,产生白色沉淀,放出刺激性气体。
(1)该气体为 (写化学式)。
(2)根据两同学的实验现象可推定此物质的组成是 。
有一包白色粉末,可能是由硫酸铜、氯化钠、碳酸钠、硫酸钠中的一种或几种组成,为检验其中的成分,按以下流程进行实验:
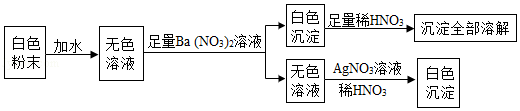
(1)根据实验现象,白色粉末中一定有 。
(2)实验中不能用BaCl 2溶液代替Ba(NO 3) 2溶液的理由是 。
某白色固体中可能含有氯化钠、碳酸钠、硫酸钠、碳酸钡、氯化钡中的几种物质,为了鉴定该白色固体的组成,拓展性学习小组的同学们进行可如下探究实验:
Ⅰ.称取15克固体于烧杯中,加入足量水充分溶解,过滤得到白色沉淀4.3克和无色溶液。
Ⅱ.Ⅰ中所得4.3克白色沉淀中加入足量稀盐酸,沉淀部分溶解并有无色气体产生,测得剩余沉淀质量为2.33克。
Ⅲ.把Ⅰ中所得滤液分成两份,第一份溶液中加入足量的稀硫酸,既没有产生气泡,也没有产生沉淀,第二溶液中加入足量的氯化钡溶液,没有产生沉淀。
根据上述实验,回答下列问题:
(1)仅根据第Ⅲ步实现现象可以得出结论,溶液中一定不存在离子是 。
(2)写出某白色固体的所有可能组成 。
某可燃性气体X可能含有H、C、O三种元素中的一种或几种,为探究其成分,某同学按如图所示装置在空气中点燃X(夹持仪器已略去)
已知:无水硫酸铜为白色粉末,遇水变蓝,分析推断:
(1)若无水硫酸铜变蓝,澄清石灰水未出现浑浊,则X一定含有的元素是 ,X燃烧的化学方程式为 ;
(2)若无水硫酸铜不变色,澄清石灰水出现浑浊,则X一定含有的元素是 X燃烧的化学方程式为 ;。
(3)若无水硫酸铜变蓝,澄清石灰水出现浑浊,则X一定含有的元素是 ,且X (选填字母编号)
A.只能是纯净物B.只能是混合物C.既可能是纯净物,也可能是混合物

某工厂排出的废水中,可能含有AgNO3、Ba(NO3)2、FeCl2、Cu(NO3)2、Na2SO4中的几种物质.某化学兴趣小组做如下实验,探究工厂废水中含有的物质并设计实验方案处理废水.
【查阅资料】①白色的Fe(OH)2沉淀在潮湿空气中迅速转化为红褐色Fe(OH)3;
②Ba的金属活动性比Fe强.
(1)取少量废水,加入过量稀盐酸,产生白色沉淀,沉淀化学式为 ;过滤,将滤液分成两份,一份加入稀硫酸,产生白色沉淀,反应化学方程式为 ;另一份加入过量氢氧化钠溶液,产生蓝色沉淀,该过程中与OH﹣反应的离子有 (写离子符号).
(2)依据工厂排出废水中含有的物质,该化学兴趣小组设计了一个处理该废水的实验方案,流程如下:
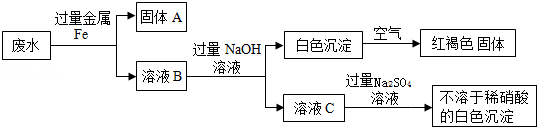
废水中含有的物质为 (写化学式),溶液C中的溶质为 (写化学式).此流程中涉及 种基本反应类型.
某小组同学做实验时。不小心使小烧杯里刚配好的FeSO4溶液混入了几种固体物质。只知道混入的物质是下列中的一种或几种:CuCl2、BaCl2、CaCO3.小组同学观察到混入其它物质后的溶液产生了浑浊。同学们决定按以下步骤对该小烧杯中的物质进行探究。请你和他们一起完成探究
资料:BaSO4,不溶于水。也不和稀酸反应
实验步骤 |
实验现象 |
向上述小烧杯中加入足量水,充分搅拌后过滤,得到溶液和滤渣a.取滤渣a于试管中。向试管中加入足量稀盐酸。 |
试管中有气泡产生 滤渣部分溶解。 |
(1)根据上述实验现象。写出滤渣a 中所含固体物质化学式
(2)有气泡放且滤渣部分溶解的原因是(用化学方程式表示)
(3)根据上述现象。滤液中一定含有的离子是(写离子符号)
(4)为进一步确定混入物质成分。对上述滤液进行如下实验:
实验步骤 |
|
取一定量的滤液,向滤液中加入过量锌粉,充分反应后过滤,得到滤渣b,向滤渣中加入足量稀盐酸 |
有气泡产生,滤渣部分溶解 |
写出锌粉和滤液发生反应的化学方程式:
滤渣b中含有的固体物质是(写化学式)
(5)原FeSO4溶液混入的物质是: 。
某工厂废气中可能含有CO、CO2、N2中的一种或几种。为确定废气成分,同学们按如下流程进行实验。
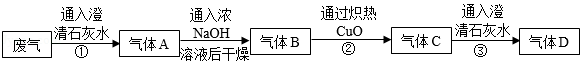
(1)①中澄清石灰水变浑浊,写出该反应的化学方程式
(2)将气体A通入浓NaOH溶液以除去CO2,其目的是
(3)③中澄清石灰水变浑浊。请写出②中发生反应的化学方程式
(4)原废气中一定含有的气体是
(5)应将气体D进行如下处理(填序号)
A.将气体D充分燃烧 B.将气体D直接排放到空气中
C.将气体D收集后再处理。
(1)初中化学关于研究物质组成的方法有多种,例如:
①化合法:适用于由两种单质发生的化合反应。如通过氢气与氧气反应生成水来研究水的组成,其化学方程式为 ;
②分解法:如通过电解水研究水的组成。如图装置中与直流电源正、负两极相连的玻璃管中生成的气体的质量比是 。运用上述两种方法研究水的组成,可知水是由氢、氧两种元素组成的。两种研究方法的理论依据是 。
③燃烧法:很多化合物燃烧有多种生成物,需通过定量研究来确定物质的组成。如: (写出一种有机物燃烧的化学方程式)
(2)资源是人类最大的财富,请完善下列保护金属资源的途径。
①防止金属的腐蚀,如防止铁制品锈蚀的方法有 (填一条);除铁锈的化学方程式是
②
③有计划合理的开采矿物,严禁不顾国家利益乱采矿,如对稀土的开采。
(1)初中化学关于研究物质组成的方法有多种,例如:
①化合法:适用于由两种单质发生的化合反应。如通过氢气与氧气反应生成水来研究水的组成,其化学方程式为 ;
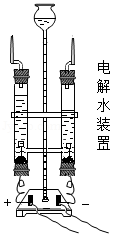
②分解法:如通过电解水研究水的组成。如图装置中与直流电源正、负两极相连的玻璃管中生成的气体的质量比是 。运用上述两种方法研究水的组成,可知水是由氢、氧两种元素组成的。两种研究方法的理论依据是 。
③燃烧法:很多化合物燃烧有多种生成物,需通过定量研究来确定物质的组成。如: (写出一种有机物燃烧的化学方程式)
(2)资源是人类最大的财富,请完善下列保护金属资源的途径。
①防止金属的腐蚀,如防止铁制品锈蚀的方法有 (填一条);除铁锈的化学方程式是
②
③有计划合理的开采矿物,严禁不顾国家利益乱采矿,如对稀土的开采。
(1)初中化学关于研究物质组成的方法有多种,例如:
①化合法:适用于由两种单质发生的化合反应。如通过氢气与氧气反应生成水来研究水的组成,其化学方程式为 ;
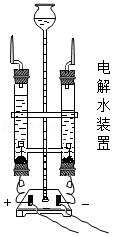
②分解法:如通过电解水研究水的组成。如图装置中与直流电源正、负两极相连的玻璃管中生成的气体的质量比是 。运用上述两种方法研究水的组成,可知水是由氢、氧两种元素组成的。两种研究方法的理论依据是 。
③燃烧法:很多化合物燃烧有多种生成物,需通过定量研究来确定物质的组成。如: ____ (写出一种有机物燃烧的化学方程式)
(2)资源是人类最大的财富,请完善下列保护金属资源的途径。
①防止金属的腐蚀,如防止铁制品锈蚀的方法有 (填一条);除铁锈的化学方程式是 _____
②
③有计划合理的开采矿物,严禁不顾国家利益乱采矿,如对稀土的开采。
(1)初中化学关于研究物质组成的方法有多种,例如:
①化合法:适用于由两种单质发生的化合反应。如通过氢气与氧气反应生成水来研究水的组成,其化学方程式为 ;
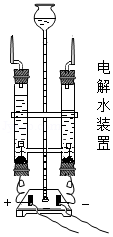
②分解法:如通过电解水研究水的组成。如图装置中与直流电源正、负两极相连的玻璃管中生成的气体的质量比是 。运用上述两种方法研究水的组成,可知水是由氢、氧两种元素组成的。两种研究方法的理论依据是 。
③燃烧法:很多化合物燃烧有多种生成物,需通过定量研究来确定物质的组成。如: _____ (写出一种有机物燃烧的化学方程式)
(2)资源是人类最大的财富,请完善下列保护金属资源的途径。
①防止金属的腐蚀,如防止铁制品锈蚀的方法有 (填一条);除铁锈的化学方程式是 ____
②
③有计划合理的开采矿物,严禁不顾国家利益乱采矿,如对稀土的开采。
试题篮
()