实验探究:
某同学将一定质量的碳酸氢钠和稀硫酸混合,反应完全后(假设反应产生的气体全部逸出),对反应后溶液中溶质的成分进行如下探究:
【实验用品】pH试纸、Zn片、氧化铜粉末、稀H 2SO 4、NaOH溶液、BaCl 2溶液.
【假设猜想】猜想一:Na 2SO 4
猜想二:Na 2SO 4、NaHCO 3
猜想三:Na 2SO 4、H 2SO 4
【实验探究】同学们取反应后的溶液用不同方案进行如下实验,请根据现象或结论填空
| 实验方案 |
A |
B |
C |
D |
| 实验操作 |
|
|
|
|
| 实验现象 |
无气泡产生 |
试纸变色,对照比色卡,pH<7 |
|
产生白色沉淀 |
| 实验结论 |
|
猜想三正确 |
猜想三正确 |
猜想三正确 |
【得出结论】猜想三正确
【评价反思】老师对同学们能用多种方案进行探究,并且得出正确的实验结论给予了肯定,同时指出探究中存在的两处明显错误,分别是:
①
②
【总结提高】依据所给实验用品,你还有什么不同类方法确认猜想三是正确的.请写出你的实验方案 .
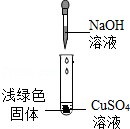
兴趣小组实验中,将NaOH溶液滴入CuSO4溶液中,结果溶液中生成了浅绿色的固体。于是,他们对该浅绿色固体的成分进行探究。
【查阅资料】
①NaOH与CuSO4反应会生产Cu(OH)2,也会生成Cu4(OH)4SO4(碱式硫酸铜)。
②Cu(OH)2在80℃会分解生成CuO。
③Cu4(OH)4SO4不溶于水,能与酸反应,分解温度需300℃。
【猜想与假设】
猜想一:浅绿色固体为Cu(OH)2。
猜想二:浅绿色固体为 。
猜想三:浅绿色固体为Cu(OH)2和Cu4(OH)4SO4。
【获取事实与证据】
①取少量浅绿色固体放入试管中,加热至100℃,观察到黑色固体物质,说明浅绿色固体中存在 。
②另取少量浅绿色固体放入试管中,加入足量稀硝酸,再滴加Ba(NO3)2溶液,出现白色沉淀,该白色沉淀是 。
【结论】整个实验证明猜想 正确。
中国药学家屠呦呦研制的抗疟疾药物青蒿素挽救了全球数百万人的生命,她因此荣获了2015年诺贝尔生理学或医学奖。某化学兴趣小组尝试探究青蒿素的组成,请你一同参与。
【猜想与假设】猜想一:青蒿素中一定含有 元素。
猜想二:青蒿素中可能含有氢元素和氧元素。
【实验与探究】他们设计了如图2所示的实验装置

(1)B装置的作用是 。
(2)实验时打开分液漏斗的活塞,将H 2O 2溶液滴入A装置中,再点燃C装置处的酒精灯。A装置中反应的化学方程式为 。
(3)E装置中观察到的实验现象是 ,
证明猜想一正确,E装置中反应的化学方程式为 。
【解释与结论】若青蒿素试样为14.1g,其完全燃烧后,装置D增重9.9g,装置E增重33g(假设各装置充分吸收有关气体)。通过计算可以确定青蒿素中除含有猜想一所含元素外,还含有 元素,得出此结论的依据是 。

实验桌上现有包白色粉末,可能是氢氧化钠、硫酸钠、碳酸钠和氯化铜的两种或两种以上组成。现将其放入一干净的烧杯M中,加入足量的水后,固体全部溶解得到无色溶液,再滴加几滴无色酚酞,溶液变为红色。
为进一步确定白色粉末的成分,同学们进行了如下探究。
【查阅资料】碳酸钠溶液呈碱性;氯化钡溶液和硫酸钠溶液呈中性。
【讨论猜想】进过分析,针对白色粉末的组成,大家提出如下猜想:
小红:氢氧化钠、硫酸钠; 小华:氢氧化钠、碳酸钠;
小明:碳酸钠、硫酸钠; 小亮:氢氧化钠、碳酸钠和硫酸钠。
【实验探究】四位同学共同设计并进行了如下实验:
| 实验步骤 |
实验现象 |
实验结论 |
| 1.取烧杯M中的少量溶液于试管A中,向其中加入一定量的稀盐酸 |
溶液由红色变为无色且有气泡产生。 |
的猜想不正确 |
| 2.另取烧杯M中的少量溶液于另一试管B中,向其中加入过量氯化钡溶液。 |
|
小亮的猜想正确 |
| 3.继续向试管B中加入过量的稀盐酸 |
|
实验完毕后,同学们将试管A、B中的物质倒在同一烧杯中,然后过滤,滤液中除酚酞外一定还含有的溶质有 。
小明设计了如下装置,验证
可以还原
。请回答下列问题:

(1)
是储气瓶,向其注水可使
流出,使用时应将(写"
"或"
")端口与
端口相连。
装置中的作用是。
(2)实验中,
中药品出现蓝色,
中溶液变浑浊。写出
中玻璃管内反应的化学方程式。
(3)小明想用
装置证明
不能使澄清石灰水变浑浊,进而排除对
装置的干扰。老师分析整个操作过程后指出省略
装置也可达到上述目的,其理由是。
在学了生活中常见盐的性质以后,某校化学兴趣小组的同学开展了测定Na 2CO 3和NaCl混合固体中Na 2CO 3含量的探究实验,他们设计了如下的实验方案:

(1)如图甲所示(铁夹夹持的仪器是注射器),把一定量的混合物与足量稀硫酸反应后,测定产生的二氧化碳气体的体积,检查该装置的气密性的方法是: ;
(2)小明同学提出用图乙代替图甲中的收集装置,则所测CO 2气体的体积 (填"偏大"、"偏小"、"不变");有同学对乙装置中的缺陷提出三种改进方案。
A方案:将广口瓶中的水改为饱和的CO 2水溶液;B方案:将广口瓶中的水改为氢氧化钠稀溶液;C方案:在广口瓶中的水面上覆盖一层植物油。你认为错误的方案是 (填字母代号);广口瓶内原有的空气对实验结果 (填"有"或"没有")影响;
(3)小宇同学用图丙装置测定CO 2的质量。则图丙实验装置主要存在哪些缺陷?这些缺陷对实验结果有何影响?请写出其中两点主要缺陷及对实验结果的影响。
① ;② 。
燃烧是一种发光、放热的剧烈的化学反应。认识燃烧,科学地利用和控制燃烧,使燃烧为人类服务是十分重要的。
[查阅资料]物质燃烧一般需要同时满足三个条件,物质具有可燃性是燃烧的首要条件,发生燃烧的另外两个条件分别是;。
[实验目的]验证木炭发生燃烧的另外两个条件中,缺少任何一个条件都不能燃烧(两个条件须分别验证)。
[实验设计与操作]下面是验证燃烧条件的实验装置图(可通过开启、关闭活塞控制液体)。

在完成气密性检查后加入药品,并已设法在整个装置中充满了氮气。若要求实验过程中不得拆、装仪器,请设计后续的实验步骤,并按要求填表。
| 步骤 |
操作 |
预计现象及得出的结论 |
| ① |
在活塞关闭的状态下,点燃酒精灯加热 |
|
| ② |
盖灭酒精灯,待仪器恢复到常温 |
|
| ③ |
||
| ④ |
[反思评价]实验过程中,装置B的作用可能是
一包固体,可能含有镁粉、碳粉、氧化铜、氢氧化钠、氯化钾中的一种或几种。为探究固体的组成,某化学兴趣小组进行了如图所示实验:

请回答下列问题:
(1)该实验中生成白色沉淀滤渣乙的化学方程式为 ;
(2)原固体中一定不含有的物质是 (写名称或化学式均可,下同),证据是 ;
(3)原固体中一定含有的物质是 ;
(4)实验结束后,该兴趣小组将滤液C和滤液D都倒入废液缸,有白色沉淀生成,上层清液E为蓝色,经检验,E中不含氯离子,则E中一定含有的溶质是 。
某兴趣小组同学欲探究NaOH溶液与CO 2气体的反应,设计如图所示实验装置:
(1)若导管a与b连接,将分液漏斗中的NaOH溶液注入锥形瓶,关闭分液漏斗上的活塞,振荡,然后打开导管上的活塞,观察到的实验现象是 ,CO 2与NaOH反应的化学方程式是 ;
(2)探究反应后锥形瓶内溶液中溶质的成分:
已知Na 2CO 3+H 2O+CO 2═2NaHCO 3
NaHCO 3+NaOH═Na 2CO 3+H 2O
【提出猜想】Ⅰ.NaOH和Na 2CO 3;Ⅱ. ;
Ⅲ.NaHCO 3;Ⅳ.Na 2CO 3和NaHCO 3.
【查阅资料】①Ca(OH) 2与Na 2CO 3、NaHCO 3均能反应且有白色沉淀生成;
②CaCl 2与Na 2CO 3能反应且有白色沉淀生成,与NaHCO 3不反应;
③NaHCO 3溶液显碱性,可与酸反应生成CO 2气体.
【设计实验】限选试剂:Ca(OH) 2溶液、CaCl 2溶液、稀盐酸、酚酞试液.
| 实验操作 |
实验现象 |
实验结论 |
| 1.取少量反应后溶液于试管中,加入足量的 振荡 |
产生白色沉淀 |
猜想Ⅲ不成立 |
| 2.将操作Ⅰ所得混合物过滤,向滤液中加入足量的 ,振荡 |
|
猜想Ⅳ成立 |
【拓展应用】联想到空气中有CO 2,所以实验室中的氢氧化钠溶液应 保存.

小明在冬天输液时发现护士在输液管上加了一个如图所示的装置,护士告诉他这是一次性输液加热棒,可以消除药液温度与体温的差异。加热棒里的成分到底是什么呢?科学研究小组通过上网查阅资料发现:一次性输液加热棒内的主要成分是还原性铁粉、炭粉和氯化钠等物质。该加热棒内是否真的含有这几种物质呢?科学研究小组设计了如下实验:

(1)探究加热棒内是否含有氯化钠
①将加热棒内的物质放入烧杯中,加入足量的水充分溶解、过滤,得到滤渣和滤液。
②取适量滤液于试管中,滴加适量的硝酸钡溶液和稀硝酸,无明显现象,
(填写正确的实验操作及现象),证明滤液中含有Cl﹣。
在老师的指导下通过进一步的实验证明滤液中还含有Na+,从而确定含有氯化钠。
(2)探究加热棒内是否含有铁粉
小明用磁铁靠近滤渣,发现部分黑色粉末被吸引。但被吸引的黑色物质也有可能是四氧化三铁。
小明通过如图装置探究黑色物质是否含有四氧化三铁,该物质鉴定的原理是:Fe3O4+4H2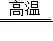 3Fe+4H2O。
3Fe+4H2O。

当观察到 这一现象时,排除了四氧化三铁存在的可能性。
小英同学认为这还不能确定铁粉的存在,因为除了四氧化三铁外,钴粉、镍粉也是能被磁铁吸引的黑色粉末。研究小组的同学在查阅资料的基础上,进行如下实验:取适量被吸引的黑色物质于试管中,加入足量的稀盐酸,充分反应后,向试管中加入足量的过氧化氢溶液(能将Fe2+转化为Fe3+),然后滴加硫氰化钾溶液。溶液变为血红色,证明溶液中有Fe2+,得出加热棒中含有铁粉这一结论。
(3)探究加热棒内是否含有炭粉
点燃不能被吸引的黑色粉末,并将产生的气体通入足量澄清石灰水,石灰水变浑浊,得出加热棒内含有炭粉这一结论。请写出此操作过程中确认炭粉存在的化学方程式: 、 。
综合上述实验,小明验证了加热棒内的主要成分。
加热棒为什么能够起到加热作用呢?小明还将进一步探究。
实验室中有一种含有纯碱、小苏打和少量水的固体粉末样品。为了测定其中小苏打的含量,某化学兴趣小组的同学在老师的指导下,利用如图所示装置(部分固定装置已略去)进行实验。

已知:①该装置气密性良好,A、C、D中所装药品足量且能完全吸收相关物质
②碱石灰是CaO与NaOH的固体混合物
③加热条件下,纯碱稳定不分解,小苏打易分解,反应的化学方程式为:
2NaHCO 3 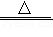 Na 2CO 3+H 2O+CO 2↑
Na 2CO 3+H 2O+CO 2↑
探究过程如下:
Ⅰ.称量样品和已装入相关药品的装置C、D的质量,分别为:m、m 1、m 2;
Ⅱ.将质量为m的样品装入B玻璃管中,按图连接好装置,关闭弹簧夹,给玻璃管加热
Ⅲ.待玻璃管中样品完全反应,打开弹簧夹通空气,再熄灭酒精灯,直到玻璃管冷却
Ⅳ.再次称量装置C、D的质量,分别为m 3、m 4
请回答下列问题
(1)装置A中碱石灰的作用是
(2)装置C中所装药品为
(3)装置D中发生反应的化学方程式为
(4)装置E的作用
(5)依据实验所得数据计算,该样品中小苏打的质量分数为 (用相关字母表示)。
(6)误差分析。按上述实验步骤测得该样品中小苏打的质量分数 (填"偏大""偏小"或"准确"),理由是 。
人们的日常生活离不开金属,高科技新材料的开发和应用也需要金属.硅钢可用于制造变压器的铁芯,某化学兴趣小组的同学为了验证硅钢(主要含有Fe、C、Si),设计了如图的实验流程(有些反应的部分反应物和生成物已省略).

查阅资料发现:常温下,单质硅(Si)不能与盐酸反应,但能与氢氧化钠溶液反应(Si+2NaOH+H 2O═Na 2SiO 3+2H 2↑).
根据以上信息,回答下列问题:
(1)固体A的成分为 ,E的化学式为 ;
(2)滤液B中的金属阳离子为 ;
(3)在过滤操作时,若发现滤液浑浊,应 ;
(4)步骤⑤中发生的是化合反应,尝试写出其化学方程式 .
某混合气体由CO、CO 2、SO 2三种气体组成,某兴趣小组对此进行了相关实验:
【查阅资料】①SO 2能使品红溶液褪色;②SO 2易与高锰酸钾溶液反应而被吸收,并能使其褪色;③SO 2能使氢氧化钡溶液和澄清石灰水变浑浊;④CO和CO 2均不能使品红溶液褪色,也不与高锰酸钾溶液反应。
【实验研究】为验证这三种气体同学们设计并进行如下实验:

【事实与结论】通过实验验证了以上三种气体都存在。
(1)装置A的作用是 ;
(2)能证明气体中含有CO 2的现象是 ;
【反思与评价】
(3)若装置按C→D→A→B→E的顺序连接,则无法验证的气体是 ;
(4)有同学提出上述原装置中省略D装置也能达到实验目的,你认为该同学的设计有无道理并说明理由 。
合金中除含金属外,也可以含有非金属。已知某铝合金粉末除含铝、铜外,还含镁和硅中的一种或两种。小冬设计实验对该铝合金粉末进行探究。
【查阅资料】
(1)硅不能与盐酸反应。
(2)铜、镁不能与氢氧化钠溶液反应
(3)铝、硅能与氢氧化钠溶液反应且得到相同的气体。硅与氢氧化钠的溶液反应的方程式为
Si+2NaOH+H2O=Na2SiO3+2H2↑,足量铝与氢氧化钠溶液反应后溶液的溶质为NaAlO2,则铝与氢氧化钠溶液反应的化学方程式为 。
【提出猜想】
猜想一:该粉末中除含铝、铜外,还含有镁。
猜想二:该粉末中除含铝、铜外,还含有硅。
猜想三:该粉末中除含铝、铜外,还含有 。
【设计实验】
实验步骤 |
实验现象 |
实验结论 |
|
实验一 |
①取一定量的合金粉末,加过量 的 ,充分反应后过滤 |
粉末部分溶解,并有无色气体放出 |
粉末中还含有硅 |
②取步骤①所得滤渣,加过量 的 ,充分反应 |
滤渣部分溶解,并有无色气体放出 |
||
实验二 |
|
略 |
|
【实验结论】猜想三正确。
实验室中有一种含有纯碱、小苏打和少量水的固体粉末样品。为了测定其中小苏打的含量,某化学兴趣小组的同学在老师的指导下,利用如图所示装置(部分固定装置已略去)进行实验。

已知:①该装置气密性良好,A、C、D中所装药品足量且能完全吸收相关物质
②碱石灰是CaO与NaOH的固体混合物
③加热条件下,纯碱稳定不分解,小苏打易分解,反应的化学方程式为:2NaHCO 3  Na 2CO 3+H 2O+CO 2↑
Na 2CO 3+H 2O+CO 2↑
探究过程如下:
Ⅰ.称量样品和已装入相关药品的装置C、D的质量,分别为:m、m 1、m 2;
Ⅱ.将质量为m的样品装入B玻璃管中,按图连接好装置,关闭弹簧夹,给玻璃管加热
Ⅲ.待玻璃管中样品完全反应,打开弹簧夹通空气,再熄灭酒精灯,直到玻璃管冷却
Ⅳ.再次称量装置C、D的质量,分别为m 3、m 4
请回答下列问题
(1)装置A中碱石灰的作用是
(2)装置C中所装药品为
(3)装置D中发生反应的化学方程式为
(4)装置E的作用
(5)依据实验所得数据计算,该样品中小苏打的质量分数为 (用相关字母表示)。
(6)误差分析。按上述实验步骤测得该样品中小苏打的质量分数 (填"偏大""偏小"或"准确"),理由是 。
试题篮
()