几种物质在不同温度时的溶解度如下表所示:
温度/℃ |
0 |
10 |
20 |
30 |
40 |
50 |
60 |
70 |
80 |
|
溶解度 /g |
NaCl |
35.7 |
35.8 |
36.0 |
36.3 |
36.6 |
37.0 |
37.3 |
37.8 |
38.4 |
KCl |
27.6 |
31.0 |
34.0 |
34.7 |
40.0 |
42.6 |
45.5 |
48.3 |
51.1 |
|
NH4Cl |
29.4 |
33.3 |
37.2 |
41.4 |
45.8 |
50.4 |
55.2 |
60.2 |
65.6 |
|
KNO3 |
14.3 |
20.9 |
31.6 |
45.8 |
63.9 |
85.5 |
110 |
138 |
169 |
|
请回答下列问题:
(1)20℃时,上述四种物质中溶解度最大的是 (填化学式,下同)。
(2)将温度为80℃、质量相同的上述四种物质的饱和溶液分别降温到20℃,析出 晶题体最多的是 。
(3)在某温度范围内NaCl和KCl的溶解度可能相等,该温度范围是 (填字母序号)。
A.10℃~20℃
B.20℃~30℃
C.30℃~40℃
D.40℃~50℃
(4)20℃时将20 gNaCl加入50g水中,充分溶解后所得溶液中溶质的质量分数是 (计算结果精确至 0.1%)。
氯化钠、碳酸钠、硝酸钾在不同温度时的溶解度如下表所示,某同学根据表中数据作出了其中一种物质的溶解度曲线(如图所示),请根据表和图中信息填空。
| 温度/℃ 溶解度/g 物质 |
0 |
10 |
20 |
30 |
40 |
| 氯化钠 |
35.7 |
35.8 |
36 |
36.5 |
37 |
| 碳酸钠 |
6 |
16 |
18 |
36.5 |
50 |
| 硝酸钾 |
13.3 |
20.9 |
31.6 |
45.8 |
63.9 |
(1)曲线M是表中 的溶解度曲线,该物质在5℃时的溶解度约为 g。
(2)如果将表中三种物质的溶解度曲线全部画出,在0℃~40℃范围内会有 个两线交点。
(3)10℃时,将15g氯化钠和15g硝酸钾固体同时加入盛有50g水的烧杯中,充分搅拌、溶解、静置后,烧杯底部剩余的固体是 。

硝酸钾和氯化钠在不同温度下的溶解度如下表,请回答。
温度/℃ |
20 |
40 |
60 |
80 |
100 |
|
溶解度/g |
硝酸钾 |
31.6 |
63.9 |
110 |
169 |
246 |
氯化钠 |
36.0 |
36.6 |
37.3 |
38.4 |
39.8 |
|
(1)60℃时硝酸钾的溶解度是 g。
(2)若硝酸钾中混有少量的氯化钠,提纯硝酸钾可以采取的方法是 。
(3)20℃时,将硝酸钾和氯化钠两种固体各36g分别加入盛有100水的烧杯中,充分溶解后可观察到如图所示的现象。
①烧杯A中溶解的物质是 。
②若向烧杯A中加入一定量的水使剩余固体刚好全部溶解变为饱和溶液,则溶液中溶质的质量分数 (填“变大”、“变小”或“不变”)。
③若将A、B烧杯中的物质同时升温至80℃,则A、B中溶质的质量 (填“一定”或“不一定”)相等。

KNO3和KCl在不同温度时的溶解度如下表所示:
温度/℃ |
0 |
10 |
20 |
30 |
40 |
50 |
60 |
70 |
KNO3 |
13.3 |
20.9 |
31.6 |
45.8 |
63.9 |
85.5 |
110 |
138 |
KCl |
27.6 |
31.0 |
34.0 |
37.0 |
40.0 |
42.6 |
45.5 |
48.3 |
回答下列问题:
(1)20℃时,KCl的溶解度为 g。
(2)依据表中数据,绘制KNO3和KCl的溶解度曲线,如图中能表示KCl溶解度曲线的是 (选填“a”或“b”)。
(3)20℃时,向10g水中加入2.5g KNO3充分搅拌得到X,再加入2.5g KNO3充分搅拌得到Y,继续升温至50℃得到Z,则X、Y、Z中为饱和溶液的是 。
(4)40℃时,现有质量均为100g的硝酸钾和氯化钾两种饱和溶液,若将它们同时降温至10℃.下列说法正确的是 。
A.40℃时,硝酸钾饱和溶液中水的质量大于氯化钾饱和溶液中水的质量
B.降温至10℃时,析出的KNO3晶体质量比析出的KCl晶体质量大
C.降温至10℃时,硝酸钾饱和溶液的质量分数大于氯化钾饱和溶液的质量分数
D.当温度降至20℃和30℃之间的某一温度,两种溶液的质量分数可能相等

溶液在生活、生产中具有广泛的用途。
(1)在20℃时,将20g氯化钾固体加入50g水中,充分搅拌后,仍有3g氯化钾固体未溶解。所得溶液中氯化钾的质量分数为 (计算结果保留一位小数);20℃时氯化钾的溶解度为 。
(2)甲、乙两种不含结晶水的固体物质的溶解度曲线如图。t1℃时,甲溶液的溶质质量分数与乙溶液的溶质质量分数相比,前者与后者的关系是 (填字母)。
A.大于 B.小于 C.等于 D.无法确定
(3)如图是实验室稀释浓硫酸的正确和错误操作,请说明不能将水直接倒入浓硫酸中进行稀释的原因 。


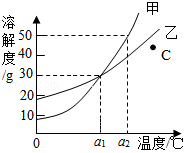
如图为甲、乙两种物质(均不含结晶水)的溶解度曲线。据此回答下列问题:
(1)当温度为 ℃时,甲、乙两种物质的溶解度相等。
(2)图中C点对应的乙溶液是 (填“饱和”或“不饱和”)溶液。
(3)当温度为a2℃时,在100g水中加入60g甲,溶液中溶质的质量分数为 (结果保留三位有效数字)。
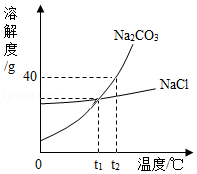
根据所给氯化钠和碳酸钠的溶解度及溶解度曲线的信息,回答下列问题:
温度 |
0℃ |
10℃ |
20℃ |
30℃ |
40℃ |
氯化钠 溶解度/g |
35 |
35.5 |
36 |
36.5 |
37 |
碳酸钠溶解度/g |
6 |
10 |
18 |
36.5 |
50 |
(1)t1℃时,NaCl的溶解度是 g。
(2)t2℃时,将40g Na2CO3固体加入50g水中,充分溶解后所得Na2CO3溶液中溶质与溶剂的质量比为 。
(3)若Na2CO3中混有少量的NaCl,提纯Na2CO3应采取的方法是 (填“降温结晶”或“蒸发结晶”)
如图是甲、乙、丙三种固体的溶解度曲线图。据图回答下列问题:
(1)乙、丙两物质在 ℃时溶解度相等。
(2)将t2℃时甲的饱和溶液变为不饱和溶液,在保证溶液质量不改变的前提下可采取的方法是 。
(3)t2℃时欲配制50g 15%的乙物质的溶液,需量取水 mL.(水的密度为1g•cm﹣3)
(4)t3℃时,将三种物质各ag分别加入100g水中,充分溶解后,只有一种物质形成不饱和溶液,则a的取值范围是 。

如表是NaCl、NH4Cl在不同温度时的溶解度。
温度/℃ |
0 |
20 |
40 |
60 |
80 |
|
溶解度/g |
NaCl |
35.7 |
36.0 |
36.6 |
37.3 |
38.4 |
NH4Cl |
29.4 |
37.2 |
45.8 |
55.2 |
65.6 |
|
(1)以上两种物质的溶解度受温度影响较大的是 。
(2)40℃时,将40.6g NaCl加入到100g水中,充分搅拌使之溶解,所得溶液的质量为 g。
(3)20℃时,NaCl饱和溶液的溶质质量分数为(精确到小数点后1位) 。
如图是甲、乙、丙三种物质的溶解度曲线。请根据图中信息回答下列问题:
(1)甲、乙两种物质在 ℃时溶解度相等;
(2)t3℃时,把30克甲充分溶解在50克水中,所得溶液质量是 g;
(3)t3℃时,甲、乙、丙三种物质的等质量饱和溶液中,所含溶剂质量最多的是 ;
(4)若甲中混有少量乙,要得到纯净的甲,常用的提纯方法是 。

请根据如图甲、乙、丙三种固体物质的溶解度曲线,回答下列问题。
(1)在 ℃时,甲、丙两种物质的溶解度相等;
(2)在t2℃时,向盛有25g甲物质的烧杯中加入50g水,充分溶解后,所得溶液的溶质质量分数为 。
(3)若乙物质中混有少量甲物质,最好采用 (填“降温结晶”或“蒸发结晶”)的方法提纯乙;
(4)t2℃时,甲、乙、丙三种物质的饱和溶液各100g,所含溶剂的质量由大到小的顺序是 。

如表是KNO3、NaCl在不同温度下的溶解度:
温度/℃ |
10 |
20 |
30 |
40 |
50 |
60 |
70 |
80 |
90 |
|
溶解度/g |
KNO3 |
20.9 |
32 |
45.8 |
64 |
85.5 |
110 |
138 |
169 |
202 |
NaCl |
35.8 |
36 |
36.3 |
36.6 |
37 |
37.3 |
37.8 |
38.4 |
39 |
|
根据上表信息,完成下列各题
(1)60℃时,KNO3的溶解度为 。
(2)溶解度受温度的影响较大的物质是 。
(3)10℃时,将KNO3和NaCl的饱和溶液同时升高温度到30℃,所得溶液中溶质的质量分数的大小关系是:前者 后者(填“大于”“小于”或“等于”)。
(4)20℃时,15g NaCl加入到40g水中充分溶解所得溶液的质量为 。
如图是甲、乙、丙三种固体物质的溶解度曲线。请根据图回答下列问题:
(1)在 ℃时,甲、丙两种物质的溶解度相等。
(2)若甲中混有少量的乙,提纯甲物质可采取的方法是 。
(3)在t2℃时,配制180g甲物质的饱和溶液,需要甲物质的质量是 g。
(4)t3℃时,将甲、乙、丙三种物质的饱和溶液各100g,分别降温到t1℃,对所得溶液的叙述正确的是 (填字母序号)。
A.溶质质量分数大小关系是:乙>甲>丙
B.溶剂质量大小关系是:丙>乙>甲
C.溶液质量大小关系是:丙>甲>乙

青海省柴达木盆地的察尔汗盐湖是我国最大的天然内陆咸水湖,当地农民通过“冬天捞碱,夏天晒盐”获得大量湖盐。
(1)“夏天晒盐”中的“盐”其溶解度可用图中 来表示(填“a”、或“b”、或“c”)。
(2)在t1℃时,三种物质的溶解度大小关系是 。
(3)在t2℃时,将40g的a放入50g水中充分搅拌,所得溶液质量为 g。
(4)将t2℃时a、b、c的饱和溶液降温至t1℃时,溶质的质量分数由大到小的顺序为 。

我国制碱工业的先驱一侯德榜成功地摸索和改进了西方的制碱方法。下表为侯氏制碱法中部分物质的溶解度。
温度/℃ |
10 |
20 |
30 |
40 |
|
溶解度/g |
Na2CO3 |
12.2 |
21.8 |
39.7 |
48.8 |
NaCl |
35.8 |
36.0 |
36.3 |
36.6 |
|
NaHCO3 |
8.2 |
9.6 |
11.1 |
12.7 |
|
(1)由上表可知,在10℃﹣40℃之间溶解度随温度变化最小的物质是 (填名称)。
(2)40℃时,将等质量的三种表中物质的饱和溶液降温至20℃,所得溶液中溶质的质量分数由大到小的顺序是 (用化学式表示)。
(3)侯氏制碱法制得的碱为纯碱,纯碱的化学式为 。
(4)制碱原理为向饱和的NaCl溶液中通入足量NH3和CO2生成 NaHCO3晶体和NH4Cl,NaHCO3加热分解即制得纯碱。
①生成 NaHCO3的化学方程式为 。
②结合上表分析,析出 NaHCO3晶体的原因可能有 (填序号)。
A.溶剂质量减少
B.同温下 NaHCO3溶解度小于NaCl
C.生成的NaHCO3质量大于消耗的NaCl质量
试题篮
()