下列四个图象分别对应四个变化过程,其中正确的是( )
| A. |
|
| B. |
|
| C. |
|
| D. |
|
下列操作或反应所对应的曲线正确的是( )
| A. |
|
| B. |
|
| C. |
|
| D. |
|
下列图象能正确反映其对应的实验操作的是( )
A.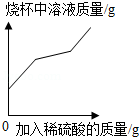 向盛有部分变质的氢氧化钠溶液的烧杯中滴加稀硫酸至过量
向盛有部分变质的氢氧化钠溶液的烧杯中滴加稀硫酸至过量
B.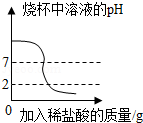 向盛有一定量的氢氧化钠溶液的烧杯中逐滴加入pH=2的稀盐酸至过量
向盛有一定量的氢氧化钠溶液的烧杯中逐滴加入pH=2的稀盐酸至过量
C.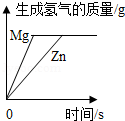 相同质量的镁、锌分别与足量的溶质质量分数相同的稀盐酸反应
相同质量的镁、锌分别与足量的溶质质量分数相同的稀盐酸反应
D.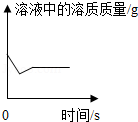 某温度时,向一定量的饱和氢氧化钙溶液中加入少量氧化钙,再恢复到原温度
某温度时,向一定量的饱和氢氧化钙溶液中加入少量氧化钙,再恢复到原温度
如图是甲、乙两种固体物质的溶解度曲线。下列说法正确的是( )

A.15℃时,甲和乙的饱和溶液中溶质质量相等
B.35℃时,30g甲加入50g水中,得到80g甲溶液
C.从乙溶液中获得乙晶体,常用蒸发结晶的方法
D.降低温度,甲溶液中溶质的质量分数一定减小
溶液与人类生产、生活密切相关。
(1)A、B、C三种固体物质的溶解度曲线如图所示。
①t1℃时,A、B、C三种物质的溶解度由大到小的顺序是 。
②A、B、C三种物质中,溶解度随温度升高而减小的是 。
③t2℃时,完全溶解agA物质最少需要水的质量是 g。
④t2℃时,相同质量的A、B饱和溶液中,A的饱和溶液中所含水的质量 B的饱和溶液中所含水的质量(填“大于”、“等于”或“小于”)。
(2)实验室欲除去粗盐样品中含有的不溶性泥沙,在过滤操作中需要用到的实验仪器和用品有:烧杯、铁架台(带铁圈)、玻璃棒、 和滤纸。
(3)在实验室中,配制溶质质量分数为10%的氯化钠溶液45g,需要氯化钠固体的质量是 g.将45g10%的氯化钠溶液配成含氯化钠为0.9%的溶液,得到氯化钠溶液的质量是 g。

下列四个图象分别对应四个变化过程,其中正确的是( )
A. 一定量的饱和石灰水中加入氧化钙
一定量的饱和石灰水中加入氧化钙
B. 常温下,相同质量的锌和铁分别与足量的溶质质量分数相同的稀硫酸反应
常温下,相同质量的锌和铁分别与足量的溶质质量分数相同的稀硫酸反应
C. 向硫酸和硫酸铜的混合溶液中滴加过量的氢氧化钠溶液
向硫酸和硫酸铜的混合溶液中滴加过量的氢氧化钠溶液
D. 向氢氧化钾溶液中不断加水,溶液的pH与加入水的质量关系
向氢氧化钾溶液中不断加水,溶液的pH与加入水的质量关系
下列关于溶液的说法错误的是( )
A.与乳化作用相比,溶解能使物质混合得更均匀
B.20℃时,50g水中溶解了15g的硝酸钾,则20℃时硝酸钾的溶解度是30g
C.一定温度下,固体物质的溶解度不随水的质量改变而改变
D.硝酸钾的饱和溶液恒温蒸发部分水后,剩余溶液溶质质量分数不变
如表是NaCl、NH4Cl在不同温度时的溶解度。
温度/℃ |
0 |
20 |
40 |
60 |
80 |
|
溶解度/g |
NaCl |
35.7 |
36.0 |
36.6 |
37.3 |
38.4 |
NH4Cl |
29.4 |
37.2 |
45.8 |
55.2 |
65.6 |
|
(1)以上两种物质的溶解度受温度影响较大的是 。
(2)40℃时,将40.6g NaCl加入到100g水中,充分搅拌使之溶解,所得溶液的质量为 g。
(3)20℃时,NaCl饱和溶液的溶质质量分数为(精确到小数点后1位) 。
如图所示,在分别盛有100g水的烧杯中放入KNO3充分溶解,则说法正确的是( )
温度(℃) |
t1 |
t2 |
KNO3的溶解度(g/100g水) |
60 |
90 |
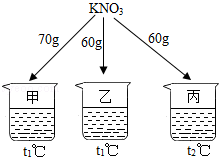
A.甲、乙混合后为t1℃的不饱和溶液
B.乙升温至t2℃,溶液质量增加
C.乙、丙溶液中溶质质量相等
D.丙降温至t1℃,有晶体析出
如图是对某固体物质的溶液在一定温度下,进行恒温蒸发操作的实验记录,请回答:

(1)乙中的溶液为 (填“饱和”或“不饱和”)溶液。
(2)该固体物质在当时温度下的溶解度为 。
(3)甲、乙、丙、丁中溶液溶质质量分数的大小关系是 。
(4)给丁中的溶液升高温度时,固体逐渐消失,说明该物质的溶解度随温度升高而 (填“增大”或“减小”)。
下表是KNO3在不同温度时的溶解度,回答问题。
温度/℃ |
30 |
40 |
50 |
60 |
70 |
80 |
90 |
溶解度/g |
45.8 |
63.9 |
85.5 |
110 |
138 |
169 |
202 |
(1)影响固体物质溶解度大小的因素有 (填一种)。
(2)30℃时KNO3溶液的溶质质量分数的最大值是 (只列出表达式)。
(3)90℃时,将一定质量的KNO3溶液按图示进行操作:

90℃时的KNO3溶液是 (填“饱和”或“不饱和”)溶液。图中n的数值为 。
如表是NaCl和KNO 3在不同温度时的溶解度,回答问题
| 温度/℃ |
10 |
20 |
30 |
40 |
50 |
60 |
|
| 溶解度/g |
NaCl |
35.8 |
36.0 |
36.3 |
36.6 |
37.0 |
37.3 |
| KNO 3 |
20.9 |
31.6 |
45.8 |
63.9 |
85.5 |
110.0 |
|
(1)两种物质中,溶解度受温度影响变化较大的是 。
(2)60℃时,按图示操作:

A中溶液是 (填"饱和"或"不饱和")溶液,C中溶液的总质量是 g。
(3)50℃时,将两种物质的饱和溶液各100g,分别加热蒸发10g水后,再恢复到50℃,剩余溶液的质量:NaCl溶液 (填"大于""等于"或"小于")KNO 3溶液。
小龙同学在工具书中查到NaOH在水和酒精中的溶解度(见右表).通过分析她得出以下结论,其中不正确的是( )
20℃ |
40℃ |
|
水 |
109g |
129g |
酒精 |
17.3g |
40g |
A.温度和溶剂种类对NaOH的溶解度都有影响
B.NaOH易溶于水,也易溶于酒精
C.40℃,40gNaOH溶解在l00g酒精中达到饱和
D.将等质量40℃的饱和NaOH水溶液和饱和NaOH酒精溶液降温至20℃,析出的晶体前者比后者多
甲图是A、B、C三种固体物质的溶解度曲线。
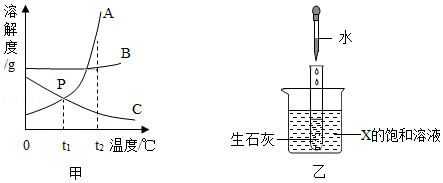
(1)甲图中,P点所表示的含义为 。
(2)t2℃时,在温度不变的情况下,将B物质的不饱和溶液转变成饱和溶液可采取的一种方法是 。
(3)将t2℃时A、B、C三种物质的饱和溶液降温到t1℃时,三种溶液的溶质质量分数由大到小的顺序是 。
(4)如乙图所示,20℃时,把试管放入盛有X的饱和溶液的烧杯中,在试管中加入一小块生石灰,再加入适量的水,烧杯中的溶液逐渐变浑浊,则X可能为 (填“A”或“B”或“C”)固体物质。
根据下表数据,回答下列问题。
温度/℃ |
10 |
20 |
30 |
40 |
50 |
60 |
70 |
80 |
90 |
|
溶解度/g |
KCl |
31.0 |
34.0 |
37.0 |
40.0 |
42.6 |
45.5 |
48.3 |
51.1 |
54.0 |
KNO3 |
20.9 |
31.6 |
45.8 |
53.9 |
85.5 |
110 |
138 |
160 |
202 |
|
(1)KCl 和KNO3中,溶解度受温度影响较小的是 ;
(2)30℃时,KCl饱和溶液中,KCl和H2O的质量比为 ;
(3)将200g KNO 3和2g KCl的混合物,投入到100g 90℃的水中完全溶解,再降温至20℃,析出晶体的化学式为 。
试题篮
()