以下四个图象与对应操作描述不相符的是( )
A. 水通直流电
水通直流电
B. 加热分解高锰酸钾
加热分解高锰酸钾
C. 向20mL pH=13的NaOH溶液中逐滴滴入pH=1的盐酸
向20mL pH=13的NaOH溶液中逐滴滴入pH=1的盐酸
D.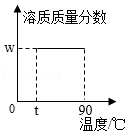 t℃时取溶质质量分数为w的KNO3饱和溶液20g,升高温度至90℃
t℃时取溶质质量分数为w的KNO3饱和溶液20g,升高温度至90℃
如图是a、b、c三种固体物质的溶解度曲线图,请判断下列说法,其中正确的是( )
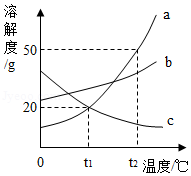
A.使a、c的饱和溶液析出晶体的方法都可以是降温结晶
B.t1℃时,a、c两种物质的溶液的溶质质量分数一定相等
C.在t2℃时,将a物质30g加入50g水中,充分溶解,所得溶液质量为80g
D.t2℃时,a、b、c三种物质的饱和溶液的溶质质量分数由大到小的关系是:a>b>c
现有编号为①、②、③的三个烧杯中均分别盛有100克水,20℃时向三个烧杯中分别加入36克、56克、76克的同种物质,充分溶解,实验结果如图所示,下列判断正确的是( )
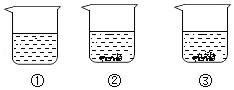
A.①中所得溶液一定是不饱和溶液
B.②③中所得溶液溶质的质量分数相等
C.若②中溶液升温到30℃,溶液的质量一定不变
D.若③中溶液恒温蒸发,溶质的质量分数一定变大
小金在配制硝酸钾溶液时得到下表数据,据此分析以下说法正确的是( )
| 序号 |
温度/℃ |
水的质量/克 |
加入硝酸钾的质量/克 |
所得溶液的质量/克 |
| ① |
10 |
100 |
40 |
120.9 |
| ② |
60 |
100 |
40 |
140 |
A.10℃时硝酸钾的溶解度为40克
B.②所得溶液一定是60℃时硝酸钾的饱和溶液
C.若通过加热将①中剩余硝酸钾全部溶解,则溶液的溶质质量分数与加热前保持一致
D.若将②所得溶液降温至10℃,则溶液的溶质质量分数会变小
本题有甲、乙两图,图甲为硝酸钾和氯化铵的溶解度曲线,图乙为兴趣小组进行的实验,R物质是硝酸钾或氯化铵中的一种。

关于图乙中烧杯内的物质,下列说法正确的是( )
A.R 物质是氯化铵
B.溶液的溶质质量分数是烧杯①小于烧杯②
C.若使烧杯③中的固体溶解,只能采用加水的方法
D.烧杯①②③中,只有烧杯③中上层清液是饱和溶液
如图是KNO3和NH4Cl的溶解度曲线,下列叙述错误的是( )
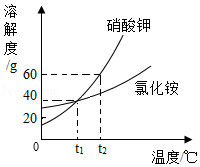
A.t1℃时,KNO3的溶解度与NH4Cl的溶解度相等
B.t2℃时,KNO3饱和溶液中溶质的质量分数是37.5%
C.t1℃时,NH4Cl的不饱和溶液降温,肯定无晶体析出
D.t2℃时,KNO3饱和溶液中溶质的质量分数大于NH4Cl饱和溶液中溶质的质量分数
在20℃时,将40g氯化钠固体加入100g水中,充分搅拌后,有4g固体未溶解。下列说法正确的是( )
A.20℃时,氯化钠的溶解度为36g
B.该溶液不能继续溶解硝酸钾固体
C.所得氯化钠溶液的质量为140g
D.将该溶液倒出一半,则溶质的质量分数改变
下列图象能正确反映其对应变化关系的是( )
A.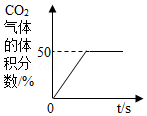 蜡烛在装满空气的密闭容器中燃烧,CO2体积分数的变化
蜡烛在装满空气的密闭容器中燃烧,CO2体积分数的变化
B.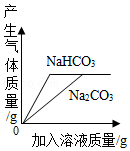 向等质量,等浓度的盐酸中不断加入Na2CO3和NaHCO3溶液,产生气体质量的变化
向等质量,等浓度的盐酸中不断加入Na2CO3和NaHCO3溶液,产生气体质量的变化
C.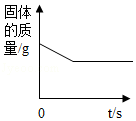 在高温下,向Fe2O3固体中通入CO,固体质量的变化
在高温下,向Fe2O3固体中通入CO,固体质量的变化
D.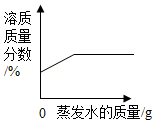 在恒温条件下,将饱和的NaCl溶液蒸发适量水,溶液中溶质质量分数的变化
在恒温条件下,将饱和的NaCl溶液蒸发适量水,溶液中溶质质量分数的变化
下列图象分别对应四个变化过程,能正确反映对应变化关系的是( )
| A. |
|
| B. |
|
| C. |
|
| D. |
|
向2个盛有100g 60℃水的烧杯中,分别加入40g的NaCl和KCl固体,充分溶解。根据实验和溶解度曲线判断,下列说法正确的是( )

A.①得到的溶液质量为140g
B.KCl的溶解度比NaCl的溶解度大
C.②得到的溶液为饱和溶液
D.②中溶液溶质的质量分数约为28.6%
关于如图所示实验的相关判断错误的是( )

A.固体X可能是NaOHB.固体X可能是NH4NO3
C.Ca(OH)2溶解度:①>②D.Ca(OH)2质量分数:①=③
下列图象不能正确反映对应变化关系的是( )
A.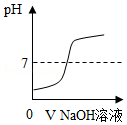 表示向pH=2的盐酸中不断加入NaOH溶液
表示向pH=2的盐酸中不断加入NaOH溶液
B.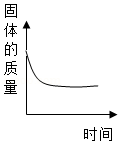 表示一定量的Fe加到AgNO3溶液中
表示一定量的Fe加到AgNO3溶液中
C.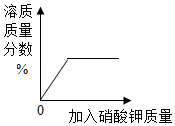 表示在20℃时,向一定量的水中不断加入KNO3晶体
表示在20℃时,向一定量的水中不断加入KNO3晶体
D.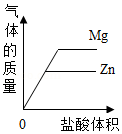 表示等质量的Mg和Zn分别加足量盐酸
表示等质量的Mg和Zn分别加足量盐酸
在20℃时,某固体物质(不含结晶水)的水溶液,经历如图变化( )
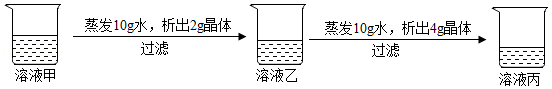
下列说法你认为正确的( )
A.溶液甲是饱和溶液
B.20℃时,该固体物质的溶解度是40g
C.溶液丙若蒸发10g水,析出的晶体一定大于4g
D.溶液乙溶质的质量分数小于溶液丙溶质的质量分数
下列能够反映物质组成的概念是( )
①溶解度 ②元素 ③溶质质量分数 ④有机物 ⑤溶液
A.①②③④⑤B.②③④⑤C.②③D.②
试题篮
()