在不同温度下,将一定量的NaCl和KNO3分别加入100 g水中,实验情况记录于下表中,有关结论正确的是
| 序号 |
温度 |
溶解情况 |
|
| 实验1 |
20 ℃ |
最多溶解36 g NaCl |
最多溶解31.6 g KNO3 |
| 实验2 |
40 ℃ |
加入36 g NaCl全部溶解 |
加入31.6 g KNO3全部溶解 |
| 实验3 |
80 ℃ |
最多溶解38.4 g NaCl |
最多溶解169 g KNO3 |
A.KNO3的溶解能力一定大于NaCl
B.40 ℃时NaCl的溶解度一定大于KNO3的溶解度
C.将实验3所得溶液分别降温至20 ℃后,两溶液中溶质的质量:NaCl < KNO3
D.将实验2所得溶液分别升温至80 ℃后,溶液的浓度:NaCl > KNO3
下图是甲、乙、丙三种固体物质的溶解度曲线,下列说法错误的是 ( )
| A.t2℃时,甲、乙两种物质的饱和溶液中的溶质质量相等 |
| B.甲的溶解度随温度的升高而增大 |
| C.分别将t3℃时甲、乙、丙的饱和溶液降温至t1℃,则所得的三种溶液中溶质的质量分数大小关系是乙>甲>丙 |
| D.t1℃时,丙的溶解度为40g |
右图是A、B、C三种物质的溶解度曲线。下列叙述正确的是 ( )
A.t1℃时三种物质的饱和溶液升温到t3℃所得溶液溶质质量分数大小关系为A>B>C
B.t2℃时,A、B两种物质的溶液中所含溶质质量相等
C.t2℃时,20g B溶解于50g水中能形成70溶液
D.若要将组成在N点的A溶液转变为M点的A溶液,可以采取恒温蒸发溶剂的方法
如图是甲、乙、丙三种物质的溶解度曲线。下列叙述正确的是
| A.60℃时,50克水中加入50克甲得到不饱和溶液的溶质与溶液质量比为4:9 |
| B.60℃三种物质的饱和溶液降到40℃时,乙析出晶体最多 |
| C.40℃时,丙和乙饱和溶液的溶质质量分数相同 |
| D.40℃时,三种物质的溶解度由大到小为:乙>甲>丙 |
夏天,实验员在实验室里配制了一瓶饱和的硝酸钾溶液并密封放置,到了冬天发现瓶底有大量的晶体析出。这是因为
| A.溶液中溶剂质量减小 | B.变成了不饱和溶液 |
| C.温度下降,硝酸钾溶解度减小 | D.溶液中溶质质量增加 |
右图是A、B两种固体物质的溶解度曲线,下列说法正确的是( )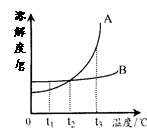
A.A的溶解度都大于B的溶解度
B.t1℃时,用等量水分别制成的A、B饱和溶液中,B的质量比A大
C.t2℃时,A、B两种饱和溶液中,溶质的质量分数相等
D.A、B两种饱和溶液都从t3℃降温到t2℃,析出的晶体一定等量
根据如图信息判断,下列叙述错误的是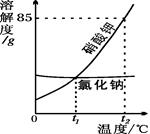
| A.硝酸钾的溶解度随温度升高而增大 |
| B.t1℃时,氯化钠和硝酸钾的溶解度相同 |
| C.要从含有少量氯化钠的硝酸钾溶液中得到较多的硝酸钾晶体,通常可采用降温结晶的方法 |
| D.t2℃时,80g硝酸钾溶于100g水中可制得饱和溶液 |
下表是NaCl、KNO3在不同温度时的溶解度:
跟据表内数据判断,下列说法错误的是
| A.KNO3和NaCl的溶解度曲线在20℃~30℃相交 |
| B.60℃时,向105g KNO3的饱和溶液中加入95g水,所得溶液的溶质的质量分数为27.5% |
| C.从含有少量NaCl的KNO3饱和溶液中得到较多的KNO3晶体,通常采用冷却热饱和溶液的方法 |
| D.20℃时,NaCl和KNO3固体各35g分别加入两只各盛有100g水的烧杯中,充分搅拌后均能形成饱和溶液 |
A、B、C三种物质的溶解度曲线如图所示,下列叙述正确的是( )
A.60℃的A、B、C三种物质的溶液中A物质的溶液中所含溶质的质量最多
B.60℃时A、B、C三种物质的等质量饱和溶液,降温至40℃时析出晶体最多的是A
C.40℃时A物质60g放入50g水溶解后升温至60℃时,溶质的质量分数增大,由饱和变为不饱和溶液
D.物质C中混有少量A时,可以用冷却热饱和溶液的方法提纯物质C
甲乙两物质的溶解度曲线如右图所示,下列说法正确的是
| A.甲物质的溶解度大于乙物质的溶解度 |
| B.t1℃时,甲、乙两物质的溶解度相等,均为30g |
| C.t2℃时,等质量的甲、乙溶解分别配成饱和溶液,所得溶液的质量乙大于甲 |
| D.甲的溶解度受温度影响较小 |
甲、乙两种固体的溶解度曲线如右图所示。下列说法中,正确的是
| A.40℃时,甲溶液的质量分数一定大于乙溶液的质量分数 |
| B.当乙中混有少量甲时,可采用冷却热饱和溶液的方法提纯 |
| C.20℃时,100 g甲的饱和溶液中溶质的质量是30 g |
| D.20℃时,分别在100 g水中加入50 g甲、乙,加热到40℃,甲、乙溶液均为饱和溶液 |
20℃右图是a、b两种固体物质的溶解度曲线,下列说法中,正确的是 
| A.20oC时,a物质的溶解度是5 |
| B.在20℃时,a、b溶液中溶质的质量分数相同 |
| C.a、b的溶解度均随温度升高而减小 |
| D.将b的不饱和溶液变为饱和溶液,可以通过降温实现 |
现有一杯20℃的饱和硝酸钾溶液,欲改变其溶质质量分数,下列方法可行的是
| A.升温到60℃ | B.恒温蒸发部分水 |
| C.加入一定量的水 | D.加入一定量的硝酸钾固体 |
右图是a、b、c三种物质的溶解度曲线。把t1℃时三种物质的饱和溶液温度升高到t2℃,则三种溶液的溶质质量分数大小关系是
| A.a>b>c | B.c>b>a |
| C.b>a=c | D.b>a>c |
x、y两物质(不含结晶水)溶解度曲线如图所示,在t2℃时分别往两份100g水中加入a克x和a克y充分搅拌后,将溶液均降温至t1℃,下列说法正确的是
| A.t1℃时,x、y两溶液均已饱和 |
| B.t1℃时,x、y的溶解度相等,且两溶液质质量分数相等 |
| C.t2℃时,x、y两溶液溶质质量分数相等,且两溶液均已饱和 |
| D.t2℃时,x、y两溶液中溶质质量分数不相等,且两溶液均不饱和 |
试题篮
()