为M、N两种固体物质的溶解度曲线,据图回答:
(1)b点表示的意义是 。
(2)t2℃时,将M溶液的状态由a点转化到b点,可采用的方法是 和 。
(3)将t1℃时,M和N的饱和溶液各100g降温至t0℃,过滤,得到滤液m和滤液n。关于m和n的说法正确的是 (填序号)。
A.都是饱和溶液 B.溶液质量:m<n C.溶剂质量:m<n
D.溶质质量:m=n E.溶质的质量分数:m=n

小明同学查阅了KCl和KNO 3在不同温度时的溶解度,并绘制出相应的溶解度曲线。
| 温度/℃ |
20 |
30 |
50 |
60 |
80 |
|
| 溶解度/g |
KCl |
34 |
37 |
42.6 |
45.5 |
51.1 |
| KNO 3 |
31.6 |
45.8 |
85.5 |
110 |
169 |
|
回答下列问题:
(1)图中表示KCl溶解度曲线的是 (填a或b)。
(2)60℃时,将KCl和KNO 3的饱和溶液同时降温到20℃,则所得溶液中溶质的质量分数大小关系是KCl KNO 3(填"大于"、"等于"或"小于")。
(3)KCl和KNO 3在t℃时具有相同的溶解度(m),则m的取值范围是 g。
(4)30℃时,将50g KNO 3固体放入100g水中充分溶解,所得溶液中溶质的质量分数为 (计算结果精确到0.1%)

如图所示是四种物质的溶解度曲线图,请回答下列问题。
(1)在60℃时,四种物质中溶解度最大的是 。
(2)将40℃时氯化钾的不饱和溶液,保持溶液温度不变,制成饱和溶液,可行的方法有 (举1例)。
(3)在t℃时,将30g氯化铵加入50g水中,充分溶解,所得溶液质量分数为 (精确到0.1%)。
(4)向饱和食盐水中加入足量的碳酸氢铵固体,会有溶解度较小的碳酸氢钠晶体析出,该反应的化学方程式是NaCl+NH4HCO3=NaHCO3↓+NH4Cl,请根据以上信息和图中物质的溶解度曲线,简述以硫酸铵固体为原料制取较纯硫酸钾晶体的方法: 。

材料一:侯德榜是我国著名的化学家,发明了侯氏制碱法,为纯碱和氮肥工业技术的发展作出了杰出的贡献。下面是实验室模拟侯氏制碱法原理的生产过程:
①20℃时,将CO 2通入含NH 3的饱和NaCl溶液中,生成 NaHCO 3晶体和NH 4Cl溶液。
②将①中的产物 NaHCO 3晶体充分加热分解,得到Na 2CO 3、H 2O和CO 2。
材料二:20℃时几种物质在水中的溶解度/g
| NaCl |
NH 4Cl |
NaHCO 3 |
| 36.0 |
37.2 |
9.6 |
请回答下列问题:
(1)在第①步反应中,有 NaHCO 3晶体析出,而没有NH 4Cl和NaCl晶体析出的原因是 。
(2)该生产过程中部分生成物可作为原料循环使用的是 ,同时得到的副产品NH 4Cl是一种氮肥。

在实验室小金分别用甲盐的晶体配置了溶质质量分数为5%的A溶液和30%的B溶液,但忘了贴标签,请你运用两种不同的科学原理,分别设计两个简单实验来判别这两瓶溶液。请写出简要的实验方案和明确的判别依据。有下列仪器、物品供选择:量筒、天平、
小烧杯、酒精灯、三脚架、石棉网、漏斗、玻璃棒、滤纸、温度计、新鲜罗卜、甲盐的晶体。
(实验室的室温为30℃,30℃甲盐的溶解度为50g)
方案1:
判别依据:
方案2:
判别依据:
化学和我们的日常生产、生活息息相关。请你用化学知识解释下列问题:
(1)打开汽水瓶盖时,为什么汽水会自动喷出来?
(2)工业用稀盐酸除铁锈的原理(用化学方程式表示)
、
、
三种物质的溶解度曲线图如图一与图二所示,请回答:

(1)由图一可知,20℃时氯化钠的溶解度为g.
(2)依据图一分析下列问题:50℃时,将氯化钠、硝酸钾固体各40g分别加入两只各盛有100g水的烧杯中,充分搅拌,其中(填写物质化学式)得到饱和溶液;另一种物质的溶液中再加入g该溶质,溶液恰好饱和;若将温度都降到20℃,硝酸钾溶液中溶质的质量分数(填">"、"<"或"=")氯化钠溶液中溶质的质量分数.
(3)依据图一分析,要从含有少量硝酸钾的氯化钠溶液中,得到较纯净的氯化钠固体,可采用先再过滤的物理方法.
(4)如图三所示,20℃时,将盛有饱和石灰水的小试管放入盛水的烧杯中,向水中加入氢氧化钠固体,结合图二分析石灰水中可能出现的现象.
(1)根据钠元素在元素周期表中的信息,将下图方框内①-⑤项内容补充完整:

(2)硝酸钾与氯化钾的溶解度曲线如图所示,回答下列问题:

①
时,两物质中溶解度较大的是。
②
时,两物质的等质量饱和溶液降温至t1℃,析出固体质量较大的是的溶液。
③
时,将100g水加入盛有50g氯化钾的烧杯中,充分溶解后,得到氯化钾的(填"饱和"或"不饱和")溶液。保持温度不变,往该烧杯中再加入10g水,充分搅拌后,氯化钾溶液的溶质的质量分数(填"变大"、"不变"或"变小")。
④欲配制溶质的质量分数为20%的硝酸钾溶液,应满足的温度范围是。
(3)某同学进行下图所示实验,证明酸碱发生反应的现象为:试管中溶液由色变为无色,该反应的化学方程式。实验后测得试管中溶液的pH=2,该溶液中的溶质有(写名称)。

甲、乙、丙三种固体物质的溶解度曲线如图所示,请回答:
(1)t1℃时,甲物质的溶解度 (填“大于”、“小于”或“等于”)乙物质的溶解度。
(2)t1℃时,100g水中最多能溶解丙物质 g。
(3)t2℃时,把等质量的甲、乙两物质的饱和溶液降温到t1℃,析出晶体较多的是 。
(4)t2℃时,向盛有100g水的烧杯中加入60g甲物质,充分溶解后,所得溶液溶质的质量分数是 (计算结果精确到0.1%)。
我国化学家侯德榜创立的侯氏制碱法,就是以海水晒盐得到的氯化钠为原料,制得纯碱碳酸钠,碳酸钠和氯化钠的溶解度曲线如图所示,试回答下列问题:
(1)t2℃时,氯化钠的溶解度 碳酸钠的溶解度。
(填“大于”“小于”“等于”之一)。)
(2)我国某些盐湖出产天然碱(主要成分是纯碱,并含有少量氯化钠杂质)。在实验室里,从天然碱中分离出较纯净的纯碱晶体应采用 的方法。
(3)在实验室中,若要测定盐湖水的酸碱性强弱,可以使用 测定。
(4)氯化钠通常采取海水晒盐的方法获得,其原因是 。
(5)在侯氏制碱法中碳酸钠是由碳酸氢钠加热分解得到的,试写出你所了解的碳酸氢钠在生活中的一项用途: 。
中国网新闻中心报道,2014年3月30日菲律宾向联合国国际海洋法法庭递交所谓的南海主权仲裁请求,中方表示不接受仲裁。南海是我国的固有领海,南海蕴藏着丰富的海洋资源.
(1)南海海底蕴含大量新型矿产资源—“可燃冰”,它是天然气(主要成分CH4)和水形成的冰状固体,极易燃烧,是一种清洁能源。写出CH4燃烧的化学方程式
,属于 反应类型。(从“置换”、“复分解”、“化合”、“氧化”中选择)
(2)我国化学科学家侯德榜创立的侯氏制碱法,就是以海水“晒盐”得到的氯化钠为原料制得Na2CO3。
Na2CO3和NaCl的溶解度曲线如图所示.回答下列问题:
①t1℃时,Na2CO3饱和溶液的溶质质量分数
NaCl 的。(填“大于”“小于”“等于”之一)
②生活在盐碱湖附近的人们有一句谚语“夏天晒盐,冬天捞碱”,请结合溶解度曲线,说明这句谚语的原理:
。
下图是a、b、c三种物质的溶解度曲线a与c的溶解度曲线相交于P点。
(1)P点的含义是 。
(2)t2℃时30g a物质加入到50g水中不断搅拌,能形成80g溶液吗? (填写“能”或“不能”)。
(3) t2℃时a、b、c三种物质的溶解度按由小到大的顺序排列是 (填写物质序号)。
(4)将t1℃时a、b、c三种物质饱和溶液的温度升高到t2℃时,三种溶液的溶质质量分数大小关系是 (填写选项序号)。
| A.c>a=b | B.a=b>c | C.a>b>c | D.b>a>c |
上图为氯化钠和硝酸钾固体的溶解度曲线.认真观察该图,回答下列有关问题: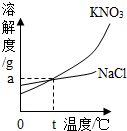
(1)根据该图可知:氯化钠的溶解度受温度影响变化不大,由该图你还获得哪些信息?(至少写出两条)
(2)若将t℃时硝酸钾饱和溶液转化为不饱和溶液,你有什么方法?
下图是甲、乙两种固体物质的溶解度曲线。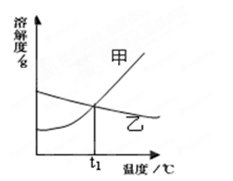
(1)在t1℃时,甲、乙两种固体物质的溶解度 (填相等或不相等);
(2)把甲物质的不饱和溶液变成饱和溶液,下列有关说法正确的是 (填字母序号);
| A.溶剂的质量一定变小 |
| B.溶质的质量一定不变 |
| C.该饱和溶液还可以溶解其他物质 |
| D.溶液的质量可能不变 |
(3)在实验室中,用固体物质甲和水配制成一定溶质质量分数的溶液,需用到的仪器有:烧杯、药匙、胶头滴管、 和 。
试题篮
()