如图是甲、乙两种固体的溶解度曲线,回答下列问题:
(1)甲、乙溶解度相等时的温度为 ℃。
(2)t2℃时,将70g乙的饱和溶液与30g水混合,所得溶液中溶质的质量分数为 。
(3)将t2℃时的甲、乙饱和溶液各100g,分别降温至t1℃,所得溶液中溶质的质量的关系为:甲 乙(填“>”“<”或“=”)。
(4)甲中混有少量的乙,若提纯甲应采用的方法是 。

根据如图所示的实验过程和提供的数据进行计算:

(1)原混合物中NaCl的质量。(要求写出计算过程)
(2)AgNO3溶液溶质质量分数为 (精确到0.1%)
往80g含有硝酸铜和硝酸银的混合溶液中加入一定量的镁粉,加入的镁粉的质量与溶液质量变化如图所示。试分析计算:
(1)a→b段表示镁粉与混合溶液中的 反应。(填化学式)
(2)原混合溶液中硝酸铜的质量分数是多少?(写出计算过程,精确到0.1%)

某同学为定量研究氢氧化钠溶液与盐酸反应,做了如下实验:取40g氢氧化钠溶液,加入到50g溶质质量分数为7.3%的稀盐酸中,恰好完全反应。计算:
(1)氢氧化钠溶液中溶质的质量分数是 。
(2)反应后所得溶液中溶质的质量分数。(写出计算过程)
硝酸钾在不同温度下的溶解度数据如下表所示:
| 温度/℃ |
0 |
20 |
40 |
60 |
80 |
| 溶解度/g |
13.3 |
31.6 |
63.9 |
110 |
169 |
回答下列问题:
(1)20℃时,将18g硝酸钾加入到50g水中,充分溶解后,所得溶液的质量是 g。
(2)80℃时,将269g硝酸钾饱和溶液降温到60℃,析出晶体的质量是 g。
(3)0℃时,硝酸钾饱和溶液中溶质的质量分数是 。(结果精确到0.1%)
(4)将40℃的硝酸钾饱和溶液变为不饱和溶液,可采取的措施是 。
为测定某工厂排放的废水中氢氧化钠的含量,化学兴趣小组将100g该废水与50g硫酸铜溶液混合恰好完全反应,得到4.9g沉淀。请计算这一废水中氢氧化钠的质量分数。
将91.6g氢氧化钾溶液与一定质量的氯化镁溶液混合,恰好完全反应,过滤后,得到11.6g沉淀和280g滤液,求氯化镁溶液的溶质质量分数.
下列选项中相关量的变化与图象不相符的是( )
选项 |
X |
Y |
|
A.向一定量饱和食盐水中加水 |
水的质量 |
溶质质量 |
|
B.向一定量锌粒中加稀硫酸 |
稀硫酸质量 |
氢气质量 |
|
C.向一定量CuCl2溶液中加NaOH溶液 |
NaOH溶液质量 |
沉淀质量 |
|
D.向一定量水中加KNO3晶体 |
KNO3晶体质量 |
溶质质量分数 |
A.AB.BC.CD.D
室温时,往盛有10.6g碳酸钙和氧化钙混合粉末的烧杯中加入100g稀盐酸,恰好完全反应,得到108.4g该温度下的不饱和溶液,则下列判断不正确的是( )
A.生成CO2为2.2g
B.原固体混合物中钙元素为6g
C.所得溶液中溶质的质量为15g
D.所加稀盐酸的溶质质量分数为10.95%
向182.5g一定浓度的盐酸中加入一定量的锌粉(杂质不溶于水也不与盐酸反应)
| 加入锌粉的质量/g |
7.0 |
14.0 |
21.0 |
28.0 |
35.0 |
42.0 |
| 溶液的质量/g |
188.8 |
195.1 |
a |
207.7 |
214.0 |
214.0 |
分析数据,试计算[第(2)问需写出计算过程]
(1)a= 。
(2)盐酸中溶质的质量分数?
为测定某盐酸的溶质质量分数,同学们进行了如下实验:将该盐酸逐滴加入到盛有20g 4%的氢氧化钠溶液的烧杯中,用玻璃棒不断搅拌,并测定溶液的pH.当pH=7时,共用去该盐酸14.6g.
(1)实验过程中,搅拌的目的是 .
(2)计算该盐酸的溶质质量分数.
中华文化源远流长,早在西汉时期《淮南万毕术》一书中就有“曾青得铁则化为铜”的记载,这是我国现代“湿法炼铜”的先驱。某大型工厂利用此原理处理含硫酸铜的废液回收金属铜时,向100kg的废液中加入足量的铁粉,得到金属铜6.4kg。
(1)计算废液中硫酸铜的质量分数是多少?
(2)金属资源保护的有效途径之一是金属的回收再利用,其它有效途径还有 (写一条)。
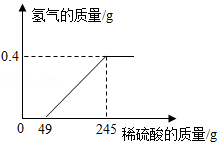
小明用镁条(表面被氧化)和稀硫酸反应的实验来测定稀硫酸的溶质质量分数。实验中,他绘制了生成氢气的质量与所用稀硫酸质量的关系图(如图),请根据如图计算该稀硫酸的溶质质量分数。
实验室测定一瓶稀硫酸中溶质的质量分数,取该稀硫酸100g,加入足量的氯化钡溶液,完全反应后生成46.6g沉淀.试计算该稀硫酸中溶质的质量分数.
某化学课外活动小组的同学在学习《化学》下册77页的资料卡片“石笋和钟乳石的形成”时,发现难溶于水的CaCO3当遇到溶有CO2的水时,会反应生成溶解性较大的Ca(HCO3)2:【CaCO3+CO2+H2O═Ca(HCO3)2】.联想到实验室检验CO2时,将气体通入澄清石灰水中.若长时间往澄清石灰水中通入CO2会产生什么样的现象呢?小组决定用小烧杯盛装一定量的氢氧化钠溶液并不断通入二氧化碳气体进行探究
【提出问题】氢氧化钠溶液中通入二氧化碳一段时间后,溶液中含有什么溶质?
【查阅资料】
(1)通入少量的二氧化碳时,NaOH与CO2反应的化学方程式为: .
(2)通入过量CO2时,反应的化学方程式为:Na2CO3+CO2+H2O═2NaHCO3.
(3)碳酸氢盐都是可溶于水的.BaCO3难溶于水且是白色固体.
(4)Na2CO3、NaHCO3溶液呈碱性,BaCl2显中性.
【提出猜想】
(1)溶质为NaOH和Na2CO3;
(2)溶质为Na2CO3;
(3)溶质是 (填化学式);
(4)溶质全都是NaHCO3.
【设计实验方案】
实验步骤 |
实验现象 |
实验结论 |
①用试管取少量小烧杯中反应后的溶液,滴加几滴 试液(填酸碱指示剂) |
溶液变红色 |
该溶液显碱性 |
②将小烧杯中反应后剩下的溶液进行称量,然后滴加过量的BaCl2溶液 |
有 生成 |
猜想(4)不成立 |
③取步骤②中的上层清液,滴入稀盐酸 |
有气泡冒出 |
猜想(1)和(2)不成立 |
【得出结论】猜想(3)成立.
【讨论交流】
(1)有同学提出实验步骤①是多余的.你认为该实验设计是否需要?并说明理由 .
(2)将实验步骤②剩下混合物进行 (填操作名称)、洗涤、干燥、称量,发现所得沉淀质量等于步骤②中所称量的溶液质量的十分之一,判断氢氧化钠溶液中通入二氧化碳一段时间后,溶液中 Na2CO3的质量分数约为 .
A.4.26% B.5.38% C.3.43%.10%
【反思应用】
验证二氧化碳性质时,如果长时间向澄清石灰水中通入二氧化碳会看到什么样的现象呢?请你描述一下 .
试题篮
()