现有A~G七种物质,已知A是赤铁矿的主要成分,B是可燃性气体单质,G溶液为蓝色,它们之间存在如图所示的转化关系:
(1)写出下列物质的化学式:
D: ; F: ;
(2)写出反应的化学方程式及实验现象
反应① ;
实验现象 ;
反应② ;
实验现象 。
(3)在反应①②③中,属于置换反应的是 (填序号)。
某Fe3O4样品中可能含有的杂质是Fe2O3和FeO其中的一种。为探究杂质的情况设计如下方案:
【实验设计】同学们称取了23.28 g该Fe3O4样品用图①进行了下列实验: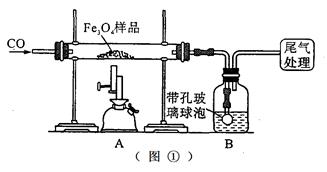
【实验分析】因探究思路不同,兴趣小组分成甲、乙、丙三个讨论小组。
甲组;(1)该组同学欲通过B装置反应前后的质量变化来计算确认该Fe3O4样品中的杂质。B中的最佳试剂是______(填序号)。
①澄清石灰水 ②氢氧化钠浓溶液 ③稀盐酸 ④水
(2)上述实验过程中,CO的作用有_______ (填序号)。
①CO气体作为反应物
②实验开始时,排尽装置中的空气,防止加热时发生爆炸
③停止加热后,防止A中生成物被氧化
④停止加热后防止B中的溶液倒吸入A中
⑤对B中反应物起到一定的搅拌作用,便于CO2与反应液充分接触而反应
乙组:
(3)乙组同学认为B装置反应前后的质量差会偏小而影响计算、分析,你认为他们的理由是_______ ;改进为在B装置后接一盛有_______(填试剂名称)的广口瓶的吸水装置,将B装置和该装置“捆绑”称量,从而减小误差。
丙组:
(4)丙组同学将B装置中液体改换为Ba(OH)2溶液,通过测量生成的_______(填化学式)沉淀的质量来计算求解。为了获得沉淀,该组同学需要进行的操作有过滤→_______→________→称量。
【查阅资料】
Fe2O3和CO反应是随温度升高而逐步进行的,先生成Fe3O4,再生成FeO(黑色),最后生成Fe;利用仪器测定并绘制成反应过程中A装置中玻璃管内的固体质量随温度的变化曲线(见图②)。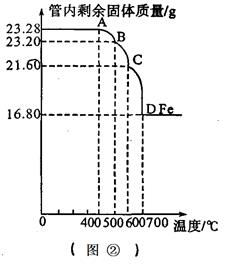
(5)写出BC段发生反应的化学方程式:______________ 。
(6)确定该Fe3O4样品中含有的杂质是_______,其中含Fe3O4的质量是_______g(不需要写出过程)(已知Fe3O4、FeO、Fe2O3中铁元素的质量分数分别为72.4%、77.8%、70.0%)。
钢铁是重要的金属材料,在工农业生产和生活中应用非常广泛。
Ⅰ.铁的应用
(1)下列铁制品的利用与金属导热性有关的是________________(填字母,下同)。
A.铁钳 B.铁锅 C.刀具
(2)“纳米α-Fe粉”可以用于食品保鲜,称之为“双吸剂”,因为它能吸收空气中的________________。
Ⅱ.铁的冶炼
工业炼铁的原理是高温下用CO作还原剂,将铁从氧化物中还原出来。请回答下列问题:
(1)写出以赤铁矿为原料,在高温下炼铁的化学方程式:___________________________;
(2)高炉炼铁中,焦炭的作用除了可以生成一氧化碳外,还能_____________________;
Ⅲ.实验探究炼铁原理
某化学兴趣小组在实验室中模拟工业炼铁的原理,并探究CO与Fe2O3反应后的产物。
通过查阅资料知道:①草酸(H2C2O4)固体与浓硫酸混合加热会产生一氧化碳,反应方程式为:H2C2O4  CO↑+ CO2↑+ H2O。
CO↑+ CO2↑+ H2O。
②NaOH溶液可以吸收二氧化碳,反应方程式为:2NaOH+CO2=Na2CO3+H2O
③常温下,Ca(OH)2微溶于水;于是他设计了下图的实验装置,结合装置回答下列问题:
(1)图A是用固体草酸和浓硫酸制取CO的反应装置,你认为应选择下图中的_________(填装置编号);
(2)图中装置C、D的作用分别是 ____________、_______________;
(3)为了证明产物中有二氧化碳,装置F中的试剂应该是少量的_____________(填试剂名称),反应的化学方程式为 ______________________;
(4)该装置设计有一个明显缺陷,你认为是______________________________。
(5)实验时准确称取一定质量纯净的Fe2O3固体按上图进行实验,当E中固体全部变黑后,继续通入CO直到玻璃管冷却。将得到黑色的固体加入到足量的稀盐酸,发现固体全部溶解,但无气泡产生。
查阅资料:a. 铁的氧化物在足量的稀盐酸中均能全部溶解。
b. Fe2O3与CO反应的固体生成物可能情况如下: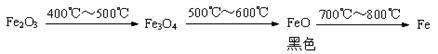
根据“无气泡”猜想,黑色粉末可能是:①Fe3O4;②_________ ③____________。
(6)定量分析 用电子天平称量得部分数据如下:
| |
玻璃管质量 |
玻璃管及其中固体的质量 |
装置F及其中物质的总质量 |
| 反应前 |
28.20 g |
33.00 g |
300.0 g |
| 反应后 |
32.84 g |
300.4 g |
根据上述数据,纯净的Fe2O3固体质量为_____________g,请选择有效的数据,推断出反应后黑色固体的成分(写出计算过程)__________________________。
根据推断结果,写出该实验中玻璃管内发生的化学反应方程式:__________________________。
Ⅰ.某研究性学习小组的同学学习了二氧化碳的性质后,对二氧化碳溶于水的过程,有没有发生化学变化?提出实验改进:用如图所示装置进行实验,验证二氧化碳能与水反应(已知氮气的密度小于空气的密度),操作为:
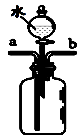
①从a端通入二氧化碳 ②从分液漏斗中滴加适量水 ③将石蕊溶液染成紫色的干燥纸花放入广口瓶中 ④从b端通入氮气
实验操作顺序最合理的是 ,发生变化的化学方程式为: 。
Ⅱ.另一小组在课外活动时对“二氧化硫能否与水反应生成酸”进行了实验探究。请你参与他们的探究活动,并回答有关问题。
[查阅资料]常温下二氧化硫是一种无色气体,易溶于水。
[假 设]二氧化硫能与水反应生成酸。
[设计实验] (1)小雨同学将二氧化硫气体通入紫色石蕊试液中,观察溶液颜色的变化。他认为,若紫色石蕊试液变 色,则证明假设成立。
(2)小涛同学认为小雨同学的实验方案不严密。小涛同学用紫色石蕊试液将白色滤纸染成紫色,干燥后做成三朵紫色的小花,然后按下列图示进行实验,在(I)、(Ⅱ)、(Ⅲ)中分别观察到变色和不变色的两种现象。
小涛同学认为,若 (填序号)中的紫色小花变色,则证明假设成立。

[交流反思]小明同学对小涛同学的实验方案提出了质疑,他认为上述实验还不足以证明“二氧化硫和水反应生成了酸”,其理由是 。三位同学讨论后补充了一个实验,使探究活动获得了成功,你认为这个实验应该是 (简述实验步骤和现象)。
[结 论]通过上述实验得出:二氧化硫能与水反应生成酸。
Ⅲ、人类的生产和生活都离不开金属。金属元素在自然界中分布很广,在地壳中主要以矿物形式存在。

下列矿石的主要成分不属于氧化物的是 (填序号),如将一定量的铁加入到硫酸铜和硫酸锌的混合溶液中,充分反应后,滤液中一定含有的溶质是 ,滤渣中一定含有 。
钢铁是重要的金属材料,在工农业生产和生活中应用非常广泛。
Ⅰ.铁的应用
(1)下列铁制品的利用与金属导热性有关的是 (填字母,下同)。
A.铁钳 B.铁锅 C.刀具
(2)“纳米α-Fe粉”可以用于食品保鲜,称之为“双吸剂”,因为它能吸收空气中的 。
Ⅱ.铁的冶炼
工业炼铁的原理是高温下用CO作还原剂,将铁从氧化物中还原出来。请回答下列问题:
(1)写出以赤铁矿为原料,在高温下炼铁的化学方程式: ;
(2)高炉炼铁中,焦炭的作用除了可以生成一氧化碳外,还能 ;
Ⅲ.实验探究炼铁原理
某化学兴趣小组在实验室中模拟工业炼铁的原理,并探究CO与Fe2O3反应后的产物。
通过查阅资料知道:①草酸(H2C2O4)固体与浓硫酸混合加热会产生一氧化碳,反应方程式为:H2C2O4  CO↑+ CO2↑+ H2O。
CO↑+ CO2↑+ H2O。
②NaOH溶液可以吸收二氧化碳,反应方程式为:2NaOH+CO2=Na2CO3+H2O
③常温下,Ca(OH)2微溶于水;
于是他设计了下图的实验装置,结合装置回答下列问题:
(1)图A是用固体草酸和浓硫酸制取CO的反应装置,你认为应选择下图中的 (填装置编号);
(2)图中装置C、D的作用分别是 、 ;
(3)为了证明产物中有二氧化碳,装置F中的试剂应该是少量的 (填试剂名称),反应的化学方程式为 ;
(4)该装置设计有一个明显缺陷,你认为是 。
(5)实验时准确称取一定质量纯净的Fe2O3固体按上图进行实验,当E中固体全部变黑后,继续通入CO直到玻璃管冷却。将得到黑色的固体加入到足量的稀盐酸,发现固体全部溶解,但无气泡产生。
查阅资料:a. 铁的氧化物在足量的稀盐酸中均能全部溶解。
b. Fe2O3与CO反应的固体生成物可能情况如下:
根据“无气泡”猜想,黑色粉末可能是:①Fe3O4;② ③ 。
(6)定量分析 用电子天平称量得部分数据如下:
| |
玻璃管质量 |
玻璃管及其中固体的质量 |
装置F及其中物质的总质量 |
| 反应前 |
28.20 g |
33.00 g |
300.0 g |
| 反应后 |
32.84 g |
300.4 g |
根据上述数据,纯净的Fe2O3固体质量为 g,请选择有效的数据,推断出反应后黑色固体的成分。(写出计算过程) 。
根据推断结果,写出该实验中玻璃管内发生的化学反应方程式:
(6分)某化学实验小组用一块表面镀锌的铁样品进行实验探究活动。
【实验探究】将表面镀锌的铁进行如图A实验,加入稀盐酸与产生氢气的质量关系如图B。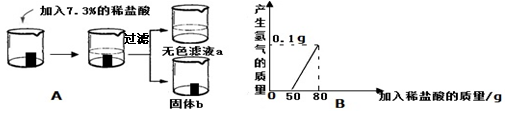
【提出问题】反应后所得的无色滤液a的溶质与固体b的成分是什么?
【猜想假设】秦思认为无色滤液a的溶质是(1) 、氯化亚铁和氯化氢。
【反思评价】请你评价秦思的猜想(2) 。
【推理判断】由无色滤液a 的成分可推知,固体b中一定含有(3) 。
【实验与结论】为验证固体b的成分,单杰向b的样品中加入一种有色物质(4) (填化学式)溶液,产生的现象是(5) ,据此现象,证明出固体b中的两种成分,同时得出这两种金属的活动性顺序。
【表达交流】石建向固体b中继续滴加少量稀盐酸也确定出固体b的成分,他观察到的现象是
(6) 。
【拓展延伸】通过比较锌、铁的活动性,结合图像B在开始加入稀盐酸的过程中并没有产生氢气的现象,你认为在铁的表面镀锌的原因是(7) ,可阻止进一步氧化。
常温下甲酸(HCOOH)是一种无色、有刺激性气味的液体,与浓硫酸混合加热的反应为:HCOOH CO↑+H2O。实验室可利用下图装置制取CO并还原CuO。下列说法不正确的是
CO↑+H2O。实验室可利用下图装置制取CO并还原CuO。下列说法不正确的是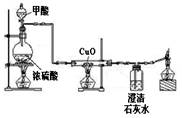
| A.甲酸生成CO的反应属于分解反应 |
| B.实验中应先加热CuO,后通入CO气体 |
| C.硬质玻璃管中的实验现象是黑色固体变为红色固体 |
| D.硬质玻璃管和其中固体的总质量反应后减小 |
铁生锈探秘
为探究铁生锈的原因,化学兴趣小组的同学进行了如图所示的四个实验:
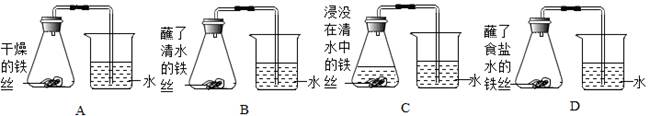
实验结果显示:B、D实验中铁生了锈,而A、C实验中没有明显的现象,仔细分析这4 个实验,回答下列问题:
(1)评价方案
对照实验指除了一个变量外,其他的量都保持不变的实验.该实验方案中采用了对照实验方法.请指出其中的对照实验(填ABCD实验代号)和变量.
第①组对照实验,变量.
第②组对照实验,变量.
第③组对照实验,变量.
(2)解释数据
实验时,每隔一段时间测量导管内水面上升的高度,结果如下表所示(表中所列数据为导管中水面上升的高度/cm ):
| 时间/小时 编号 |
0 |
0.5 |
1.0 |
1.5 |
2.0 |
2.5 |
3.0 |
| A |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
| B |
0 |
0 |
0 |
0.3 |
0.8 |
2.0 |
3.5 |
| C |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
| D |
0 |
0.4 |
1.2 |
3.4 |
7.6 |
9.5 |
9.8 |
导致B、D实验装置中导管内水面上升的原因是.
(3)获得结论
根据本实验,你认为导致铁生锈的物质有;能加快铁生锈的物质是.
钢铁是重要的金属材料,在工农业生产和生活中应用非常广泛。
Ⅰ.铁的冶炼
工业炼铁的原理是高温下用CO作还原剂,将铁从氧化物中还原出来。请回答下列问题:
(1)高炉炼铁中,焦炭的作用除了可以生成一氧化碳外,还能 ;
(2)某钢铁厂每天消耗5000t含氧化铁80%的赤铁矿石,该厂理论上可日产含铁98%的
生铁的质量是多少?
Ⅱ.实验探究炼铁原理
某化学兴趣小组在实验室中模拟工业炼铁的原理,并探究CO与Fe2O3反应后的产物。
通过查阅资料知道:
①草酸(H2C2O4)固体与浓硫酸混合加热会产生一氧化碳,反应方程式为:H2C2O4  CO↑+ CO2↑+ H2O。
CO↑+ CO2↑+ H2O。
②NaOH溶液可以吸收二氧化碳,反应方程式为:2NaOH+CO2=Na2CO3+H2O
③常温下,Ca(OH)2微溶于水;
于是他设计了下图的实验装置,结合装置回答下列问题:
(1)图A是用固体草酸和浓硫酸制取CO的反应装置,你认为应选择下图中的 (填装置编号);
(2)图中装置C、D的作用分别是 、 ;
(3)为了证明产物中有二氧化碳,装置F中的试剂应该是少量的澄清石灰水,该反应的化学方程式为 ;
(4)该装置设计有一个明显缺陷,你认为是 。
(5)实验时准确称取一定质量纯净的Fe2O3固体按上图进行实验,当E中固体全部变黑
后,继续通入CO直到玻璃管冷却。将得到黑色的固体加入到足量的稀盐酸,发现
固体全部溶解,但无气泡产生。
查阅资料:a. 铁的氧化物在足量的稀盐酸中均能全部溶解。
b. Fe2O3与CO反应的固体生成物可能情况如下: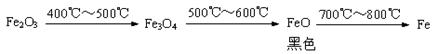
根据“无气泡”猜想,黑色粉末可能是:①Fe3O4;② ③ 。
(6)定量分析 用电子天平称量得部分数据如下:
| |
玻璃管质量] |
玻璃管及其中固体的质量 |
装置F及其中物质的总质量 |
| 反应前 |
28.20 g |
33.00 g] |
300.0 g |
| 反应后 |
32.84 g |
300.4 g |
根据上述数据,请选择有效的数据,推断出反应后黑色固体的成分。(写出计算过程) 。
右图是关于铁的化学性质的知识网络图(箭头表示转化方向,部分反应物、生成物省略),其中B是可燃性气体单质,C为红色金属,D是疏松多孔的红色物质---铁锈。请回答下列问题: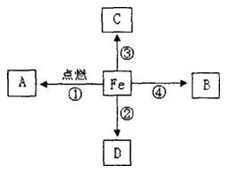
(1)反应①在盛有氧气的集气瓶里发生时,现象是________;A的化学式为________。
(2)D物质为铁锈,其主要成分的化学式为________________。
(3)写出反应③的化学方程式________________________。
(4)写出B在空气中燃烧的化学方程式________________。
下列铁制品的防锈方法不合理的是
| A.公交车扶手—涂防锈油 | B.水龙头—镀防护金属 |
| C.汽车外壳—烧漆 | D.脸盆—烧涂搪瓷 |
某化学小组对铁的冶炼、铁的锈蚀与防护进行以下实验探究.
(1)该小组设计如图1研究铁的冶炼.
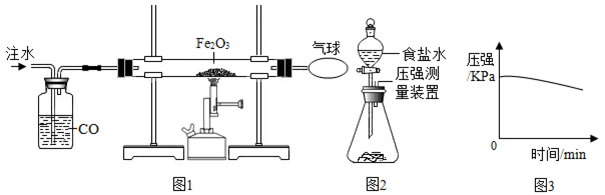
①实验时,应先注水片刻后再加热的目的是 .
②硬质玻璃管中发生反应的化学方程式是 .
(2)该小组又设计如图2装置,将反应所得铁粉置于锥形瓶底部,塞紧瓶塞,滴加适量食盐水,开始 测量容器内压强的变化.压强与时间变化关系如图3所示:
①实验中食盐的作用是 .
②锥形瓶内压强下降的原因是 .
③生产、生活中铁制品的常见防锈方法有 (举一例).
某化学兴趣小组进行铁生锈的实验探究活动。

[探究一]铁生锈的条件
(1)该兴趣小组将洁净无锈的铁钉分别置于上图所示装置中,经过一段时间观察,(填装置序号)装置中出现了明显的锈迹。
他们的结论:铁生锈是因为铁与空气中的等发生了化学反应。
(2)甲同学提出了疑问:空气中的氮气、二氧化碳没有参与铁的生锈过程吗?请设计实验为甲同学释疑。,观察并记录现象即可证明。
[探究二]影响铁生锈速率快慢的因素
乙同学说:妈妈常说菜刀沾有盐水生锈更快。这种说法对吗?同学广泛查阅资料。
资料一:导电性强的溶液都可加速铁的生锈。
资料二:海上航行的轮船在与海水接触的部分镶嵌一锌块,能有效降低钢材被腐蚀的速率。
(3)将上述
装置中的蒸馏水改为下列液体中的,可使铁生锈的速率加快。
| A. |
硫酸钠溶液 |
B. |
无水乙醇 |
C. |
蔗糖溶液 |
(4)一些铁制品表面覆盖了某些涂层。不同的涂层被破坏后,铁生锈的速率不同。你认为下列涂层破坏后,铁生锈的速率较快。
| A. |
镀锌铁 |
B. |
镀锡铁 |
(5)一些建筑的大门刷上了一层银白色的金属,你认为该金属可能是。
| A. |
银粉 |
B. |
铜粉 |
C. |
镁粉 |
[交流与思考]
(6)写出一种防止铁生锈的方法。
钢铁是重要的金属材料,在工农业生产和生活中应用非常广泛。
I.铁的冶炼
工业炼铁的原理是高温下用CO作还原剂,将铁从氧化物中还原出来。请回答下列问题:
(1)高炉炼铁中,焦炭的作用除了可以生成一氧化碳外,还能 ;
(2)某钢铁厂每天消耗5000t含氧化铁80%的赤铁矿石,该厂理论上可日产含铁98%的生铁的质量是多少?
II.实验探究炼铁原理某化学兴趣小组在实验室中模拟工业炼铁的原理,并探究CO与Fe2O3反应后的产物。通过查阅资料知道:①草酸(H2C2O4)固体与浓硫酸混合加热会产生一氧化碳,反应方程式为:H2C2O4 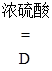 CO↑+ CO2↑+ H2O。
CO↑+ CO2↑+ H2O。
②NaOH溶液可以吸收二氧化碳,反应方程式为:2NaOH+CO2=Na2CO3+H2O
③常温下,Ca(OH)2微溶于水;于是他设计了下图的实验装置,结合装置回答下列问题:
(1)图A是用固体草酸和浓硫酸制取CO的反应装置,你认为应选择下图中的 (填装置编号);
(2)图中装置C、D的作用分别是 、 ;
(3)为了证明产物中有二氧化碳,装置F中的试剂应该是少量的澄清石灰水,该反应的化学方程式为 ;
(4)该装置设计有一个明显缺陷,你认为是 。
(5)实验时准确称取一定质量纯净的Fe2O3固体按上图进行实验,当E中固体全部变黑后,继续通入CO直到玻璃管冷却。将得到黑色的固体加入到足量的稀盐酸,发现固体全部溶解,但无气泡产生。
查阅资料:a.铁的氧化物在足量的稀盐酸中均能全部溶解。
b.Fe2O3与CO反应的固体生成物可能情况如下:
根据“无气泡”猜想,黑色粉末可能是:①Fe3O4;② ③ 。
(6)定量分析 用电子天平称量得部分数据如下:
| |
玻璃管质 |
玻璃管及其中固体的质量 |
装置F及其中物质的总质量 |
| 反应前 |
28.20 g |
33.00 g |
300.0 g |
| 反应后 |
32.84 g |
300.4 g |
根据上述数据,请选择有效的数据,推断出反应后黑色固体的成分。(写出计算过程)
试题篮
()