在一密闭容器中,有甲、乙、丙、丁四种物质,在一定的条件下,充分反应,测得反应前后各物质质量如下表:
| 物质 |
甲 |
乙 |
丙 |
丁 |
| 反应前质量(g) |
4 |
1 |
42 |
10 |
| 反应后质量(g) |
待测 |
20 |
6 |
31 |
完全反应后,甲的“待测”值应为
A.10 B.8 C.4 D. 0
下列由物质性质或实验事实所进行的判断正确的是
| A.水结成冰前后质量保持不变,说明该变化符合质量守恒定律 |
| B.焊锡的熔点比锡低、硬铝的熔点比铝低,说明合金的熔点一般比组成金属低 |
| C.实验室制取气体前都要检查装置的气密性,说明有气体生成的实验均要检查装置气密性 |
| D.镁粉可以在空气中燃烧、而铁丝只能在氧气中燃烧,说明反应物间的接触面积决定了化学反应能否发生 |
下面是一些关于铁的实验研究,试按要求填空。
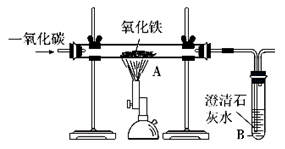
(1)模拟工业炼铁(装置图如右图):在硬质玻璃管内加入少量氧化铁粉末,先通入一氧化碳,排出装置内空气后,再用酒精喷灯加热A处药品。
① 硬质玻璃管内发生反应的化学方程式为: 。
② 试管B中发生反应的化学方程式为: 。
③ 该装置的主要缺点是 。
(2)铁锈蚀的探究
某化学兴趣小组进行家庭化学实验“探究铁锈蚀的原因”,设计如下图所示。他们预设的实验结果是仅有图Ⅲ中的铁钉生锈。但经过一周时间的观察,他们发现三支试管中铁钉都生锈了。
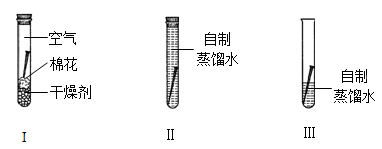
老师在听取了同学汇报后,做了如下实验帮助同学分析原因:取4份等量自来水样,经过不同的方法处理后,用数字传感器测定水样中的溶解氧,并进行如上图(Ⅰ、Ⅱ、Ⅲ)的实验。
水样溶解氧数据如下:
| 自来水 |
1号水样 |
2号水样 |
3号水样 |
4号水样 |
| 处理方法 |
不处理 |
煮沸 密封迅速冷却 |
煮沸 密封自然冷却 |
煮沸 敞口冷却 |
| 溶解氧(mg/L) |
5.37 |
0.52 |
0.66 |
3.44 |
[教师实验的现象记录(部分)]用2号水样进行的如图Ⅱ的实验中:一天后,铁钉有轻微生锈,从第二天到第七天,铁锈不再增加。
参考所给数据分析:①学生实验中:图Ⅰ中铁钉生锈的原因可能是 ;
图Ⅱ中铁钉生锈的原因可能是 。
②教师实验所记录的实验现象的原因可能是 。
完成下列变化的化学方程式,并按要求填空。
(1)常温下,铝和氧气发生反应: ;在铝表面生成了一层 。
(2)铁丝插入盛有硫酸铜溶液的试管中: ;溶液的颜色变化为: 。
(3)甲烷(CH4)在空气中完全燃烧: ;该反应将化学能转化为 。
(4)加热铜绿: ;其基本反应类型是: 。
(5)实验室用高锰酸钾制取氧气: ;排水集气时看到 现象时说明氧气集满。
某一个危险品仓库的硝酸铵发生爆炸,造成很大的财物损失.硝酸铵在约200℃时发生如下反应:NH4NO3=X+2H2O,则X的化学式为( )
| A.NO | B.N2 | C.N02 | D.N20 |
某天然矿泉水中元素及物质含量如下表所示,请用相关化学用语回答下列问题。
(1)右表中的一种阴离子 ;

(2)标出偏硅酸中硅元素的化合价 ;
(3)产自溶洞中的水中含有微量的二氧化碳,保持二氧化碳化学性质的最小粒子是 ;
(4)在自来水厂净水方法中,说法正确的是( )
①通过沉淀、过滤、吸附除去水中难溶性杂质,就可得到纯净水
②常用的方法有:沉淀、吸附、过滤、蒸馏,其中净化程度最高的是蒸馏
③通过过滤的方法将不溶于水的固体杂质与水分离开
④用氯气给水杀菌是化学变化,用活性炭净化水是物理变化.
(5)自来水中含有少量Ca(HCO3)2等可溶性化合物,烧水时Ca(HCO3)2发生分解反应,生成难溶性的碳酸钙、水和二氧化碳,这就是壶中出现水垢的原因之一。请写出Ca(HCO3)2受热分解的化学方程式: ;
(6)有经验的鱼民在进行长途运输鲜鱼的过程中常常在水中加入少量的过氧化钙固体。已知过氧化氢的化学式可表示为H2O2,过氧化钾为K2O2,则过氧化钙的化学式为 ,若过氧化钾与水反应的方程式表示为2K2O2+2H2O=4KOH+O2↑,则过氧化钙与水的反应方程式为 ,请说出使用过氧化钙可以使鱼长期存活的理由: 。
如图是画家用碳墨绘画的我国明朝诗于谦《石灰吟》的国画,诗中写道:“千锤万凿出深山,烈火焚烧若等闲,粉身碎骨浑不怕,要留清白在人间”.试回答:

(1)文房四宝中的徽墨是松树枝不完全燃焼产生的炭黑,炭黑书写的字画能够保存多年而不变色,原因是 .若在生活中选用含碳元素的燃料,为确保其充分燃烧,可采取的方法为 ,请写出乙醇不完全燃焼生成二氧化碳、一氧化碳和水的化学方程式 、
(2)诗句中“千锤万凿出深山”所体现物质的变化是 变化;“烈火焚烧若等闲”所体现的化学反应是石灰石受热分解,反应的化学方程式为 ,该反应是反应 (填“吸热”或“放热”).
(3)“要留清白在人间”指的是氢氧化钙暴露在空气中所发生的化学反应,判断氢氧化钙已经变质的方法是 。
只用C、CO、CuO、CaCO3、稀盐酸五种物质,进行单一或两两反应,可写出生成物中有CO2 的化学方程式有
A.2个 B.3个 C.4个 D.5个
下表中所描述的变化与右图相符合的是

| |
化学变化 |
Y轴 |
a |
b |
| A |
等质量的高锰酸钾和水在不同条件下分解 |
氧气质量 |
高锰酸钾 |
水 |
| B |
等质量、等浓度的双氧水在不同条件下反应 |
氧气质量 |
加催化剂 |
加热 |
| C |
等质量的镁片和铁片分别与足量的稀硫酸反应 |
氢气质量 |
镁 |
铁 |
| D |
等质量的二氧化碳和生石灰分别与等量的水反应 |
温度 |
二氧化碳 |
生石灰 |
下列说法中,与化学变化中遵循的质量守恒定律不相符合的是
| A.水结冰后,质量保持不变 |
| B.铜粉在空气中加热后,质量增大 |
| C.蜡烛在空气中燃烧后,质量减小 |
| D.1.2 g碳与3.2 g氧气完全反应,生成4.4 g二氧化碳 |
下列食品、调味品的制作过程中,主要发生物理变化的是
| A.水果榨果汁 | B.黄豆酿酱油 | C.糯米酿甜酒 | D.鲜奶制酸奶 |
合成氨是人类科学技术上的一项重大突破,对社会发展与科技进步做出了巨大贡献。合成氨工艺的主要流程如下:
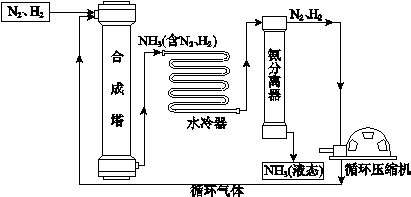
(1)合成塔中的反应在高温、高压、催化剂条件下进行,其化学方程式是 。
(2)生产过程中可循环使用的物质是 。
(3)根据表中的数据回答问题。
| 物质 |
H2 |
N2 |
O2 |
NH3 |
| 沸点/℃(1.01×105 Pa) |
–252 |
–195.8 |
–183 |
–33.35 |
在1.01×105 Pa时,欲将NH3与N2、H2分离,适宜的方法是 。
在“宏观”、“微观”、“符号”三者之间建立联系是化学学科特有的思维方式。
(1)①FeO名称:____ ;
②Mg2+中2表示的意义: ;
③2Hg表示的意义:____ 。
(2)写出实验室制取二氧化碳气体的化学方程式:____________________________。
(3)酒精检测仪中的反应原理:C2H5OH +4X +6H2SO4=2Cr2(SO4)3 +2CO2↑+9H2O,推测X的化学式为 。
(4)已知:甲+乙_丙+丁。
①若反应物分别为单质和化合物,写出一个符合条件的化学方程式.
②若反应的微观示意图如下,写出化学方程式:______________。

下列应用和相应的原理(用化学方程式表示)及基本反应类型均正确的是
A.拉瓦锡测定空气中氧气的含量 4P+5O2 P2O5化合反应 P2O5化合反应 |
B.比较铜和银的金属活动性 Cu + 2AgNO3 Cu(NO3)2 +2Ag置换反应 Cu(NO3)2 +2Ag置换反应 |
C.用硫酸除铁锈 Fe2O3 +2H2SO4 2FeSO4 +3H2O置换反应 2FeSO4 +3H2O置换反应 |
D.煅烧石灰石制生石灰 CaCO3 CaO + CO2↑分解反应 CaO + CO2↑分解反应 |
下图为汽车尾气净化装置中发生反应的微观示意图,有关叙述错误的是
| A.该反应是置换反应 | B.图中单质的化学式为N2 |
| C.反应后分子总数减少 | D.该装置可净化汽车尾气 |
试题篮
()