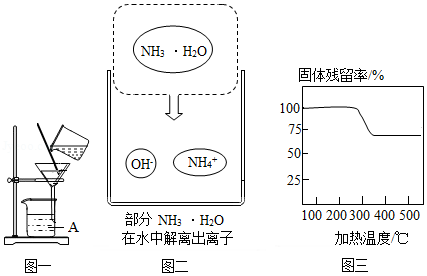
以镁矿石(主要成分MgCO3、SiO2)为原料生产MgO的工艺流程如图

注:SiO2难溶于水和常见的酸;“沉镁”过程中有Mg(OH)2生成。
(1)滤渣X的主要成分为 (填化学式)。
(2)实验室中用图一所示装置进行过滤。
①该装置中仪器A的名称为 。
②若过滤时滤液出现浑浊,可能的原因是 (填字母)。
a.滤纸已破损 b.漏斗中液面低于滤纸边缘 c.滤纸未紧贴漏斗内壁
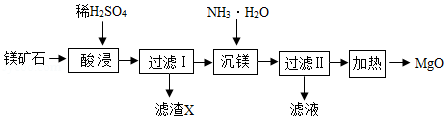
(3)“沉镁”时MgSO4与NH3•H2O发生反应。结合图二,写出该反应的化学方程式 。
(4)已知在不同温度下,充分加热等质量的Mg(OH)2,加热温度与固体残留率的关系如题图三所示。“加热”时温度至少要达到350℃,原因是 。
以镁矿石(主要成分MgCO3、SiO2)为原料生产MgO的工艺流程如图
注:SiO2难溶于水和常见的酸;“沉镁”过程中有Mg(OH)2生成。
(1)滤渣X的主要成分为 (填化学式)。
(2)实验室中用图一所示装置进行过滤。
①该装置中仪器A的名称为 。
②若过滤时滤液出现浑浊,可能的原因是 (填字母)。
a.滤纸已破损 b.漏斗中液面低于滤纸边缘 c.滤纸未紧贴漏斗内壁
(3)“沉镁”时MgSO4与NH3•H2O发生反应。结合图二,写出该反应的化学方程式 。
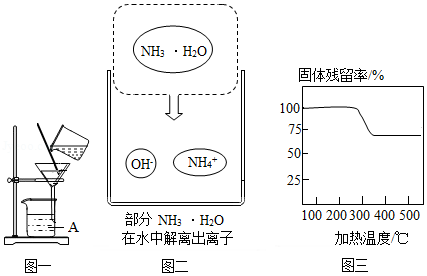
(4)已知在不同温度下,充分加热等质量的Mg(OH)2,加热温度与固体残留率的关系如题图三所示。“加热”时温度至少要达到350℃,原因是 。
胆矾(CuSO4•5H2O)在工农业生产中有广泛的用途。实验室利用废旧电池的铜帽(主要含铜和锌)为原料制备胆矾。实验流程如图所示:
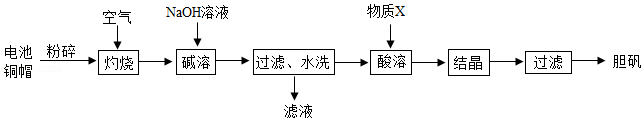
查阅资料:氧化锌能溶于氢氧化钠溶液。
(1)废旧电池铜帽的表面常有油污,可用洗洁精预先除去,洗洁精在除去油污的过程中起 作用。
(2)“碱溶”步骤中,为加快反应速率可采取多种措施,如搅拌、 等。
(3)“酸溶”时,发生反应的化学方程式是 。
(4)“灼烧”完全(已充分反应)的判断依据是 。
我国煤炭资源丰富,目前人们除了将煤作为燃料外,更是重要的化工原料。工业上以煤和空气为原料生产尿素[CO(NH2)2]的一种流程如图:
(1)从液态空气中分离出N2的过程属于 (填“物理”或“化学”)变化。
(2)在煤和水蒸气反应前需先将煤粉碎,这样做的目的是 。
(3)水煤气在铜催化下实现CO的转化:CO+H2O CO2+X,其中X的化学式为 。
(4)上述流程中合成尿素的同时还有水生成,该反应的化学方程式为 。
(5)实际生产中,N2和H2不可能全部化为NH3.上述流程中可以循环利用的物质有 。
(6)以CO2和H2为原料还可合成液体燃料乙醇(C2H6O),该过程可用化学方程式表示为:
2CO2+6H2 C2H6O+3H2O.已知:每克燃料完全燃烧数出的热量叫做热值
物质 |
煤 |
乙醇 |
热值/kJ•g﹣1 |
约33 |
30 |
若将含12g碳的煤为原料合成的乙醇完全燃烧,理论上最多可放出 kJ的热量,从而提高了煤的利用效率。
无水氯化钙的用途广泛。以石灰石矿粉(含有MgSO4、Fe2O3、SiO2等杂质)为原料,生产无水氯化钙的流程如图:
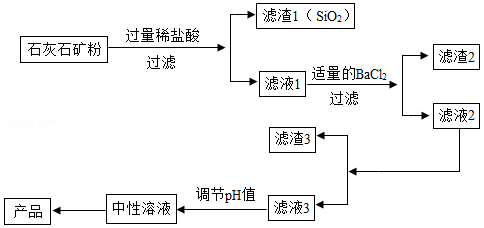
(1)写出过滤操作中用到的任意一种玻璃仪器的名称 ;
(2)写出滤液1中含有的所有金属阳离子的符号 ;
(3)滤渣3中的固体除有Ca(OH)2外,还有 (写化学式);
(4)对滤液3调节pH值时发生反应的化学方程式为 。
氯碱工业以粗盐(主要成分是NaCl,含少量泥沙、CaCl 2、MgCl 2)为原料,生产氯气和氢氧化钠,模拟流程如图: 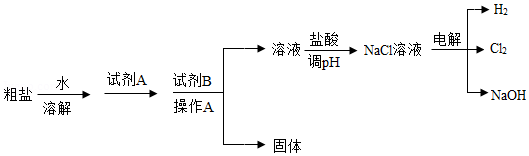
(1)试剂A与试剂B的组合为 (填序号)
①KOH ②NaOH ③K 2CO 3 ④Na 2CO 3
(2)操作A需使用玻璃棒,玻璃棒的作用是 。
(3)流程中Mg元素必须转化成 (填化学式)才能完全除去。
(4)写出电解NaCl溶液的化学方程式 。
(5)该工业副产品H 2目前还不能作为燃料被广泛应用,其理由 (答一条即可)。
海洋是人类宝贵的自然资源,海水“制盐”体现了人类利用化学科学征服和改造自然的智慧。通过晾晒海水,可以得到粗盐,粗盐中含有不溶性杂质(如泥沙等)和可溶性杂质(如MgCl2、CaC12等),工业上以粗盐为原料制取精盐,其生产流程如图所示
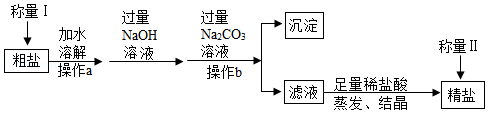
请回答下列问题:
(1)操作b中玻璃棒的作用是 。
(2)加入Na2CO3溶液除去的离子是 (填离子符号),加入NaOH溶液发生反应的化学方程式为 ;
(3)滤液中溶质的主要成分是 (填化学式),加入足量稀盐酸的目的是 。
(4)如果称量Ⅰ中称得粗盐的质量为3g,称量Ⅱ中称得精盐的质量为3.1g,则下列分析正确的是 (填字母)
A.精盐的产率为103.3%
B.蒸发操作中可能有水分没有蒸干
C.除杂过程中有NaCl生成
D.溶解操作中粗盐没有完全溶解
2020年奥运会奖牌制作原料来自于电子垃圾中提炼出来的金属。从废线路板中提炼贵重金属和制备硫酸铜晶体的一种工艺流程如图:

已知:在酸性环境中有过氧化氢存在时,铁和铜分别会转化为铁离子和铜离子。
(1)操作①的名称是 ;
(2)提炼出的贵重金属可制作奖牌,其成分是 ;
(3)调节pH的主要目的是除去滤液中 (填金属离子符号);
(4)写出粗铜中的铜与稀硫酸和过氧化氢的混合溶液发生反应的化学方程式: 。
分子筛(又称为沸石,主要成分为水和硅铝酸钠)可作为催化剂或吸附剂等,以高岭土[主要成分为Al2(Si2O5](OH)4].烧碱等为主要原料生产分子筛的工艺流程如图:

(1)步骤①所得烧渣中主要含有两种固体氧化物,分别为SiO2和 (写化学式)
(2)步骤②加入NaOH溶液前需将烧渣粉碎,其目的是 。
(3)步骤③发生的反应之一是Na2SiO3溶液和通入的CO2气体生成偏硅酸(H2SiO3)沉淀和碳酸氢钠,该反应的化学方程式为 。
(4)上述流程中可以循环利用的物质(水除外)是 。
碳酸亚铁(FeCO3)可用于制作补铁药物,以下是用硫铁矿烧渣(主要成分为Fe2O3、SiO2等)为原料制备碳酸亚铁的生产流程示意图:
【资料】40℃以上时,(NH4)2CO3易分解。

(1)操作Ⅰ的名称为 。
(2)写出向固体A中加入稀硫酸后发生的化学方程式: 。
(3)加入(NH4)2CO3后,该反应必须控制的条件是 。
(4)从溶液C中可回收一种化工产品,请写出它的一种用途 。
某兴趣小组利用实验室制CO2的废液得到CaCO3和NaCl晶体,过程如下:

(1)试剂X可用 (选填序号)。
a.NaOH溶液 b.Na2CO3溶液 c.K2CO3溶液
(2)操作I需要用到的玻璃仪器有 、 和烧杯。
(3)操作Ⅱ的名称为 。
海洋是人类巨大的资源宝库,如图为从海水中提取金属镁的简易流程图。

(1)海洋中含量最多的物质是 ;
(2)实验室中进行操作Ⅰ时,玻璃棒的作用是 ;
(3)生石灰转化为石灰乳的过程是 反应(选填“吸热”或“放热”);
(4)上述流程中未涉及到的基本反应类型是 反应。
工业上,常采用“盐硝联产工艺”生产高纯度食盐,还可以制得硫酸钠。卤水中主要含有NaCl,还含有少量Na2SO4、CaSO4、MgSO4、CaCl2、MgCl2、FeCl3,用火碱和烟道气中的CO2为原料净化卤水,符合低碳经济发展要求。分析流程,回答问题:
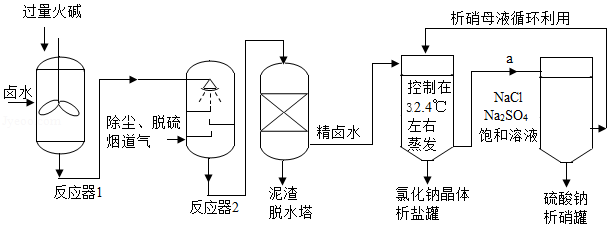
(1)反应器1中主要除去的离子是 (填符号)。
(2)烟道气通入反应器2前要脱硫,是为了除去有害气体 (填化学式)。反应器2中生成沉淀的化学方程式 (写一个)。
(3)下表为NaCl和Na2SO4在不同温度时的溶解度:
温度/℃ |
0 |
10 |
20 |
30 |
32.4 |
40 |
50 |
60 |
70 |
80 |
90 |
100 |
溶解度/g |
35.7 |
35.8 |
36.0 |
36.3 |
36.4 |
36.6 |
37.0 |
37.3 |
37.8 |
38.4 |
39.0 |
39.8 |
4.9 |
9.1 |
19.5 |
40.8 |
52.0 |
48.8 |
46.2 |
45.3 |
44.3 |
43.7 |
42.7 |
42.5 |
从析盐罐中排出的溶液a,在温度不变的条件下,每10g水中含有NaCl约 g.为提高Na2SO4纯度,析硝罐中析出Na2SO4,需采用 (填“升温”或“降温”)结晶方法。
化学是认识、改造和应用物质的科学。从海水中提取镁、制“碱”,都体现了人类改造物质的智慧。结合下列流程图(其中部分操作和条件已略去),请回答相关问题:

(1)提纯物质常用转化的方法,就是将杂质转化为沉淀或气体而除去。 粗盐中含有氯化镁、硫酸钠、氯化钙等可溶性杂质,通过步骤Ⅰ,再利用过滤操作进行除杂。步骤Ⅰ加入下列三种溶液的先后顺序为 (填字母序号);
a.稍过量的Na2CO3溶液 b.稍过量的BaCl2溶液 c.稍过量的NaOH溶液
(2)母液中有MgCl2,却经历了步骤Ⅳ、Ⅴ的转化过程,其目的是 ;
(3)步骤Ⅱ中先向饱和食盐水中通入氨气,有利于二氧化碳的吸收,这样做的目的是 ,写出该反应的化学方程式 ;
(4)化学变化是改造物质的重要途径。上述流程图中没有涉及的基本反应类型是 。
试题篮
()