如图是四种粒子的结构示意图。下列说法错误的是( )

A.①②③④均达到稳定结构B.④表示Cl﹣
C.①②③属于同种元素D.①③可形成化合物Na2O
元素组成万物
2019年是“国际化学元素周期表年”,元素周期表迎来了它150周岁的生日。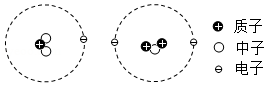
(1)人们很早就意识到物质都是由几种亘古不变的基本成分﹣﹣“元素”组成的。
①古人曾认为水是组成物质的元素之一,在你学过的知识中能说明“水不是元素”的实验事实是 。
②如图是两个微粒的结构模型示意图,这两个微粒是否属于同种元素?你的观点及依据是 。
(2)1869年,俄国化学家门捷列夫在前人研究的基础上制作出第一张元素周期表,为预测新元素的结构和性质提供了线索,如图是元素周期表的部分内容和铝原子结构示意图,据图回答下列问题:
①下列说法正确的有 。
A.表中元素都是金属元素
B.铝的相对原子质量是26.98g
C.铝原子在化学反应中易失去电子变成Al3+
D.锗原子中质子数等于中子数
E.铝原子最外层3个电子能量最高
②图中空白处元素原子的质子数为 ,小明根据元素周期表预测该元素组成的单质(用R表示)与铝有相似的化学性质,他的依据应是 。R在空气中被氧化的化学方程式是 。若要比较R与Al的活动性强弱,实验方案为 。

(3)如图是二氧化碳循环的部分过程。
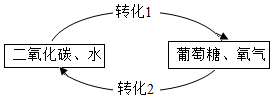
该循环中,生成物葡萄糖中的元素来源于(填化学符号) 。
德谟克利特曾说过“无中不能生有,任何存在的东西也不会消灭”。在该循环过程中,“不会消灭”的微粒有 (填符号)。无论经过多少化学变化,这些微粒永远“不会消灭”的原因是 。
(4)人体是一个巨大的元素仓库,青少年需要适当补钙。某钙片的主要成分是碳酸钙,这种钙片在胃中消化时发生反应的化学方程式是 。咀嚼有利于钙片消化,其原理是增大了反应物的接触面积,除此之外,影响化学反应速率的因素还有 。
我国拥有自主知识产权的硅衬底高光效氮化镓发光二极管(简称LED)技术,已广泛用于照明、显像等多个领域。氮和镓的原子结构示意图及镓在元素周期表中的信息如图所示,下列说法正确的是( )
A.镓元素位于第三周期,属于金属元素
B.镓原子核内有31个中子
C.镓的相对原子质量是69.72g
D.氮化镓的化学式为GaN
联合国将 2019 年列为"国际化学元素周期表年"。锶、镁元素在元素周期表中的部分信息及原子结构示意图如下,请回答下列问题。
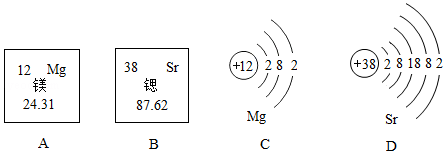
(1)镁原子的核电荷数为 ,镁元素的相对原子质量为 。
(2)锶原子在化学反应中容易 (选填"得"或"失")电子,锶的氧化物的化学式为 。
(3)元素的性质与其原子结构有密切关系。原子的最外层电子数相同时,电子层数越多,最外层电子离核越远,原子核对最外层电子的吸引力越小。由此推测,锶的金属活动性比镁的金属活动性 (选填"强"或"弱")。
如图是A、B元素的离子结构示意图。请回答:
(1)其中属于阴离子的是(填离子符号) ,该元素原子的核外电子数为 。
(2)A元素与地壳中含量最多的非金属元素组成化合物的化学式为 。

如图是氯原子结构示意图,下列有关叙述中,错误的是( )

A.氯原子易形成阳离子
B.氯元素属于非金属元素
C.氯原子核外有3个电子层
D.氯原子核内有17个质子
硒元素具有抗衰老、抑制癌细胞生长的功能,其原子结构示意图及在元素周期表中的信息如图,下列说法错误的是( )

A.硒原子核内有34个质子
B.硒元素的相对原子质量是78.96g
C.硒元素位于元素周期表中第四周期
D.硒元素在某些化合物中可显﹣2价
为庆祝元素周期表诞生150周年,联合国将2019年定为国际化学元素周期表年,请根据下表(元素周期表的部分内容)完成下题:
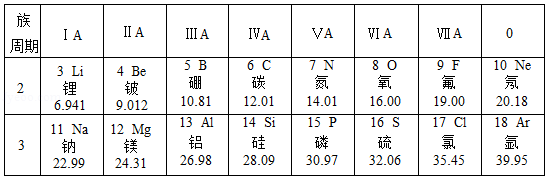
Ⅰ.(1)请根据上表写出关于氩元素的一条信息: 。
(2)镁与铝两种元素的最本质区别在于 ;由溴元素的原子结构示意图(如图 所示)可知;溴元素与上表中的 元素化学性质相似。
所示)可知;溴元素与上表中的 元素化学性质相似。
(3)第11号元素钠在化学反应中易 (填“得到”或“失去”)电子。则钠元素和硫元素形成的化合物的化学式为 。
(4)电池是高端电动汽车的主要动力源,其正极材料为LiCoO2,其中Co元素的化合价为 。
Ⅱ.从化学视角看人体,人体就是一张元素周期表。
(1)“关爱生命,拥抱健康”是人类永恒的主题,下列说法不科学的是 。
A.只要患甲状腺肿大,就必须补充适量的碘
B.适当晒太阳和增加维生素D的摄入,做到科学补钙
C.人是大自然的一部分,人体中所含元素全部来自大自然
D.低血糖病症发作时,喝葡萄糖水要比吃馒头见效快
(2)请根据生活常识结合已有知识分析:胃酸的成份是盐酸而不是硫酸的原因 。
我们通过学习知道:钠原子结构示意图 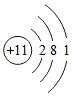 ,钠原子在化学反应中易 电子,成为 (填名称)。
,钠原子在化学反应中易 电子,成为 (填名称)。
(1)"在金属活动顺序里,位于前面的金属能把位于后面的金属从其盐溶液里置换出来",金属钠排在铜的前面。有的同学据此推测:钠能从蓝色硫酸铜溶液中把铜置换出来。教师按照下列图示顺序进行演示实验,并记录实验现象:

①由以上实验现象得出结论:因为反应中没有 色的物质生成,所以金属钠 (填:"能"或"不能")把铜从硫酸铜溶液中置换出来。
②对实验涉及的物质进行分析:硫酸铜溶液中溶剂为水,溶质为 (填化学式)。钠与硫酸铜溶液反应后培养皿中所含元素有:Na、Cu、H、O、 (填元素符号)五种元素。
查阅资料得知:"蓝色絮状难溶物"是一种学过的碱,该物质的名称是 。
(2)有的同学又产生新的疑问:钠能否与水发生反应?生成物是什么?
教师为解答学生的疑惑,又设计并进行如下实验,同时记录有关现象:

请结合如图所示信息,回答下列问题:
①用手触摸图3中烧杯外壁,感觉烫手,说明钠与水发生的是 (填:"吸热"或"放热")反应。
②从"图3"中可以断定:液体中出现红色说明反应后液体显 性,结合液体中所含元素,继而推断有 (填化学式)生成。另外,钠与水反应还生成一种可燃性气体单质。请写出钠与水反应的化学方程式: 。
如图是氧元素、钠元素在元素周期表中的相关信息及有关粒子的结构示意图,下列说法错误的是( )
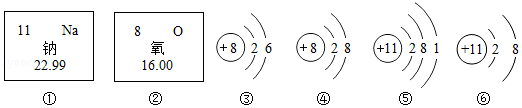
A.氧元素的原子序数为8
B.Na+的结构示意图是⑥
C.氧元素与钠元素的本质区别是最外层电子数不同
D.①②两种元素可组成化学式为Na2O的化合物
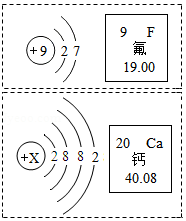
氟元素、钙元素对人体的主要作用是帮助构造骨骼和牙齿。如图是氟元素和钙元素的原子结构示意图,以及这两种元素摘自元素周期表的图示。其中x= ,钙的离子符号为 ,氟元素与钙元素形成化合物的化学式为 。葡萄糖酸钙【化学式Ca(C 6H 11O 7) 2】是一种促进骨骼生长的营养物质,葡萄糖酸钙由 种元素组成。
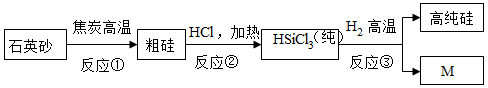
2018年4月16日,美国商务部宣布,禁止美国公司向中兴公司销售电子技术和通讯元件。其中一个聚焦点就是芯片技术,生产芯片的半导体材料有硅、锗、砷化镓等,应用比较广泛的是硅,硅可由石英砂(主要成分是二氧化硅)制得,其生产流程如图所示:
(1)上述三种半导体材料中属于金属材料的是 ,硅和锗的组成元素在周期表中的位置如图所示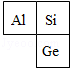 ,则两种元素属于同一 (填“周期”或“族”)
,则两种元素属于同一 (填“周期”或“族”)
(2)硅原子结构示意图为 ,则x为 ,”14”表示 。
,则x为 ,”14”表示 。
(3)根据上述流程图推断,反应①中化合价发生变化的元素有 ;反应③中M的化学式为 。
关于下列五种粒子结构示意图的说法中正确的是( )
A.①④属于不同种元素
B.②⑤属于金属元素
C.④⑤均具有稳定结构
D.①③两种粒子可以形成化合物MgCl2
阅读下面材料,回答问题。
人类赖以生存的环境由自然环境和社会环境组成。自然环境由生物圈、岩石圈、大气圈、水圈组成(如图1所示),四个圈层经过漫长演化,既相对稳定、动态平衡,又相互作用、不断变化,各圈层之间的物质和能量不停循环,这些循环既跟物质的组成、结构和性质有关,也受人类活动的影响,并通过复杂的物理变化和化学变化实现。
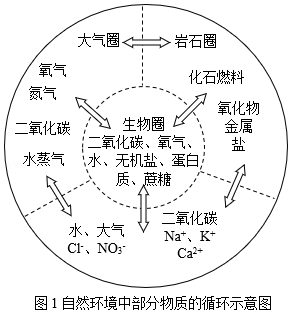
(一)内涵决定身份﹣﹣物质的组成与分类
(l)用化学符号填空:
岩石圈中含量最高的金属元素是 。大气圈中含量最高的物质是 。水圈中含量最高的元素是 。土壤中能促进农作物根系发达的元素是 。
(2)按要求填表:
物质所属圈层 |
物质名称 |
物质的化学式 |
用符号表示构成物质的微粒 |
物质类别 |
生物圈 |
蔗糖 |
|||
大气圈 |
氩气 |
|||
水圈 |
氢氧化钙 |
|||
岩石圈 |
Na+、SiO32﹣ |
(二)甲烷﹣﹣小分子,大作为
在图1的四大圈层中,有下列6种物质:①甲烷;②水;③二氧化碳;④一氧化碳;⑤氢气;⑥氧气。构成这些物质的分子虽然简单,但这些物质有的是人类赖以生存的基本物质,有的是物质循环关键物质,有的是人类社会生产活动必需的物质。请回答:
(1)在这6种物质中,元素种类共有 种,人类的生命活动不可缺少的物质有 (填化学式,下同),植物生长必需的物质有 ,元素种类完全相同的物质是 。
(2)甲烷是最重要的基础有机物之一,不仅可做燃料,还能发生如下反应:
①在隔绝空气和1000℃条件下,甲烷分解产生炭黑和氢气;
②在隔绝空气和1500℃条件下,甲烷分解产生乙炔和氢气;
③在1400℃条件下,适当比例的甲烷和氧气反应生成氢气和一氧化碳;
④在800℃和催化剂条件下,适当比例的甲烷和二氧化碳反应生成氢气和一氧化碳。
试写出上述②~④三个反应的化学方程式:
② ;
③ ;
④ ;
(3)在反应①~④中,属于置换反应的有 。
在反应①和②中,反应物相同,而生成物不同,从微观的角度看,是因为反应条件不同导致 。
③和④两个反应的反应物不同,但生成物相同,从物质组成的角度看,其原因是 。
在实际生产中,反应③需要按比例控制氧气不能超量,从物质性质的角度看,原因是 。
(三)柔之力﹣﹣神奇的水溶液
水在生活、生产和科学实验中应用广泛。岩石圈约有四分之三被水覆盖,其中的某些物质被水溶解,其随水的天然循环在水圈中富集,富集后的物质可能再次沉积到岩石圈。
图2是氯化钠和碳酸钠的溶解度曲线。据图回答下列问题:
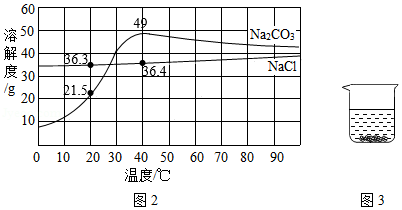
(1)青海湖区的人们有一种经验,冬天捞“碱”、夏天晒盐,这里的“碱”指纯碱,盐指氯化钠,他们所依据的原理是 。
(2)纯碱是一种重要的化工原料,但仅用物理方法从盐湖中“捞碱”远远不能满足需求,工业上主要利用从水圈中获得的食盐来制备纯碱,其反应的化学方程式是 、 。
(3)为确定某白色周体是碳酸钠还是氯化钠,在20℃时,取2.5g样品加入盛有10g水的烧杯中,充分搅拌后现象如图3所示,则固体粉末是 。若将该溶液升温到40℃时,则所得溶液溶质质量分数为 。
(四)金属﹣﹣工业的脊梁
金属及合金广泛应用于生活、生产和航天军工。
资料:水圈和岩石圈中含有丰富的镁元素。工业生产中,可用菱镁矿做原科制'备金属镁,流程如图4所示:

请回答下列问题:
(l)已知①和②属于分解反应,化学方程式分别为 和 。
(2)通过化学反应,以岩石圈的矿石为原料还可以制备很多其他金属,请举一例说明(用化学方程式表示其制备原理) 。
(3)图5是镁原子结构示意图,镁化学性质活泼,原因是 。四大圈层中含有下列物质:①硫酸锌;②氯化钠;③硫酸;④氢氧化钙;⑤氧气。其中能和铁反应的物质有(填序号) 。
(4)小梅同学将点燃的镁条伸入盛二氧化碳的集气瓶中,看到镁条剧烈燃烧,发出耀眼白光,瓶壁上有黑色物质生成,她认为这种黑色物质是碳单质。在上述过程中,小梅运用的科学方法有 。
试题篮
()