某化学兴趣小组为测定某有机物(含C、H、O三种元素)中各元素的质量比,用如图实验装置(部分夹持装置略去)进行探究。
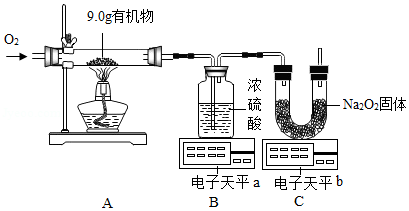
提示:装置C中发生的反应为2Na2O2+2CO2=2Na2CO3+O2
实验数据:
读数 |
反应前质量/g |
反应后质量/g |
电子天平a |
217.0 |
222.4 |
电子天平b |
150.0 |
158.4 |
请计算该有机物中各元素的质量比(写出计算过程)。
碳酸氢铵(化学式NH 4HCO 3)是农业生产中常用的铵态氮肥。
(1)①碳酸氢铵中氮、氢、碳、氧四种元素的最简质量比为 ;
② g碳酸氢铵中含4.8g氧元素。
(2)将15.8g碳酸氢铵加入到盛有100g稀盐酸的烧杯中,恰好完全反应。求反应后所得溶液的溶质质量分数。(写出计算步骤)
碳酸氢铵(化学式NH 4HCO 3)是农业生产中常用的铵态氮肥。
(1)①碳酸氢铵中氮、氢、碳、氧四种元素的最简质量比为 ;
② g碳酸氢铵中含4.8g氧元素。
(2)将15.8g碳酸氢铵加入到盛有100g稀盐酸的烧杯中,恰好完全反应。求反应后所得溶液的溶质质量分数。(写出计算步骤)
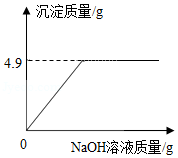
将氯化钠和氯化铜的固体混合物20g完全溶于100g水中,再向所得的溶液中加入溶质质量分数为10%的NaOH溶液。有关的变化如图所示。(反应的化学方程式为:CuCl 2+2NaOH═Cu(OH) 2↓+2NaCl)请计算:
(1)NaOH中氧元素和氢元素的质量比为 。
(2)求恰好完全反应时,所用NaOH溶液的质量。(写出计算过程)
(3)求恰好完全反应时溶液中溶质的质量分数。(写出计算过程,结果精确到0.1%)
食用小苏打含有 NaHCO 3外还含有少量NaCl.为了测定某食用小苏打中NaHCO 3的质量分数,某同学做了如下实验:称取一定量该样品于烧杯中,加水使其完全溶解,得到104.4g溶液,再向其中滴加100g稀盐酸,恰好完全反应时得到200g溶质质量分数3.1%的不饱和溶液。(反应的化学方程式为:NaHCO 3+HCl═NaCl+H 2O+CO 2↑)请计算:
(1)NaHCO 3中碳、氧元素的质量比为 ,
(2)生成CO 2的质量为 g,
(3)该食用小苏打中 NaHCO 3的质量分数(写出计算过程)。
取MgCl 2和NaCl的固体混合物10g做如下实验.请根据图中实验及数据进行计算.

(1)MgCl 2中镁元素和氯元素的质量比为 .
(2)计算溶液B中NaCl的质量分数(写出计算过程).
(3)要配制与溶液B相同质量分数的NaCl溶液200g,需要质量分数为24.4%的NaCl溶液的质量是多少?(写出计算过程)
将100g氯化钾样品(含有碳酸钾杂质)加入到50g盐酸中,样品完全反应,产生的气体全部逸出,并测得反应后的溶液总质量为145.6g。请计算:
(1)K 2CO 3中K、C、O元素的质量比为 。
(2)产生气体的质量为 g;
(3)样品中氯化钾的质量分数。(写出计算过程,最后结果精确到0.1%)
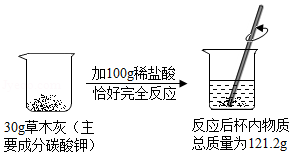
草木灰是农家肥料,其主要成分是碳酸钾,某化学兴趣小组进行如图实验,以下是他们的实验过程及数据(假设杂质不与稀盐酸反应,生成的气体全部逸出)。请你回答下列问题:
(1)碳酸钾中钾元素、碳元素、氧元素的质量比为 ;
(2)反应后生成的气体质量为 g;
(3)稀盐酸中溶质质量分数是多少?
化学小组同学取某黄铜(铜和锌的合金)样品进行如下实验,他们取该黄铜样品碎屑50g,把200g稀硫酸分4次加入到该样品中,测得数据记录如下表:
(1) 当加入稀硫酸的质量为 g时,反应恰好完成。
(2) 计算生成氢气的总质量(写出计算过程)。
据统计,全世界每年人类活动排放到大气中的二氧化硫超过一亿五千万吨.其中三分之二来自煤炭的燃烧.某煤厂向原煤中加入适量生石灰制成“环保煤”,以减少二氧化硫的排放.削弱二氧化硫对大气的污染。燃烧时吸收二氧化硫的化学方程式是2CaO+2SO2+O2高温 2CaSO4.该厂现有含硫3.2%的原煤1000t,问:
(1)这些原煤中含有硫元素多少吨?
(2)如果这些原煤不经“加工处理”直接燃烧,可生成多少二氧化硫?
(3)如果将这些原煤全部制成“环保煤”,理论上需要含杂质10%的生石灰多少吨?
试题篮
()