某公司生产出的纯碱产品中经检测只含有氯化钠杂质。为测定产品中碳酸钠的质量分数,20℃时,称取该产品样品26.5g,加入到盛有一定质量稀盐酸的烧杯中,碳酸钠与稀盐酸恰好完全反应,气体完全逸出,得到不饱和NaCl溶液。反应过程用精密仪器测得烧杯内混合物的质量(m)与反应时间(t)关系如下图所示。
求:(1)生成CO2的质量。
(2)反应后所得溶液中NaCl的质量分数。
“过碳酸钠”(2Na2CO3·3H2O2)俗称固体双氧水,它既有碳酸盐的性质,又有双氧水的不稳定性和氧化性,是很好的消毒剂和供氧剂,广泛应用于洗涤、印染和医药等领域。“过碳酸钠”的制备流程如下:
请回答下列问题:
(1)H2O2在催化或受热条件下易分解,说明化学变化的速度和 相关;
(2)在“过碳酸钠”中加入下列物质时,不会导致“过碳酸钠”变质的是 (填序号)。
| A.二氧化锰 |
B.稀盐酸 |
C.硫酸钠 |
D.石灰水 |
(3)“过碳酸钠”极易分解,得到碳酸钠、水和氧气,其反应方程式可表示为
2(2Na2CO3.3H2O2)==4Na2CO3+6H2O+3O2↑
请通过计算说明(必须有计算的过程):
①若“过碳酸钠”分解产生氧气12g,则同时产生碳酸钠的质量是多少?
②若将上述产生的碳酸钠全部配制成溶质质量分数为10.6%的溶液,共需水多少毫升?
在实验考试前夕,小东同学在实验操作练习中,发现用完全相同的两份稀盐酸和相同质量的大块大理石、小块大理石分别反应,大块的反应速率要慢,原因是什么? _________ .
小东又发现盛放氢氧化钠的试剂瓶口有白色粉末.为了确定白色粉末的成分,他进行了如下的探究:
(1)小毛猜测白色粉末中含有碳酸钠,请指出他的理由: _________ (用化学方程式表示).
(2)为了确定自己的猜测,小东设计了如下的方案:取少量白色粉末于试管中,加水溶解配成溶液,再用 _________ 检验,看到溶液中有 _________ 产生,从而使自己的猜想得到了证实.
(3)玻璃中的SiO2可以和氢氧化钠发生类似的CO2的反应,则SiO2与氢氧化钠反应生成盐的化学式为 _________ .
(4)为了进一步确定白色粉末中碳酸钠的质量分数,小东取了2g白色粉末,加入足量的水充分溶解,再滴加澄清石灰水,充分反应后,过滤,得到了白色沉淀1g.
①在过滤时,需用到玻璃棒,它的作用是 _________ ;
②请你帮小东计算:白色粉末中碳酸钠的质量分数.
今年我国“世界环境日”的主题是向污染宣战,某化工厂排放的废水中含有碳酸钠,提取50g废水样品于集气瓶中,逐滴加入10%的稀硫酸,至恰好完全反应时,收集到4.4g二氧化碳,请回答问题:
(1)判断滴加硫酸至恰好反应的依据是 。
(2)所消耗的稀硫酸质量是多少?
(3)最后所得溶液中溶质的质量分数是多少?(本小题最后结果取整数)
小明同学想测量某赤铁矿样品中氧化铁的纯度(假设其他成分不和酸反应,也不溶于水),进行如下实验:
称取10g赤铁矿样品,加入到烧杯中,再加入92.5g的稀硫酸,恰好完全反应。过滤得滤渣2.5g。试计算:
(1)赤铁矿样品中氧化铁的质量分数?
(2)上述反应所得滤液中溶质的质量分数?
用 溶液测定某种氮肥中 的质量分数(杂质溶于水,但不参加反应).
实验如下:称取该氮肥20
加水完全溶解,向该溶液中不断滴入
溶液,生成气体及沉淀质量与加入
溶液的质量关系如下所示:

| 实验次序 |
1 |
2 |
3 |
| 滴入 溶液的质量 | 20 |
40 |
60 |
| 生成气体的质量 | 0.85 |
2.55 |
试分析并计算:【已知:
】
(1)表格中
的值为
.
(2)实验所用氢氧化钡溶液中溶质的质量分数.
(3)该氮肥中 的质量分数.(计算结果精确至0.1 )
Na2CO3中往往会含有少量的NaCl,现在一烧杯中盛有20.4g的固体混合物,向其中逐渐滴加溶质质分数为10%的稀盐酸。放出气体的总质量与所滴入稀盐酸的质量关系曲线如下图所示,请根据题意回答问题: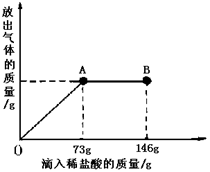
①当滴加稀盐酸至图中B点时,烧杯中溶液的pH 7(填>、=、<)。
②当滴加稀盐酸至图中A点时,烧杯中为不饱和溶液(常温),通过计算求出其中溶质的质量分数。(计算结果保留一位小数)
工业上通常用黄铁矿(主要成分FeS2)为原料生产硫酸,先将黄铁矿粉碎,然后按照以下流程制备硫酸:
(1)先将黄铁矿石粉碎的目的是 。
(2)写出稀释浓硫酸的具体操作步骤 。
(3)将10g98%的浓硫酸稀释成9.8%的稀硫酸,需要加水 g。
(4)取20g矿渣样品(含Fe2O3),向其中加入300g溶质质量分数为9.8%的稀硫酸(已知矿渣中的Fe2O3与稀硫酸恰好完全反应得到Fe2(SO4)3溶液),试通过化学方程式计算该矿渣样品中Fe2O3的质量分数。
小芳在实验室用石灰石和稀盐酸制取了二氧化碳,并对实验产生的废液进行溶质成分鉴定:取废液上层清液50克,滴加质量分数为26.5%的碳酸钠溶液,出现气泡,滴加至10克开始出现白色沉淀,继续滴加至沉淀不再产生,过滤,洗涤,干燥,称得沉淀质量为5克,并绘制了图象,如图:
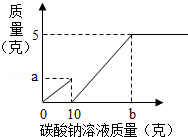
(1)图象中的a点数值
(2)废液中含有的溶质是 (写化学式)
(3)通过计算说明,图象横坐标中b点表示的溶液的质量是多少?
某同学测定一瓶标签残缺的硫酸镁溶液的溶质质量分数,取30g该溶液,向其中逐滴加入溶质质量分数为10%的氢氧化钠溶液.生成沉淀的质量与所用氢氧化钠溶液的质量关系如图所示.反应方程式为:MgSO4+2NaOH=Na2SO4+Mg(OH)2↓

(1)配制100g溶质质量分数为10%的NaOH溶液,需NaOH的质量为 g.
(2)计算MgSO4溶液中溶质的质量分数(列式计算).
黄铜是一种常见的合金材料,其作用成分为
、
,还含有少量不与酸反应的成分.现向一定质量的黄铜中加入体积为100mL,密度ρ=1.2g/mL的稀硫酸,产生
的质量和硫酸溶液体积的关系如图所示.充分反应后溶液中剩余固体的质量为27g。

(1)观察图象,黄铜与硫酸充分反应后,硫酸是否有剩余?(选填"是"或"否")
(2)黄铜中
的质量分数为多少?(请列式计算,结果精确到0.1%)
(3)若往反应后的溶液中滴加26%的
溶液至恰好不再产生沉淀时,共消耗
溶液400g,则原硫酸溶液的质量分数为多少?(请列式计算,结果精确到0.1%)
某碳酸钠样品含有少量的硫酸钠,取一定质量的该样品,完全溶解在水中配制成
溶液,将其全部加入到
一定质量分数的硫酸溶液中,恰好完全反应,生成的气体全部逸出后,所得溶液质量是
,将溶液蒸干,得到
硫酸钠。
计算:
(1)加入的硫酸溶液的溶质质量分数;
(2)原碳酸钠样品中碳酸钠的质量分数(计算结果精确到0.1%)。
酸和碱发生中和反应,它在日常生活和农业生产中有着广泛的应用。小强同学在做中和反应实验时,向盛有40克10%氢氧化钠溶液的烧杯中逐滴加入稀硫酸,滴加过程如图所示,求所加稀硫酸的溶质质量分数。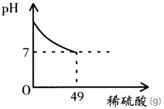
实验室制取二氧化碳后,将废液过滤,得到含有氯化钙和稀盐酸的混合液,20℃时,取混合液141.2g于烧杯中,向其中逐滴滴加溶质质量分数为10.6%的碳酸钠溶液,所产生的沉淀与所滴入碳酸钠溶液的质量关系如图所示。当滴入碳酸钠溶液至图中A点时,通过计算确定所得溶液是否为饱和溶液。(提示:20℃时,氯化钠溶解度为36克。)
试题篮
()