我国煤炭工业“十三五”科技发展指导意见中指出,煤炭工业应重点关注煤炭安全色开采、智能矿山建设、煤炭清洁利用和高效转化.
(1)煤是一种 (填“可再生”或“不可再生”)能源‘
(2)煤的气化是使煤变清洁能源的有效途径,煤气化的主要反应有:
①2C+O2=2CO ②C+H2O=CO+H2③CO+H2O=H2+CO2
反应①的基本反应类型是 反应.
反应②和反应③的相同点是 (填序号)
A、都是置换反应 B、水都发生了还原反应
C、生成物都是可燃性气体 D、反应后碳元素的化合价都升高.
工业用2Mg+TiCl4 2MgCl2+Ti来冶炼金属钛,该反应属于( )
A.化合反应B.分解反应C.置换反应D.复分解反应
废旧金属可以回收利用,用合金废料(含Fe、Cu和Al)制取FeSO4溶液和回收金属Cu.实验流程如图所示(部分生成物已略):

(1)合金属于 (填“纯净物”或“混合物”).
(2)生活中铝比铁更耐腐蚀的原因 (用化学反应方程式解释).
(3)步骤A化学反应方程式表示为:2Al+2NaOH+2R═2NaAlO2+3H2↑,依据质量守恒定律推出R的化学式为 .
(4)步骤B发生的化学方程式为 ;反应的基本类型为 .
2020年中国首次火星探测,利用火星车一次实现“环绕、着陆、巡视”三个目标,这是其他国家第一次实施火星探测从未有过的,面临的挑战也是前所未有的。(火星车模型如图)。
(1)硅片太阳能电池板在日光照射下或跟空气、水分接触时都不容易发生反应,则硅必备的化学性质 (选填“较活泼”或“稳定”)。
(2)火星车采用钛合金、铝合金、复合记忆纤维等材料制造,为保证火星车在火星上着陆并正常工作,钛、铝合金应具有密度小、硬度 、耐腐蚀等优良性能;铝的化学性质很活泼,但铝制品却很耐腐蚀的原因是 。
(3)火星大气中二氧化碳含量高,二氧化碳在一定条件下能发生反应生成一氧化碳和氧气,该反应的化学方程式 ,所属的基本反应类型为 ,生成的一氧化碳可解决火星探测器的燃料问题。

化学课上,小亮与老师一起演示了如图所示的实验:

请回答下列问题:
(1)甲中铜加热时因生成了氧化铜而变黑,该变化属于 (填"物理"或"化学")变化.
(2)小亮将变黑的铜丝a伸入试管内的稀硫酸中,再取出时,铜丝表面又变红了,试管内发生反应的化学方程式是 ,该反应属于基本反应类型中的 反应.
(3)老师将加热变黑的铜丝b趁热迅速伸入试管内的活性炭中,再取出时,铜丝表面也变红了,则试管内活性炭的质量一定会 (填"增大"或"减小").
2019年底,徐宿淮盐铁路将建成通车,淮安人可实现高铁出行。
(1)高铁在建造时使用了大量的新材料,下列属于金属材料的是 (填序号)。
A.生产高铁车头的玻璃钢
B.制造高铁车身的镁铝合金
C.制造轨道枕木的聚氨酯材料
D.建筑高铁路基的钢筋混凝土
(2)高铁刹车制动盘使用合金锻钢制作,主要利用该合金耐高温、 等特性。
(3)在高铁站的建设中,使用了大量的钢铁。工业上用赤铁矿(主要成分是氧化铁)和一氧化碳反应冶炼铁,该反应的化学方程式为 。
(4)高铁轨道焊接时,可用铝热反应:2Al+Fe2O3 2Fe+Al2O3,该反应的基本类型是 。

元素化合价发生改变的反应都是氧化还原反应.例如:2 +
+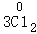
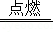 2
2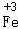
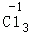 ,反应前后,Fe和Cl元素的化合价发生了改变,该反应是氧化还原反应.下列判断错误的是( )
,反应前后,Fe和Cl元素的化合价发生了改变,该反应是氧化还原反应.下列判断错误的是( )
A.分解反应都属于氧化还原反应
B.置换反应都属于氧化还原反应
C.复分解反应都不属于氧化还原反应
D.有单质参加的化合反应属于氧化还原反应
工业上可通过如下反应制取氧化钠:2NaNO3+10Na 6Na2O+N2↑,下列相关说法正确的是( )
A.反应物NaNO3属于氧化物
B.生成物N2的化学性质由氮气分子(N2)保持
C.该反应属于复分解反应
D.反应前后只有氮元素化合价发生变化
多角度认识物质及其变化,能帮助我们更全面了解物质世界。
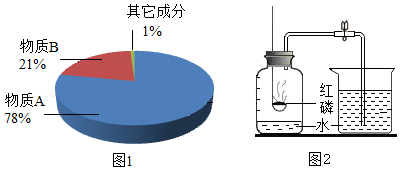
(1)图1为空气成分的示意图,物质B的化学式为 。
(2)利用红磷燃烧测定空气里物质B含量的实验装置如图2所示。
红磷燃烧反应的化学方程式为 ,该反应属于 (填基本反应类型)。
工业上处理黄铜渣(含Cu、Zn、CuO、ZnO和杂质)废料时,通常将其转化为硫酸锌并回收铜(黄铜渣中的杂质不溶于水,也不参与反应),其主要流程如图所示:
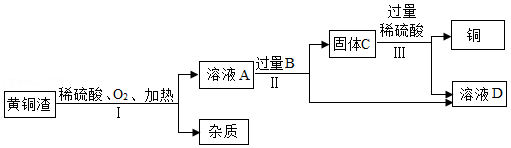
查阅资料:
2Cu+2H2SO4+O2 2CuSO4+2H2O
2CuSO4+2H2O
CuO+H2SO4 CuSO4+H2O
CuSO4+H2O
ZnO+H2SO4 ZnSO4+H2O
ZnSO4+H2O
(1)黄铜的熔点比铜的熔点 (填“高”或“低”);
(2)过程Ⅱ中分离操作的名称是 ,该操作需要用到的玻璃仪器有烧杯、玻璃棒和 (填仪器名称);
(3)过程Ⅲ中有气体产生,该反应的化学方程式是 ,该反应的基本类型为 反应。
为解决能源与环境问题,有学者提出如图1所示的含碳物质转化的技术路线。
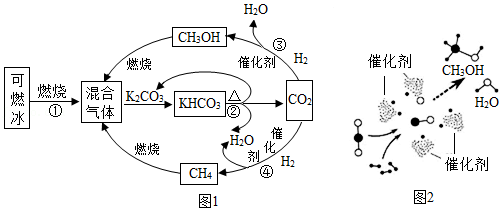
(1)“可燃冰”中甲烷完全燃烧的化学方程为 。
(2)反应②属于 (填基本类型)。
(3)反应④中,参加反应的CO2和生成的CH4的分子数目之比为 。
(4)我国学者开发促进反应③的一种新型催化剂,催化过程微观示意图如图2。该过程的中间产物 (填化学式)、氧和氢进一步作用生成甲醇(CH3OH)和水。
(5)该技术路线有利用于实现 (填标号)。
A.碳循环利用
B.减少碳排放
C.减少白色污染
化学就在我们身边,人类的生活离不开化学,回答下列问题。
(1)人们穿的衣服通常是由纤维织成的,下列属于天然纤维的是 。
A.蚕丝 B.涤纶 C.棉花 D.尼龙
(2)水是一种重要的自然资源,是生产、生活必不可少的物质。
①生活中可以通过 的方法,既可以杀灭水中的细菌,又可以降低水的硬度。
②下列各种水中属于纯净物的有 。
A.矿泉水 B.糖水 C.蒸馏水 D.自来水
(3)服用含氢氧化铝[Al(OH)3]的药物可以治疗胃酸过多症,反应的化学方程式为 ,该反应属于 (填基本反应类型)。
(4)吸烟除了影响自身的健康外,也会使周围的人“被动吸烟”,其原因是 (从微观角度解释)。
下列化学方程式及对应的基本反应类型都正确的是( )
A.CaHCO3═CaCO3↓+CO2↑+H2O 分解反应
B.Al(OH)3+3HCl═AlCl3+3H2O 复分解反应
C.P+O2 P2O5 化合反应
D.Fe2O3+3CO 3CO2+2Fe 置换反应
2020年,新型冠状病毒引起的疫情席卷全球,给人类的生命安全带来了巨大威胁。我们在日常生活和学习中,既要保持安全距离,又要注意消毒杀菌。过氧乙酸[CH3COOOH]是一种绿色高效的消毒剂,常用于校园环境消毒。过氧乙酸具有酸性、腐蚀性(尤其是对金属)、可燃性,遇热、遇碱易分解。用浓硫酸作催化剂,制备过氧乙酸的一种模拟流程如图(部分反应条件未标出):
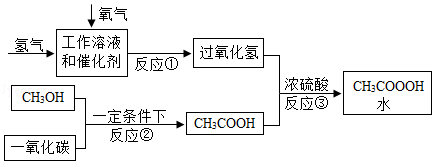
(1)认识过氧乙酸:它属于 (填“有机化合物”或“无机化合物”)。
(2)制备过氧乙酸:写出反应③的化学方程式 ;上述3个反应中属于化合反应的是 (填数字序号)。
(3)使用过氧乙酸:在校园消毒中,将lkg质量分数为20%的过氧乙酸溶液稀释至0.5%,需要加水 kg;下列关于过氧乙酸使用的说法正确的是 。
A.应低温、避开火源贮存
B.环境消毒,浓度越大越好
C.谨防溅到眼睛和皮肤上
D.最好不要用金属容器盛放
试题篮
()