五氧化二钒(V 2O 5)是一种工业催化剂,如图是制取V 2O 5的工艺流程。
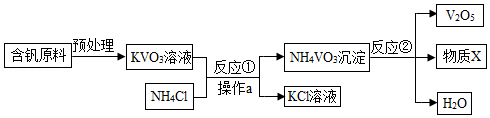
(1)写出反应①的化学方程式 。
(2)操作a的名称是 ,实验室进行该操作所需的玻璃仪器有烧杯、玻璃棒和 。
(3)反应②的反应类型是 ,物质X中一定含有的元素是 。
(4)写出副产物KCl的一种用途 。
氧气是一种重要的气体。小颖在试管中加入5mL 5%过氧化氢溶液,再依次进行实验:①插入带有火星的木条;②加入少量二氧化锰;③插入带有火星的木条。
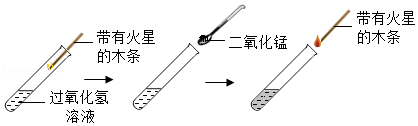
(1)当出现带有火星的木条 的现象时,说明试管中有大量氧气产生。
(2)实验③中产生氧气的化学方程式为 ,该反应属于 (填基本反应类型)。
CO2是造成温室效应的主要气体,而工业上却可用CO2来制备甲醛等物质,“碳捕捉技术”是指通过一定的方法,将工业生产中产生的CO2分离出来并加以利用﹣﹣如可利用NaOH溶液来“捕捉”CO2,其过程如图所示(部分条件及物质未标出)。

请根据有关信息回答问题:
(1)用NaOH溶液“捕捉”CO2的化学方程式是 ;
(2)“反应分离”环节中,分离物质所采用的基本操作是 ;
(3)此化学工艺流程中没有涉及到的基本反应类型是 。
中国是全球第一个实现在海域"可燃冰"试开采中获得连续稳定产气的国家。"可燃冰"是甲烷和水在低
温、高压条件下形成的水合物(CH 4•nH 2O)
(1)在常温常压下,"可燃冰"会发生反应:CH 4•nH 2O═CH 4+nH 2O,该反应属于 (填基本反应类型);
(2)甲烷可制成合成气(CO、H 2),再制成甲醇(CH 3OH),代替日益供应紧张的燃油,由合成气制甲醇的反应方程式为:CO+2H 2  CH 3OH,由甲烷制成合成气有两种方法:
CH 3OH,由甲烷制成合成气有两种方法:
①CH 4+H 2O  CO+3H 2
CO+3H 2
②2CH 4+O 2  2CO+4H 2
2CO+4H 2
从原料配比角度比较方法①和②,更适宜用于合成甲醇的方法是 (填序号)。
材料是人类社会物质文明进步的重要标志之一。回答下列问题:
(1)商代后母戊鼎代表着我国古代高超的金属制造水平,它主要是含 元素的合金。
(2)从陶瓷、玻璃、水泥到电子芯片,硅元素的用途非常广泛。工业制取高纯硅的一个反应的微观示意图如图:

①写出该图示表示的化学方程式 ,其基本反应类型是 。
②从如图图示看出:微观上,化学反应前后分子改变了,而 没有改变。
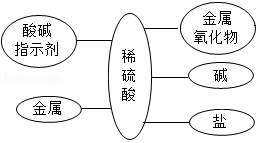
通过构建知识网络,可以帮助我们理解知识间的内在联系,如图是稀硫酸与不同类别物质之间反应的知识网络图。
(1)稀硫酸与锌反应的反应类型是 。
(2)可用稀硫酸与 、 等不同类的物质反应制取硫酸铜。
(3)向氯化钡溶液中加入一定量的硫酸溶液,反应后过滤,滤液中一定含有的溶质是 ____(填化学式,下同),可能存在的溶质是 。
能源的开发、利用与人类社会的可持续发展息息相关。
(1)白居易有诗句:"野火烧不尽,春风吹又生。"下列能源可以"春风吹又生"的是 (填序号)。
a、氢能 b、石油 c、风能 d、煤炭
(2)硅(Si)相对于氢气便于运输、贮存,是开发价值很高的燃料,晶体硅制得的太阳能电池,是将太阳能转化为 能。硅原子的结构示意图为 。硅元素的最高正化合价等于其原子的最外层电子数,硅元素最高正化合价对应氧化物的化学式为 。在高温条件下金属镁可以上述氧化物反应制得单质硅,写出该反应的化学方程式 。
(3)金属镁虽然性质活泼,但常温下,将镁粉与碘粉(紫黑色)均匀混合,几乎不反应。滴加几滴水后,发生剧烈反应,并伴有大量紫色蒸气(固体碘易升华),该反应过程中 热量(填"吸收"或"放出"),该反应的反应类型是 ,水的作用是 。
(1)“洁厕灵”、“漂白精”是家庭常用的两种清洁剂.“洁厕灵”的有效成分是盐酸,可清除污垢,但不能用于清洁大理石制品,理由是(写化学方程式) ;“漂白精”的有效成分是次氯酸钠(NaClO),能快速漂除衣服污渍.但“洁厕灵”与“漂白精”不能混用,二者若混合易产生一种有毒气体,化学方程式为NaClO+2HCl=NaCl+X+H2O,则X的化学式为
(2)波尔多液是一种农业上的杀菌剂,它由石灰乳与硫酸铜等配置而成.请用化学方程式解释不能用铁制容器来配制波尔多液的原因是 ,基本反应类型是 反应.
华为公司作为我国高科技的代表,一直致力于核心技术的开发。2019年,华为公司推出了5G商用芯片。制造芯片需要用到高纯硅,工业上利用二氧化硅制备高纯硅的工艺流程如图:
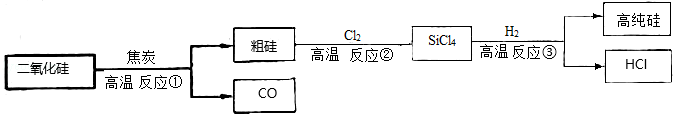
(1)写出CO的任意一点物理性质 。
(2)写出反应③的化学方程式 ,该反应属于 (填基本反应类型)反应。
(3)玻璃的主要成分是二氧化硅,二氧化硅属于 (填“金属氧化物”或“非金属氧化物”)。二氧化硅(SiO2)与氢氧化钠溶液反应类似于二氧化碳与氢氧化钠溶液的反应。请写出二氧化硅与氢氧化钠溶液反应的化学方程式 。
(4)整个制备过程必须在无水、无氧气的环境中进行,原因是 。
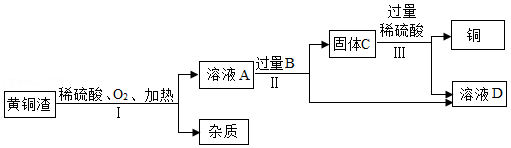
工业上处理黄铜渣(含Cu、Zn、CuO、ZnO和杂质)废料时,通常将其转化为硫酸锌并回收铜(黄铜渣中的杂质不溶于水,也不参与反应),其主要流程如图所示:
查阅资料:
2Cu+2H2SO4+O2 2CuSO4+2H2O
2CuSO4+2H2O
CuO+H2SO4 CuSO4+H2O
CuSO4+H2O
ZnO+H2SO4 ZnSO4+H2O
ZnSO4+H2O
(1)黄铜的熔点比铜的熔点 (填“高”或“低”);
(2)过程Ⅱ中分离操作的名称是 ,该操作需要用到的玻璃仪器有烧杯、玻璃棒和 (填仪器名称);
(3)过程Ⅲ中有气体产生,该反应的化学方程式是 ,该反应的基本类型为 反应。
质量守恒定律的发现对化学的发展做出了重要贡献。
(1)通过称量下列各组试剂在密闭容器内混合前后的总质量,能验证质量守恒定律的是 (填标号) 。
A.蔗糖和水 B.氯化钠溶液和硝酸钾溶液 C.铁和氯化铜溶液
(2)在氧气中点燃红磷的实验过程,固体质量变化如图1所示。
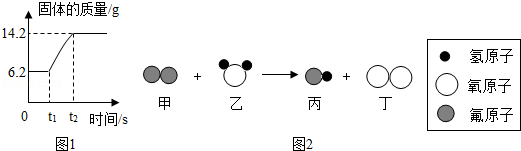
①从燃烧条件分析,固体质量在t1前没有发生变化的原因为 。
②该反应的化学方程式为 。
③参加反应的氧气质量为 g。
(3)某反应的微观示意图如图2所示:
①该反应所属的基本类型为 。
②参加反应的甲物质和生成的丙物质分子数目比为 。
海水资源丰富,工业以海水为原料提取镁的过程如图:

回答下列问题:
(1)操作①的名称是 。
(2)反应③的化学方程式为 。
(3)上述反应①②③未涉及的基本反应类型为 。
2020年,新型冠状病毒引起的疫情席卷全球,给人类的生命安全带来了巨大威胁。我们在日常生活和学习中,既要保持安全距离,又要注意消毒杀菌。过氧乙酸[CH3COOOH]是一种绿色高效的消毒剂,常用于校园环境消毒。过氧乙酸具有酸性、腐蚀性(尤其是对金属)、可燃性,遇热、遇碱易分解。用浓硫酸作催化剂,制备过氧乙酸的一种模拟流程如图(部分反应条件未标出):
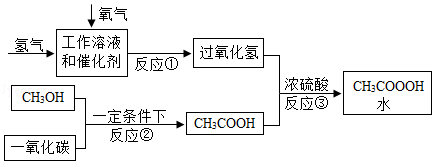
(1)认识过氧乙酸:它属于 (填“有机化合物”或“无机化合物”)。
(2)制备过氧乙酸:写出反应③的化学方程式 ;上述3个反应中属于化合反应的是 (填数字序号)。
(3)使用过氧乙酸:在校园消毒中,将lkg质量分数为20%的过氧乙酸溶液稀释至0.5%,需要加水 kg;下列关于过氧乙酸使用的说法正确的是 。
A.应低温、避开火源贮存
B.环境消毒,浓度越大越好
C.谨防溅到眼睛和皮肤上
D.最好不要用金属容器盛放
按要求填空:
(1)溶洞里形态各异的钟乳石的形成过程可简单理解为:石灰岩长时间缓慢的“溶解”在水中,水在滴落时又缓慢的生长出钟乳。钟乳石生长的化学方程式为 ,其反应类型为 。
(2)汽车尾气中含有多种氮的氧化物和一氧化碳,对空气有污染作用。有人设计在尾气处加装高效催化剂,将其转化成无污染的一种单质和一种化合物。则生成的化合物的化学式为 ,反应中化合价降低的元素符号是 。
(3)侯德榜是我国杰出的化学家,他发明的联合制碱法大大提高了原料的利用率。联合制碱的主要反应原理:向饱和的食盐溶液通入过量的氨气(易溶于水的碱性气体)和二氧化碳气体,反应后分离出碳酸氢钠。反应方程式为:NaCl(饱和)+NH3+H2O+CO2=NaHCO3+NH4Cl
向饱和的食盐溶液是先通入氨气还是二氧化碳? (填化学式)。该反应属于复分解反应,该反应能够发生的依据是 。
(4)已知某铁的氧化物可表示为FexOy=aFeO•bFe2O3.经测:15.2克的某铁的氧化物中铁的质量为11.2克。则x:y= ,a:b= (均填最小整数比)。
试题篮
()