下列属于置换反应的是( )
A.3Fe+2O2 Fe3O4B.Zn+2HCl=ZnCl2+H2↑
Fe3O4B.Zn+2HCl=ZnCl2+H2↑
C.2HgO 2Hg+O2↑D.KOH+HCI=KCl+H2O
2Hg+O2↑D.KOH+HCI=KCl+H2O
空气中含量较高的气体是氮气和氧气,氮气和氧气在放电的条件下发生化学反应的微观模拟示意图如图所示:

请回答下列问题
(1)在B图中将相关粒子的图形补充完整。
(2)此变化中发生改变的粒子是 (填化学式)。
(3)结合该图示从微观角度解释由A到B的实质是 。
(4)生成物中氮元素的化合价为 价。
(5)该反应所属的基本反应类型为 。
(6)画出O 2 ﹣的结构示意图 。
孔雀石的主要成分为Cu2(OH)2CO3,在加热条件下发生如下反应:Cu2(OH)2CO3 2R+CO2↑+H2O,请回答问题:
(1)R的化学式为 ;
(2)该反应属于 (填基本反应类型).
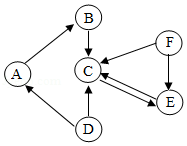
A~F均为初中化学常见的物质,他们之间的关系如图所示("→"表示转化关系,所涉及反应均为初中常见的化学反应),其中A俗称生石灰,C是最常用的溶剂,C与F元素组成相同。
(1)C的化学式是 ;
(2)D的一种用途是 ;
(3)A→B反应的基本类型是 ;
(4)F→E反应的化学方程式为 。
凡是有元素化合价发生变化的化学反应都属于氧化还原反应,下列不属于氧化还原反应的是( )
A.Zn+H2SO4═ZnSO4+H2↑
B.2H2O 2H2↑+O2↑
2H2↑+O2↑
C.2NaOH+H2SO4═Na2SO4+2H2O
D.4P+5O2 2P2O5
2P2O5
某品牌新能源电动汽车使用磷酸铁锂电池,其反应原理:LiFePO4 FePO4+Li.该电池具有容量大、续航能力强的特点。
(1)LiFePO4中铁元素与氧元素的质量比为 。
(2)该电池充电时发生的化学反应属于 (填基本反应类型)。
已知4FeS2+11O2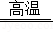 2Fe2O3+8X,则下列关于该反应说法错误的是( )
2Fe2O3+8X,则下列关于该反应说法错误的是( )
A.O2与X的相对分子质量之比为1:2
B.该反应属于置换反应
C.X属于空气污染物之一
D.该反应中硫元素的化合价升高
煤燃烧产生的废气中含有SO2,SO2是大气污染的主要气体之一,用NaOH、Na2SO3溶液可将90%以上的SO2吸收。涉及的反应有:
①2NaOH+SO2═Na2SO3+H2O
②Na2SO3+SO2+H2O═2NaHSO3
③NaHSO3+NaOH═Na2SO3+H2O
下列说法中,不正确的是( )
A.反应②发生的是化合反应
B.反应③说明NaHSO3属于酸
C.Na2SO3中硫元素的化合价是+4
D.反应①说明SO2与CO2有相似的化学性质
如图表示三种物质在密闭容器中反应一段时间后质量的变化,其反应的基本类型是( )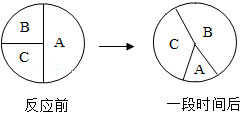
A.化合反应B.分解反应C.置换反应D.复分解反应
化学课堂上,老师做了如图一的实验(网罩的作用是集中火焰,提高温度)。

(1)随着不断加热,试管①里逐渐有红色固体产生,化学方程式为C+2CuO 2Cu+CO2↑,该反应的基本反应类型属于 。同时试管②里的现象是 ,化学方程式为 。
(2)小明发现通入试管②里的气体有逸出液面的现象,怀疑试管①里还有其它气体生成,比如一氧化碳。老师首先赞扬小明有科学的质疑精神,建议在化学兴趣小组的活动中展开探究。请你也参与其中,一起探究。
[提出问题]碳还原氧化铜的反应还有一氧化碳生成吗?
[猜想与假设]猜想一:没有一氧化碳生成;猜想二:还有一氧化碳生成
[设计方案]在老师的帮助下,小明设计出如图二实验。为了提高实验效果,小明加大了反应物的用量。老师提示:先将两个开关都打开,再加热,反复挤压气球一会儿。老师这样提示的目的是 。
[进行实验]
实验操作 |
实验现象 |
实验结论 |
先按老师的提示操作,加热一会儿后,关闭开关2.待充分反应,关闭开关1,停止加热。 |
逸出液面的气体不是二氧化碳 |
|
逸出液面的气体是一氧化碳。猜想二成立。 |
[交流与提高]同学们通过对以上实验的讨论与分析,认为一氧化碳的产生至少源自两个反应:一是试管内反应物直接反应生成;二是生成物又发生反应而生成。请你写出其中一个化学方程式 。
实验中生成的二氧化碳被氢氧化钠浓溶液吸收没有明显现象,同学们想进一步检验该反应的生成物,可选用的药品有 (填序号)。
①酚酞溶液 ②氢氧化钙溶液 ③稀盐酸 ④锌粒 ⑤氯化钙溶液
[评价与反思]经过本次活动,同学们感到,正是因为小明具有 精神,我们这次活动才有了更多、更新的收获。
水与自然界中矿石长期接触,常含Ca(HCO3)2、Mg(HCO3)2等物质,导致钙离子、镁离子含量较多,称之为硬水。生活中,水的硬度过高会造成一定危害。长期使用硬水烧水的热水壶,内部会形成一层水垢,其主要成分为碳酸钙和氢氧化镁,说明加热煮沸可使这类硬水成为软水。其原理的流程如下(气体产物已略去):

回答下列问题:
(1)反应Ⅰ属于四大基本反应类型中的 反应;反应Ⅱ除产生水垢外,还有一种气体产物为 ;如果当地硬水中CaSO4含量较多,则水垢中还常含有少量CaSO4,CaSO4析出的原因是 。
(2)向200g水垢中加入400g过量的稀盐酸,充分反应,测得3分钟内混合物质量的变化(不考虑水与HCl的挥发)如下表所示:
时间/s(秒) |
0 |
30 |
60 |
90 |
120 |
180 |
混合物的质量/g |
600 |
574 |
554 |
547.2 |
547.2 |
547.2 |
①观察到的现象是 。
②计算水垢中碳酸钙的质量分数,写出必要的计算过程。
某兴趣小组利用氯酸钾和二氧化锰制取氧气并回收剩余固体,实验过程表示如图
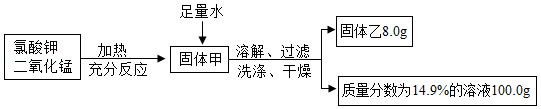
(1)上述制取氧气的反应属于 (填基本反应类型)。
(2)计算所用氯酸钾、二氧化锰混合物的总质量。
绿色环保是未来工业发展的方向,我市锰矿资源丰富,某电解锰厂排放的废液中可能含有少量硫酸,某校兴趣小组同学取该废液样品100g,加入某碱性M物质充分反应后得到的相关数据如图(废液中其它物质不与M物质反应)。请根据相关知识和图表信息回答下列问题。
(1)从经济和效果考虑,该电解锰厂应选择什么物质除去废液中硫酸?
(2)该反应的基本类型是 。
(3)计算废液中硫酸的质量分数(写出计算过程)。

CO2是最主要的温室气体,也是巨大的碳资源,CO2的低能耗捕集、转化和利用正受到世界各国的广泛关注。
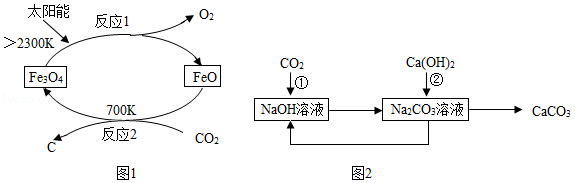
(1)以CO2为原料制取炭黑的太阳能工艺如图1所示。
①反应1的基本类型为 。
②反应2中碳元素的化合价 (填“升高”“不变”或“降低”)。
(2)利用NaOH溶液吸收CO2,部分转化关系见图2。
反应①的化学方程式为 ,该转化中循环使用的物质是 。
(3)利用Na2CO3或K2CO3溶液吸收低浓度的CO2,将其转化为NaHCO3或KHCO3,NaHCO3或KHCO3受热分解生成高浓度的CO2储存利用,生成的Na2CO3或K2CO3循环使用以降低生产成本。
吸收剂 |
Na2CO3 |
K2CO3 |
20℃最高浓度(g/L) |
212 |
1104 |
价格(元/Kg) |
1.25 |
9.80 |
根据表中信息,选择K2CO3溶液作吸收液的优点是 。
(4)利用一种新型“人造树叶”将CO2转化为乙醇(C2H5OH)的反应如下:2CO2+3H2O C2H5OH+3O2,研究显示,1L“人造树叶”每天能从空气中吸收968g CO2,计算1L“人造树叶”工作1天可得到乙醇的质量(写出计算过程)。
(5)某研究小组设计如图3所示实验,探究CO2和H2在一定条件下反应的产物。
查阅资料:①CO2和H2在合适催化剂和一定温度下反应转化为CO和H2O;
②白色无水硫酸铜吸水后变为蓝色。
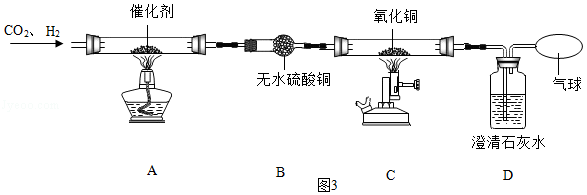
实验过程中观察到的主要现象有:B装置中白色固体变为蓝色,C装置中黑色固体变为红色,D装置中澄清石灰水变浑浊。
①设计B装置的目的是 。
②C装置中发生的反应的化学方程式为 。
③研究小组反思后认为,根据上述实验现象不能确认CO2和H2反应生成了CO,理由是 。
试题篮
()