硝酸铵在一定条件下发生如下反应:NH4NO3 N2O↑+2X.则X的化学式为( )
A.H2B.NH3C.H2OD.H2O2
我国载人航天技术达到了世界先进水平。其中“神舟号”系列火箭使用的一种燃料是偏二甲肼,其化学式为C2H8N2,燃烧时发生如下反应:C2H8N2+2X 2CO2+4H2O+3N2,则X的化学式是( )
A.NOB.NO2C.N2OD.N2O4
工业上可以用电解饱和食盐水的方法来制取氯气、氢气及另外一种重要的化工原料,反应方程式为2NaC1+2H 2O 2X+C1 2↑+H 2↑(方程式已配平),则X的化学式为( )
| A. |
HCl |
B. |
NaOH |
C. |
NaClO |
D. |
Na 2O |
在一个密闭容器中有A、B、C、D四种物质,在一定条件下充分反应,测得数据如表:
| 物质 |
A |
B |
C |
D |
| 反应前的质量/g |
6.4 |
3.2 |
4.0 |
2.8 |
| 反应后的质量/g |
5.2 |
待测 |
7.2 |
2.0 |
反应后待测的B的质量是 克,该反应所属的基本反应类型是 。
化学式造福人类的科学.
(1)能源化学﹣﹣使用新能源的汽车可节约化石燃料.化石燃料包括煤、天然气和 ;
(2)农业化学﹣﹣化肥对提高农作物产量具有重要作用.尿素属于 (填"氮"、"磷"或"钾")肥;
(3)医药化学﹣﹣我国药学家屠呦呦因研制抗疟新药青蒿素获得诺贝尔奖.由青蒿酸(C 15H 22O 2)合成青蒿素(C 15H 22O 5)的过程中主要发生了 (填"物理"或"化学")变化;
(4)材料化学﹣﹣南昌大学研发的"硅衬底高光效GaN基蓝色发光二极管技术"获得2015年国家技术发明一等奖.请回答下列问题:
①传统制备氮化镓(GaN)的化学原理是:GaCl 3+NH 3 GaN+3X,其中X的化学式为 .
②镓元素的原子结构示意图为  ,下列原子结构示意图所对应的元素与镓元素的化学性质相似的是 (填序号).
,下列原子结构示意图所对应的元素与镓元素的化学性质相似的是 (填序号).
| A. |
|
B. |
|
C. |
|
D. |
|
某物质X在空气中燃烧的化学方程式为:X+3O 2 2CO 2+2H 2O,下列说法正确的是( )
| A. |
X 的化学式是 C 2H 4 |
| B. |
该反应属于置换反应 |
| C. |
O 2中氧元素的化合价为﹣2 |
| D. |
CO 2中碳、氧元素的质量比为 1:2 |
在一定条件下,一个密闭容器内发生某反应,测得反应过程中各物质的质量部分数据如表所示:下列说法正确的是( )
物质 |
甲 |
乙 |
丙 |
丁 |
反应前的质量/g |
12 |
26 |
3 |
0 |
反应中的质量/g |
9 |
22 |
3 |
b |
反应后的质量/g |
0 |
a |
3 |
28 |
A.a等于10
B.该化学反应为复分解反应
C.丙一定为催化剂
D.b等于12
碳可以与浓硫酸在加热的条件下发生如下反应:C+2H2SO4(浓) CO2↑+2X↑+2H2O其中X的化学式为( )
CO2↑+2X↑+2H2O其中X的化学式为( )
A.O2B.SO3C.SO2D.H2S
在"2A+3B=2C+4D"的反应中,已知8g物质A完全反应生成11g物质C和9g物质D.若A的相对分子质量为32,则物质B的相对分子质量( )
| A. |
16 |
B. |
32 |
C. |
48 |
D. |
64 |
某市空气受到SO 2的严重污染,环保部门立即派出飞机喷洒X粉末,快速降低空气中的SO 2含量,该过程发生的化学反应是2X+2SO 2+O 2═2CaSO 4+2CO 2,X的化学式是( )
| A. |
H 2O |
B. |
Na 2CO 3 |
C. |
CaO |
D. |
CaCO 3 |
农业生产中有一种氮肥,若运输过程中受到猛烈的撞击,会发生爆炸性分解,其反应的化学方程式为:2X═2N 2↑+O 2+4H 2O,则X的化学式是( )
| A. |
NH 4NO 3 |
B. |
NH 4HCO 3 |
C. |
NH 3•H 2O |
D. |
NH 3 |
生活中处处有化学,请用所学知识回答下列问题:
(1)明矾可用于净水,是因为明矾溶于水生成的胶状物可以 悬浮于水中的杂质,使之从水中沉降出来,日常生活中常用 的方法降低水的硬度.
(2)某学校食堂的早餐提供:鸡蛋、小米粥、鲜肉包、馒头及面条,请你从均衡营养的角度建议食堂增加含 的食物(填字母)
A.蛋白质 B.油脂 C.糖类 D.维生素
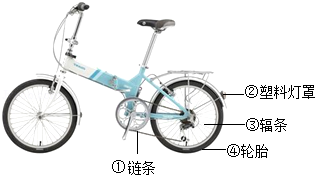
(3)图中所标示的各部件中,属于有机合成材料的是 (填序号)
(4)甲醛(CH3OH)有毒,误饮可使眼镜失明,甚至死亡,最新研究证明,用氨气(NH3)处理含有甲醛的工业废水,可使其转变成无毒的物质,有关反应的化学方程式为5CH3OH+12O2+6NH3 3X+5CO2+19H2O,则X的化学式为 .
3X+5CO2+19H2O,则X的化学式为 .
(5)丙烷(C3H8)是家用液化石油气的主要成分之一,它和甲烷在空气中染色生成物相同,请写出丙烷燃烧的化学方程式 .
工业上用100t含氧化铁(Fe 2O 3)80%的赤铁矿石,理论上可以冶炼出含铁96%的生铁的质量是( )
| A. |
56t |
B. |
58.3t |
C. |
70t |
D. |
72.9t |
在奥运比赛中,举重运动员举重前常用白色的"镁粉"搓手,是因为"镁粉"质轻,吸水性好,可做防滑剂。"镁粉"的有效成分是碱式碳酸镁,它不可以燃烧,300℃即分解,其分解的化学方程式为Mg 5(OH) 2(CO 3) 4  5MgO+H 2O+4X↑,则X的化学式是( )
5MgO+H 2O+4X↑,则X的化学式是( )
| A. |
CO |
B. |
CO 2 |
C. |
O 2 |
D. |
Mg(OH) 2 |
试题篮
()