发展低碳经济,降低碳排放,就是要尽量减少温室气体二氧化碳的排放!如图是部分物质与二氧化碳的相互转化关系,请回答下列问题:
(1)碳酸钠在高温下与SiO2发生反应,化学方程式为:Na2CO3+SiO2  Na2SiO3+CO2↑,Na2SiO3中硅元素的化合价为 价;
Na2SiO3+CO2↑,Na2SiO3中硅元素的化合价为 价;
(2)葡萄糖在酶的催化作用下缓慢氧化可转变为二氧化碳,其原理可以表示为:C6H12O6+6O2  6CO2+6X,其中X的化学式为 ;
6CO2+6X,其中X的化学式为 ;
(3)物质R能发生分解反应生成CO2,写出一个符合要求的化学方程式 ;
(4)甲烷是天然气的主要成分,甲烷(CH4)、乙烷(C2H6)、丙烷、丁烷(C4H10)等物质都属于有机物中的烷烃,写出丙烷燃烧的化学方程式 。

碳酸钠俗称纯碱或苏打,在生活、生产和实验研究中均有广泛应用。
[配制溶液]配制溶质质量分数分别为1%、2%和4%的Na2CO3溶液
(1)若配制50g溶质质量分数为4%的Na2CO3溶液,下列操作正确的是 (填字母)。
a.用托盘天平称取2g Na2CO3固体
b.选用50mL量筒量取所需体积的水
c.选用带玻璃塞的广口试剂瓶,将配好的溶液装瓶并贴标签
(2)分别测定25℃时,上述3种溶液的pH,记录数据如下:
实验编号 |
Ⅰ |
Ⅱ |
III |
溶质质量分数 |
1% |
2% |
4% |
溶液pH |
11.62 |
11.76 |
11.90 |
分析Ⅰ、Ⅱ、Ⅲ三组数据可得出的结论是 。
[制备物质]用Na2CO3溶液和FeSO4溶液发生复分解反应制备FeCO3
[已知溶液pH大于8.8时,Fe2+完全生成Fe(OH)2沉淀]
(3)在烧杯中制备FeCO3沉淀时,应选用的加料方式是 (填字母)。
a.将FeSO4溶液与Na2CO3溶液同时加入到烧杯中
b.将Na2CO3溶液缓慢加入到盛有FeSO4溶液的烧杯中
c.将FeSO4溶液缓慢加入到盛有Na2CO3溶液的烧杯中
(4)潮湿的FeCO3固体置于空气中易变质,反应如下:4FeCO3+6H2O+O2═4X+4CO2.则X的化学式为 。
[标定浓度]标定待测盐酸的溶质质量分数
(5)将Na2CO3固体在270℃干燥至恒重,准确称取0.212g无水Na2CO3于锥形瓶中,加入50mL蒸馏水溶解,滴入待测盐酸,当两者恰好完全反应时,消耗盐酸的体积为20.00mL(该盐酸的密度近似等于lg•mL﹣1,反应中Na2CO3所含的碳元素全部转化为CO2)。
①列式计算待测盐酸的溶质质量分数(结果用百分数表示,保留两位小数)。
②若上述测定过程中Na2CO3固体未经充分干燥,则测出盐酸的溶质质量分数将 (填“偏大”、“偏小”或“无影响”)。
自来水厂有一种新型的消毒剂ClO2,其工业生产原理是:2NaClO3+4X=2ClO2↑+Cl2↑+2NaCl+2H2O,则X 的化学式为 。
化学与生活、社会、环境密切相关。
(1)打开可乐瓶盖后,有大量气泡冒出,这种现象说明气体的溶解度与 有关。
(2)制备手机芯片的主要材料是硅,可以利用石英砂(主要成分是SiO2)制得,二氧化硅中硅元素的化合价是 。
(3)防疫期间,人们常用84消毒液【主要成分为次氯酸钠(NaClO)】对生活场所进行杀菌、消毒。工业上制备NaClO的反应原理为2NaOH+Cl2═X+NaClO+H2O,则X的化学式为 。
(4)山药中含有碱性皂角素,皮肤沾上会奇痒难忍。你认为可涂厨房中的 (填溶质名称)来止痒。
(5)煤燃烧时放出的二氧化氮、 (填化学式)等污染物,这些气体或气体在空气中发生反应后的生成物溶于雨水,会形成酸雨。
消毒与清洁对公共场所和家庭是至关重要的。
(1)二氧化氯(ClO 2)可作水处理消毒剂,二氧化氯中氯元素的化合价是 。
(2)"洁则灵"与"漂白剂"不能混用,二者若混合易产生一种有毒气体X.反应原理为:NaClO+2HCl=NaCl+X↑+H 2O,则X的化学式为 。
(3)用炉具清洁剂(含有NaOH )清洗炉具时,应避免接触皮肤,其原因是 。
(4)使用洗洁剂清洗餐具上的油污时,利用了洗涤剂对油污的 作用。
2020年1月23日,永州首例新型冠状病毒感染的肺炎患者确诊后,全市实施居家隔离措施。在居家抗疫中,我们常使用浓度为75%的酒精(C2H5OH)和“84消毒液”(有效成分为NaClO)进行消毒杀菌。请回答下列问题:
(1)①在酒精分子中,C、H、O的原子个数比为 。
②下列对酒精性质的描述,属于化学性质的是 。
A.易挥发
B.消毒杀菌
C.无色有特殊香味
D.熔点﹣114℃、沸点78℃
(2)①“84消毒液”与厕所清洁剂(俗称“洁厕灵”,有效成分为稀盐酸)可发生反应:
NaClO+2HCl═NaCl+Cl2↑(有毒)+H2O
在使用过程中,这两种物质 (填“能”或“不能”)混合使用。
②在实验室可往NaOH溶液中通入Cl2制得“84消毒液”,请完成此反应的化学方程式:2NaOH+Cl2═NaClO+ +H2O
(3)在疫情防控中,你做了哪些有效的防护措施 (写一条即可)。
燃料的发现和利用提高了人类生活的质量,推动了人类文明的进步。
(1)将煤隔绝空气加强热,得到焦炭、煤气等,该过程属于 (填“物理”或“化学”)变化。煤与高温水蒸气反应生成CO和H2.在300℃、1.5MPa、催化剂存在的条件下,CO和H2可转变为液体燃料甲醇(CH3OH)。写出CO与H2反应成甲醇的化学方程式: 。
(2)焦炭(主要成分是碳)是高炉炼铁的重要原料。炼铁高炉内发生的主要化学反应如图1所示,其中反应②体现了焦炭的 性。

(3)乙醇可作为酒精灯、酒精喷灯的燃料。某铜质酒精喷灯的结构如图2所示。使用酒精喷灯时,先在预热盘中注入酒精并点燃,一段时间后,调节空气调节杆,即可点燃酒精喷灯。结合燃烧的条件回答:点燃预热盘中酒精的目的是 。
(4)氢气的制取和储存越来越受到人们的关注。
①最理想的制氢方法:在合适的催化剂作用下,利用太阳光使水分解。该制氢过程 (填“吸收”和“放出”)能量,生成的氢气与氧气在相同条件下的体积之比为 。
②我国稀土资源丰富,某种稀土储氢材料(用M表示)的储氢原理可表示为M+3H2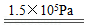 LaNi5H6.M的化学式为 。
LaNi5H6.M的化学式为 。
医用消毒酒精为75%的乙醇溶液,化工生产中可用A(主要成分的化学式为C8H18)作原料,经以下流程制取乙醇:

(1)步骤①的转化属于 (选填“化学”或“物理”)变化。
(2)步骤②是乙烯和含两种元素的化合物B发生化合反应,则B中所含元素是 。
化学变化是反应物的原子重新组合转变成生成物的过程。图3是某化学变化过程的微观示意图。
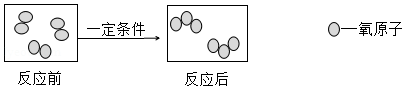
(1)图示反应的化学方程式为 。
(2)下列关于图示反应的说法正确的是 。
A.该反应属于化合反应 B.反应前后原子的种类不变 C.反应前后分子的个数不变
(3)图示反应前后物质的质量之比为 。
2020年6月23日9时43分,我国长征三号乙运载火箭将北斗系统第55颗导航卫星成功送入预定轨道,标志着我国北斗卫星导航系统正式建成。长征三号乙运载火箭是一种三级大型液体捆绑式运载火箭。它的第一、二级使用偏二甲肼(C 2H 8N 2)和四氧化二氮(N 2O 4)作为推进剂,其反应原理为:C 2H 8N 2+2N 2O 4 2CO 2+3X+4H 2O,反应放出大量的热产生推力,第三级则使用效能更高的液氢和液氧作为推进剂。请根据以上信息回答下列问题:
(1)四氧化二氮中氮元素的化合价为 ,物质X的化学式为 ;
(2)火箭第三级中发生反应的化学方程式为 。
中国承诺在2030年前实现碳达峰,2060年前实现碳中和。请回答下列问题。

(1)自然界中CO2的来源有 (任写一点),大气中的CO2过多会引起 效应增强。
(2)“碳捕捉和封存”技术是实现碳中和的重要途径之一。用NaOH溶液喷淋“捕捉”空气中的CO2,可达到消耗CO2的目的,写出该反应的化学方程式 。重庆合川实验基地通过如图1技术将CO2压入地下实现CO2的封存。此封存技术可行的依据是 。
(3)若CO2能合理利用,将会是一种重要的原料。
①CO2与H2在催化条件下反应生成甲醇。反应的化学方程式为CO2+3H2 X+H2O,X的化学式为 。
X+H2O,X的化学式为 。
②CO2可用于食品保鲜,实验测得气体中的CO2体积分数与溶液pH的关系如图2所示。
a.气体中CO2体积分数增大时,造成图示变化的主要原因是溶液中 的浓度增大(填化学式)。
b.智能化食品包装通过颜色变化显示包装内CO2气体含量的变化。举出一种可通过颜色变化用于该智能化包装的物质 。
我国力争在2060年前实现"碳中和"(二氧化碳的排放与吸收平衡,实现"零排放"),保护环境。实现"碳中和"通常可采取如下措施:
(1)碳减排:使用氢能源汽车可以有效减少二氧化碳的排放。单质硼(B)可与物质X反应制取氢气,化学方程式为:2B+6X  2B(OH) 3+3H 2↑,则X的化学式为 ,B(OH) 3中B的化合价为 。
2B(OH) 3+3H 2↑,则X的化学式为 ,B(OH) 3中B的化合价为 。
(2)碳"捕捉"与封存:碳"捕捉"可用氢氧化钠溶液吸收空气中的二氧化碳,该反应的化学方程式为 。
(3)碳转化:一定条件下,可将二氧化碳在催化剂表面转化成某种有机清洁燃料,其反应原理如图所示,该反应的化学方程式为 。

金属钛常被用于航天、化工、医疗领域,工业上常用钛铁矿制取钛,并获得副产品氧化铁,其工艺流程的部分步骤如图所示:

(1)TiO2中钛元素的化合价为 。
(2)在下列反应中,属于分解反应的有 (填标号)。
A.反应①
B.反应②
C.反应③
D.反应④
(3)反应⑤的化学方程式为:2FeSO4 Fe2O3+SO3↑+X↑,则X的化学式为 。
复学防疫,化学助力。
(1)起床后,测体温。测体温时水银体温计中汞柱会上升的微观原因是汞原子 。
(2)上学时,戴口罩。制作口罩用的无纺布面料主要是聚丙烯[(C3H6)n],聚丙烯中碳、氢元素的质量比为 。
(3)到校后,勤消毒。过氧乙酸用于教室消毒,其化学性质不稳定,分解的化学方程式为:2C2H4O3═2C2H4O2+X↑,则X的化学式为 。用于手部消毒的酒精溶液属于易燃物,使用时要注意安全,酒精燃烧的化学方程式为 。
(4)用餐时,讲营养。如午餐仅食用米饭、红烧肉、鸡蛋汤、牛奶,从均衡营养角度出发还应补充的一种食物是 。
试题篮
()