化学式造福人类的科学.
(1)能源化学﹣﹣使用新能源的汽车可节约化石燃料.化石燃料包括煤、天然气和 ;
(2)农业化学﹣﹣化肥对提高农作物产量具有重要作用.尿素属于 (填"氮"、"磷"或"钾")肥;
(3)医药化学﹣﹣我国药学家屠呦呦因研制抗疟新药青蒿素获得诺贝尔奖.由青蒿酸(C 15H 22O 2)合成青蒿素(C 15H 22O 5)的过程中主要发生了 (填"物理"或"化学")变化;
(4)材料化学﹣﹣南昌大学研发的"硅衬底高光效GaN基蓝色发光二极管技术"获得2015年国家技术发明一等奖.请回答下列问题:
①传统制备氮化镓(GaN)的化学原理是:GaCl 3+NH 3 GaN+3X,其中X的化学式为 .
②镓元素的原子结构示意图为  ,下列原子结构示意图所对应的元素与镓元素的化学性质相似的是 (填序号).
,下列原子结构示意图所对应的元素与镓元素的化学性质相似的是 (填序号).
| A. |
|
B. |
|
C. |
|
D. |
|
碳酸钠俗称纯碱或苏打,在生活、生产和实验研究中均有广泛应用。
[配制溶液]配制溶质质量分数分别为1%、2%和4%的Na2CO3溶液
(1)若配制50g溶质质量分数为4%的Na2CO3溶液,下列操作正确的是 (填字母)。
a.用托盘天平称取2g Na2CO3固体
b.选用50mL量筒量取所需体积的水
c.选用带玻璃塞的广口试剂瓶,将配好的溶液装瓶并贴标签
(2)分别测定25℃时,上述3种溶液的pH,记录数据如下:
实验编号 |
Ⅰ |
Ⅱ |
III |
溶质质量分数 |
1% |
2% |
4% |
溶液pH |
11.62 |
11.76 |
11.90 |
分析Ⅰ、Ⅱ、Ⅲ三组数据可得出的结论是 。
[制备物质]用Na2CO3溶液和FeSO4溶液发生复分解反应制备FeCO3
[已知溶液pH大于8.8时,Fe2+完全生成Fe(OH)2沉淀]
(3)在烧杯中制备FeCO3沉淀时,应选用的加料方式是 (填字母)。
a.将FeSO4溶液与Na2CO3溶液同时加入到烧杯中
b.将Na2CO3溶液缓慢加入到盛有FeSO4溶液的烧杯中
c.将FeSO4溶液缓慢加入到盛有Na2CO3溶液的烧杯中
(4)潮湿的FeCO3固体置于空气中易变质,反应如下:4FeCO3+6H2O+O2═4X+4CO2.则X的化学式为 。
[标定浓度]标定待测盐酸的溶质质量分数
(5)将Na2CO3固体在270℃干燥至恒重,准确称取0.212g无水Na2CO3于锥形瓶中,加入50mL蒸馏水溶解,滴入待测盐酸,当两者恰好完全反应时,消耗盐酸的体积为20.00mL(该盐酸的密度近似等于lg•mL﹣1,反应中Na2CO3所含的碳元素全部转化为CO2)。
①列式计算待测盐酸的溶质质量分数(结果用百分数表示,保留两位小数)。
②若上述测定过程中Na2CO3固体未经充分干燥,则测出盐酸的溶质质量分数将 (填“偏大”、“偏小”或“无影响”)。
(1)“酒香不怕巷子深”,说明分子 ;
(2)某有机物在空气中燃烧生成二氧化碳和水,该有机物的组成肯定有 元素;
(3)在过滤操作中,玻璃棒的作用是 .
消毒与清洁对公共场所和家庭是至关重要的。
(1)二氧化氯(ClO 2)可作水处理消毒剂,二氧化氯中氯元素的化合价是 。
(2)"洁则灵"与"漂白剂"不能混用,二者若混合易产生一种有毒气体X.反应原理为:NaClO+2HCl=NaCl+X↑+H 2O,则X的化学式为 。
(3)用炉具清洁剂(含有NaOH )清洗炉具时,应避免接触皮肤,其原因是 。
(4)使用洗洁剂清洗餐具上的油污时,利用了洗涤剂对油污的 作用。
现有一份氧元素质量分数为 89.5%的过氧化氢溶液,加入MnO2充分反应后,得到液体的质量为90g(不考虑操作过程中液体的损失),则生成氧气的质量为 g(精确到小数点后1位)。
坚持“人与自然和谐共生”是新时代中国特色社会主义的基本方略之一,让“山更绿,水更清,空气更清新”是我们共同的追求。
(1)“山更绿”离不开绿色植物。
①植物的光合作用需要吸收空气中的水和 ,可有效减缓温室效应。
②酸雨不利于植物生长。煤燃烧产生的 进入大气后可形成“硫酸型”酸雨。
(2)“水更清”就得保护好水资源。
①下列关于水的说法正确的是 (填字母)。
a.工业废水需经处理达标后才可排放
b.为保护好水资源,禁止使用化肥和农药
c.天然水只要通过处理后变清即可饮用
d.为了改善水质,可向其中加入大量的净水剂和消毒剂
②“赤潮”或“水华”主要是由于水中某些营养元素含量过高,导致藻类大量繁殖,鱼类等死亡。这里的营养元素主要指 (写出一种即可)。
(3)“空气更清新”需要监测防治大气污染。
①目前未计入空气污染指数监测项目的有 (填字母)。
a.一氧化碳 b.二氧化氮 c.可吸入颗粒物 d.稀有气体
②硝酸工厂排放的尾气中常含有NO、NO2等有害气体,可用氢氧化钠溶液来吸收:NO+NO2+2NaOH=2X+H2O. X的化学式为 。
氧烛是一种用于缺氧环境中自救的化学氧源,广泛用于航空、航海等领域,其主要成分为NaClO3还含有适量的催化剂、成型剂等。氧烛通过撞击火帽引发反应后,能持续放出高纯氧气,主要反应原理为2NaClO3 2X+3O2↑,则X的化学式为 ,该反应属于基本反应类型中的 ,NaClO3中Cl的化合价为 。
2X+3O2↑,则X的化学式为 ,该反应属于基本反应类型中的 ,NaClO3中Cl的化合价为 。
维C泡腾片是一种常见的补充维生素C的保健品。某品牌维C泡腾片(以下称“本品”)的主要成分如图1所示。
(1)下列关于维生素C的说法正确的是 (填字母)。
a.维生素C由C、H、O三种元素组成
b.维生素C的相对分子质量为176g
C.维生素C由6个碳原子、8个氢原子和6个氧原子构成
d.维生素C中C、H、O元素的质量比为9:1:12
(2)阅读本品的营养成分表:每100g维C泡腾片含钠5750mg(1mg=10﹣3g)。已知本品其他成分不含钠元素,则本品中碳酸氢钠的质量分数为 。
(3)维C泡腾片水溶液酸碱性的测定:将本品一片投入蒸馏水中,有气泡产生,反应原理为:H3C6H5O2+3NaHCO3=Na3C6H5O2+3CO2↑+3 (填化学式)。
待不再产生气体后,测得溶液呈酸性。
(4)维C泡腾片中碳酸氢钠质量分数的测定:称量相关实验用品质量,将本品一片投入蒸馏水中,待不再产生气体后,称量锥形瓶及瓶内所有物质的总质量。装置如图2所示。
相关数据如表:
物品 |
反应前 |
反应后 |
||
锥形瓶 |
蒸馏水 |
维C泡腾片 |
锥形瓶及瓶内所有物质 |
|
质量/g |
71.75 |
50.00 |
4.00 |
125.53 |
①根据以上数据计算本品中碳酸氢钠的质量分数(写出计算过程,结果精确到0.1%)。
②实验测定结果与题(2)计算结果相比有明显偏差,其可能原因是 。

建立宏观﹣微观的联系是化学学习的重要思想.阅读下列材料,回答问题.
材料:2017年5月18日,我国试采可燃冰成功,这将点亮新能源时代曙光.可燃冰是天然气(甲烷CH4)和水在高压低温条件下形成的类冰状物质,1体积可燃冰可释放出约164体积的天然气,可燃冰有储量巨大、高效清洁、燃烧值高的特点.
(1)甲烷是 (填“有机物”或“无机物”),对“1体积可燃冰可释放出约164体积的天然气”体积明显增大的微观解释是 .
(2)如图是甲烷燃烧时反应的微观示意图.

就该反应,从质量守恒角度看,请在图方框中补充画出微观粒子,完善微观示意图;从微观角度看,没有发生变化的是 ;从能量角度看,能量变化是 .
(3)如图所示的反应是氧化反应,其特征是反应前后有元素化合价的变化,则反应中发生化合价变化的元素有 .
2020年1月23日,永州首例新型冠状病毒感染的肺炎患者确诊后,全市实施居家隔离措施。在居家抗疫中,我们常使用浓度为75%的酒精(C2H5OH)和“84消毒液”(有效成分为NaClO)进行消毒杀菌。请回答下列问题:
(1)①在酒精分子中,C、H、O的原子个数比为 。
②下列对酒精性质的描述,属于化学性质的是 。
A.易挥发
B.消毒杀菌
C.无色有特殊香味
D.熔点﹣114℃、沸点78℃
(2)①“84消毒液”与厕所清洁剂(俗称“洁厕灵”,有效成分为稀盐酸)可发生反应:
NaClO+2HCl═NaCl+Cl2↑(有毒)+H2O
在使用过程中,这两种物质 (填“能”或“不能”)混合使用。
②在实验室可往NaOH溶液中通入Cl2制得“84消毒液”,请完成此反应的化学方程式:2NaOH+Cl2═NaClO+ +H2O
(3)在疫情防控中,你做了哪些有效的防护措施 (写一条即可)。
防疫情,测体温。体温测量仪功不可没。
(1)传统型﹣﹣体温计。含汞体温计将在2026年起全面禁止生产,因为汞是人体中的 (选填“必需”或“有害”)元素。汞的元素符号是 。
(2)方便型﹣﹣额温枪。某种额温枪的红外温度传感器所用材料含有钽酸锂(LiTaO3)。钽酸锂中锂元素(Li)的化合价为+1价,则钽元素(Ta)的化合价为 价。在惰性气氛中制取钽的原理为:5Na+K2TaF7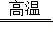 Ta+2KF+5R,则R的化学式为 。
Ta+2KF+5R,则R的化学式为 。
(3)快捷型﹣﹣红外热成像测温仪。该测温仪可实现远距离、多目标、非接触式测温,可用于快速筛查人群中的高温个体。
①该测温仪还可用于 。(填序号,双选)
A.测量物质溶解时的热量变化
B.分析赣江水质
C.探测炼铁高炉是否漏热
D.检测室内甲醛含量是否超标
②该测温仪外壳的塑料是热固性塑料。生活中检验热固性塑料的方法是 。
阅读下面的短文,回答有关问题。
新型灭菌消毒剂﹣﹣ClO2
目前,新冠肺炎疫情肆虐全球。为抑制新冠病毒传播,“含氯消毒剂”被广泛使用,其中就包含一种新型灭菌消毒剂﹣﹣ClO2.在通常情况下,ClO2是一种有刺激性气味的黄绿色,气体,熔点﹣59℃,沸点11℃.在常温下,1L水中大约能溶解2.9g ClO2.ClO2受热或者见光易分解,具有强氧化性和很强的腐蚀性。含有2%的ClO2和0.085% Na2CO3的水溶液无色、无臭、无腐蚀性,常温下稳定,不易分解;该溶液用于杀菌、消毒的同时,还有除臭、防霉、保鲜等作用,是特性优良、高效安全的消毒剂。我国从2000年起就逐渐用ClO2取代氯气(Cl2)对饮用水进行消毒。
(1)ClO2的名称是 ,分子中氯元素的化合价是 。
(2)下列消毒剂中,不属于“含氯消毒剂”的是 (填字母序号)。
A.84消毒液(含NaClO)
B.双氧水
C.氯气
D.过氧乙酸(C2H4O3)
(3)ClO2的化学性质有 (写出两点即可)。
(4)下列有关ClO2的说法正确的是 (填字母序号)。
A.0℃时,ClO2为黄绿色气体
B.常温下,100g水中大约能溶解0.29g ClO2
C.用棕色试剂瓶盛装ClO2并置于冷暗处保存
D.ClO2溶液浓度越小杀菌效果越差
(5)ClO2遇热水生成次氯酸(HClO)和两种气态单质。完成该反应的化学方程式:8C1O2+2H2O + + 。
防范新冠疫情,需要我们"戴口罩,勤洗手,勤消毒,勤通风"。
(1)医用口罩的核心材料是聚丙烯制成的熔喷布,聚丙烯属于 (填"金属材料"或"有机合成材料");
(2)请从微现角度解释:教室进行消杀后室内充满消毒液气味的原因 ;
(3)某消毒液稀释后pH=6,则稀释前其pH (填">"、"="或"<")6;
(4)在疫情期间要学会正确的洗手方法,沾有油污的手,可使用洗洁精清洗,洗洁精的作用是 ;
(5)"84消毒液"的主要成分是次氯酸钠(NaClO)。其中氯元素的化合价是 ,制取NaClO的原理是2NaOH+Cl 2═NaClO+X+H 2O,其中X的化学式是 ;
(6)某校要配制100kg溶质质量分数为0.2%的过氧乙酸消毒液,需要10%的过氧乙酸溶液 kg,所需水的质量为 kg。
科学使用化学物质,可以保障人体健康。
(1)某同学的部分体液的pH如图所示。
①图中碱性最强的体液是 。
②该同学胃酸(主要成分为盐酸)过多,可服用胃舒平[主要成分为Al(OH)3]治疗,其原理是 (用化学方程式表示)。
(2)某84消毒液产品的部分说明如下表。
84消毒液 [产品特点]主要成分为次氯酸钠(NaClO),有效氯的质量分数为5.1%~6.9%。 [餐具消毒]用有效氯的质量分数为0.04%的消毒液浸泡,20min后用生活饮用水冲净。 [注意事项]①外用消毒剂,须稀释后使用。 ②不得将本产品与酸性产品(如洁厕类清洁产品)同时使用。 |
①依据表中信息,将有效氯的质量分数为6.0%的84消毒液与水按质量比为1: 进行稀释,即可用于餐具消毒。
②洁厕灵(主要成分为盐酸)与84消毒液混合会产生有毒的氯气(Cl2)。请将该反应的化学方程式补充完整:2HCl+NaClO═ +Cl2↑+H2O

厉害了我的国!厉害了复兴号!复兴号动车组列车(如图)是由中国铁路总公司牵头组织研制、具有完全自主知识产权、达到世界先进水平的动车组列车。
(1)列车利用碳滑板与接触网接触来获取电。碳滑板通常用石墨制成,是因为石墨具有 性;石墨在常温下,受日光照射或与空气、水分接触都不容易起变化,说明其化学性质 。
(2)制造列车的材料有:铝合金、不锈钢、高强度钢、高分子材料等。不锈钢、铝合金属于 (选填"金属材料"或"合成材料");铝合金的硬度比纯铝的硬度 ;在空气中,铝制品耐腐蚀的原因是 。
(3)列车轨道建设中常用铝和氧化铁(化学式为Fe 2O 3)在高温条件下发生反应,生成熔融状态下的铁单质对钢轨中的缝隙进行焊接。其反应的化学方程式为:Fe 2O 3+2Al 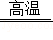 X+2Fe,则X的化学式为 ,该反应属于 (选填"置换"或"复分解")反应。
X+2Fe,则X的化学式为 ,该反应属于 (选填"置换"或"复分解")反应。

试题篮
()