某兴趣小组在相同条件下,将10.00g下列物质分别置于相同规格的烧杯,并敞口存放于空气中,烧杯中物质质量随时间变化如表,回答下列问题。
| 时间 |
质量/g |
|||||
| |
水 |
饱和石灰水 |
稀盐酸 |
浓硫酸 |
氯化钠浓溶液 |
氯化钙浓溶液 |
| 1天 |
8.16 |
8.37 |
8.64 |
11.18 |
9.38 |
10.25 |
| 2天 |
5.76 |
5.94 |
6.69 |
12.55 |
8.47 |
10.33 |
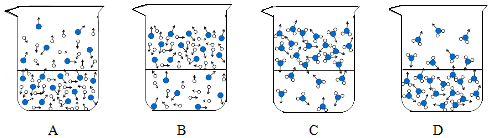
(1)下列图示能反映水在空气中放置时发生变化的微观示意图是 (填字母序号)
(图中  表示氧原子,○表示氢原子)
表示氧原子,○表示氢原子)
(2)石灰水在空气中久置后有浑浊现象,写出该反应的化学方程式 。
(3)为研制一种安全、环保的除湿剂,可选择上表中的 (填溶质的化学式)。
(4)将10.00g氯化钠浓溶液敞口久置后,最终得到2.26g晶体,则该溶液是 (填"饱和"或"不饱和")溶液。(已知该温度下氯化钠的溶解度为36.1g)
(5)为进一步研究稀盐酸敞口久置后浓度变化,该小组开展如下探究。
①甲同学猜想浓度可能会变大,理由是 。
②为验证甲同学的猜想是否正确,设计实验方案: 。
(6)乙同学取20%的氢氧化钠溶液20.00g,敞口放置一段时间后部分变质,得到18.80g溶液,由此能否计算所得溶液中溶质组成?若能,请计算其组成;若不能,请补充完成实验方案设计,同时说明需要测定的数据(用a表示),并计算a的取值范围。(不要求写出计算过程)
家中蒸馒头用的纯碱中含有氯化钠,某实验小组要测定该纯碱中碳酸钠的质量分数。取6 g纯碱样品放入烧杯中,逐滴加入稀盐酸至不再产生气泡,此时烧杯中没有不溶物,其消耗稀盐酸61.7 g,测得反应后溶液的质量为65.5 g。请帮助实验小组完成以下计算:
(1)样品中碳酸钠的质量分数是多少?(计算结果保留至0.1%)
(2)反应后溶液中溶质的质量分数是多少?
黄铜的颜色与黄金相似,在生活中常常误认为黄金。兴趣小组为探究某黄铜(铜锌合金)中锌的含量,向10.0g该黄铜中加稀硫酸,测得实验数据如图所示。以下分析错误的是( )
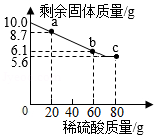
A.a点时,锌有剩余
B.c点时,硫酸没有完全参与反应
C.该黄铜中锌的质量分数为44%
D.所用稀硫酸的溶质质量分数为8.29%
某氯化钙样品中可能混有氯化铁、氯化镁、氯化钠、碳酸钠中的一种或几种物质。取该样品11.1 g溶于适量水中,得到澄清的无色溶液,然后向其中加入足量的硝酸银溶液,得到29.7 g白色沉淀,则该样品组分的下列推断中,正确的是
| A.既无氯化铁,也无碳酸钠 |
| B.只有氯化镁,没有氯化钠 |
| C.肯定有氯化镁,可能有氯化钠 |
| D.肯定有氯化镁,也肯定有氯化钠 |
实验室有甲乙两瓶久置的氢氧化钠固体,某学习小组为了研究其变质情况,进行了如下实验:(电子秤示数单位为克)

(1)滴入紫色石蕊试液后溶液为红色,说明反应后溶液呈 性。
(2)上述实验中产生的二氧化碳气体质量为 克。
(3)计算甲瓶固体样品中碳酸钠的质量分数。
(4)某同学另取10克乙瓶中的固体样品,用100克15%的稀硫酸按同样方法进行实验,他认为不管固体样品变质程度如何,稀硫酸加入后,都不需要使用石蕊试液,请计算说明他做出此判断的原因。
下列四个图象分别对应四个变化过程,其中正确的是( )
| A. |
|
| B. |
|
| C. |
|
| D. |
|
下列图像能正确反应其对应关系的是( )
A.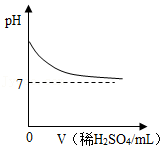 表示向一定质量的Ba(OH)2溶液中逐滴加入稀H2SO4至过量
表示向一定质量的Ba(OH)2溶液中逐滴加入稀H2SO4至过量
B.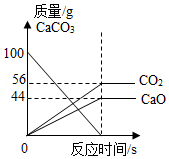 表示发生的反应为:CaCO3
表示发生的反应为:CaCO3 CaO+CO2↑
CaO+CO2↑
C. 表示等质量且过量的锌粉和铁粉,分别与质量和质量分数都相同的稀硫酸反应
表示等质量且过量的锌粉和铁粉,分别与质量和质量分数都相同的稀硫酸反应
D. 表示向盛有MnO2的烧杯中加入H2O2溶液
表示向盛有MnO2的烧杯中加入H2O2溶液
某氯化钠溶液中含有氯化镁(MgCl2),学习小组为测定其中氯化镁的质量分数,在50.0g该溶液中加入50.0g氢氧化钠溶液恰好完全反应,经测定生成沉淀的质量为2.9g。请回答下列问题:
(1)反应后溶液的质量为 g;
(2)求原氯化钠溶液中氯化镁的质量分数(写出计算过程)。
一定质量M、N两种金属,分别与相同质量和相同质量分数的稀硫酸反应,生成氢气的质量与反应时间的关系如图所示。分析图象得到的以下结论中,不正确的是( )

A.两种金属的活动性:M>N
B.两种金属生成氢气的质量:M=N
C.两种金属消耗稀硫酸的质量:M=N
D.充分反应后,得到溶液的质量:M=N
金属在生产、生活和社会发展中应用较为广泛,中国制造,让世界瞩目!
(1)航天:我国用长征三号乙运载火箭成功发射第55颗北斗导航卫星,化学材料在其中起到了重要作用,铝合金和钛合金被广泛用于航天工业、一般情况下,铝合金的强度和硬度比纯铝 (填“高”或“低”)。
(2)交通:制造港珠澳大桥需要大量的钢铁,请写出一种防止钢铁生锈的方法: 。
(3)冶炼:我国湿法炼铜很早就有记载,东汉《神农本草经》曾记载石胆“能化铁为铜”。向硝酸铜和硝酸银的混合溶液中加入一定量的镁粉,充分反应后过滤,滤液呈蓝色,则滤出的滤液中一定含有金属离子是 。
(4)应用:随州编钟被誉为“世界第八大奇迹”,代表了我国古代青铜工艺的较高水平,青铜是铜锌合金。现有铜锌合金质量20克,与100克质量分数为19.6%的稀硫酸恰好完全反应,则铜锌合金中铜的质量分数为 。
在两只烧杯中分别放入相同质量的镁、锌两种金属,然后向两只烧杯中分别倒入相同质量、相同质量分数的稀硫酸,反应产生氢气的质量与消耗硫酸的质量关系见图。综合以上信息得到以下结论,合理的是( )

A.从图象可以看出,金属镁比金属锌的活动性强
B.若两种金属都有剩余,二者得到的氢气质量相同
C.若硫酸有剩余,二者得到氢气的质量相同
D.若两种金属完全溶解,二者消耗硫酸的质量相同
中国古代四大发明之一的"黑火药"是由木炭(C)、硫粉(S)和硝酸钾(KNO 3)按一定比例混合而成。
(1)分类。下列关于"黑火药"说法正确的是 。
a."黑火药"由"黑火药分子"构成
b."黑火药"中的KNO 3属于复合肥料
c."黑火药"中的C、S不再保持各自的化学性质
(2)变化。"黑火药"爆炸时发生的主要反应是:S+2KNO 3+3C═K 2S+N 2↑+3 ↑。
①依据质量守恒定律,空格上缺少的物质是 (填化学式)。
②"黑火药"爆炸时能闻到刺鼻的火药味,是因为爆炸时除了有硫化物,还有硫的氧化物生成。硫在空气中燃烧的化学方程式为 。
(3)制备。古代曾用硝土(含有Ca(NO 3) 2、少量NaCl等)和草木灰(含有K 2CO 3)作原料制取KNO 3.某化学兴趣小组设计了如图实验流程:
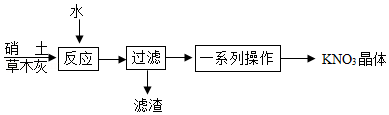
①"反应"过程中的化学方程式为 。
②"过滤"操作必须用到的玻璃仪器有烧杯、玻璃棒和 。
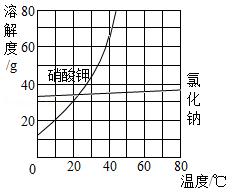
③如图是硝酸钾和氯化钠的溶解度曲线。"一系列操作"包括"加热蒸发浓缩、再冷却到一定温度、过滤"等步骤。其中"冷却到一定温度"能获得纯度较高的硝酸钾晶体的原因是 。
(4)发展。现代国防、开矿等使用的烈性炸药,主要成分为硝化甘油(C 3H 5O 9N 3)。
①硝化甘油在人体内能缓慢氧化生成一种氮的氧化物,用于治疗心绞痛。该氧化物中氮为+2价,其化学式为 。
合成硝化甘油的化学方程式为C 3H 8O 3+3HNO 3═C 3H 5O 9N 3+3H 2O.现用46kg甘油(C 3H 8O 3)和足量硝酸反应,理论上能生成多少硝化甘油?(写出计算过程)
下面是同学们在复习中梳理得到的一组图象,其中图象与实验描述一致的是( )
A. 将氢氧化钡溶液逐滴滴入稀硫酸中至过量
将氢氧化钡溶液逐滴滴入稀硫酸中至过量
B.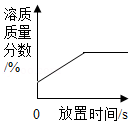 浓硫酸敞口放置一段时间
浓硫酸敞口放置一段时间
C.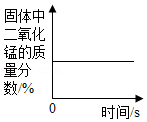 加热一定量氯酸钾和二氧化锰固体的混合物
加热一定量氯酸钾和二氧化锰固体的混合物
D. 等质量的镁、铁分别与溶质质量分数相等且足量的稀硫酸反应
等质量的镁、铁分别与溶质质量分数相等且足量的稀硫酸反应
在相同质量、相同质量分数的稀硫酸中,分别加入足量的Mg、Fe、Zn三种金属,其发生反应的质量关系如图所示,读识如图并判断,下面推理合理的是( )
①反应速率:Mg>Fe>Zn
②反应生成氢气质量:Mg=Fe=Zn
③反应后溶液质量:Mg=Fe=Zn
④反应后溶液溶质质量分数:Mg<Fe<Zn。

A.①②B.③④C.①③D.②④
试题篮
()