某石化厂有一种石油产品中含有质量分数为4.9%的残余硫酸,过去他们都是用
溶液来清洗这些硫酸.现在石化厂进行了技术改造,采用
中和这些残余硫酸.则每处理100
这种石油产品,可以节约经费多少?
和
市场价格如下表:
| 名称 |
||
| 价格(元/
) |
6.00 |
24.00 |
| A. |
73.8元 |
B. |
72元 |
C. |
51.6元 |
D. |
22.2元 |
有Fe2O3、CuO、ZnO组成的混和物与足量的CO高温反应,将反应产生的气体通入足量的澄清石灰水中,得沉淀质量为50.0g,金属混合物的质量为24.1g,原固体混合物的质量为( )
| A.32.1g | B.35.9 g | C.40.1g | D.74.1g |
KMnO4和MnO2混合物中,K%为15.6%。取10g混合物,加热至完全反应,则剩余固体质量为
| A.5.68g | B.6.32g | C.8.99g | D.9.36g |
在一个密闭容器中放入M、N、Q、P四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表,则关于此反应认识不正确的是
| 物 质 |
M |
N |
Q |
P |
| 反应前质量(g) |
18 |
1 |
2 |
32 |
| 反应后质量(g) |
X |
26 |
2 |
12 |
A.反应后物质M的质量为l3g B.该变化的基本反应类型是分解反应
C.反应中N、P的质量比为5:4 D.物质Q可能是该反应的催化剂
在加热条件下,向装有10 的硬质玻璃管中通入 一段时间,最终玻璃管中剩余固体8.4 .则下列说法正确的是
| A. | 与 反应, 是过量的 |
| B. | 反应生成 的质量为8.4 |
| C. | 反应生成 的质量为1.6 |
| D. | 参加反应的 占原总质量的80% |
在一个密闭容器内有四种物质,在一定条件下充分反应后,测得反应前后各物质的质量如下:
| 物质 |
X |
Y |
Z |
Q |
| 反应前质量/g |
4 |
10 |
1 |
21 |
| 反应后质量/g |
0 |
12 |
15 |
待测 |
且X的相对分子质量为n,Q的相对分子质量为2n,则下列推理正确的是( )
A.反应物是Y和Z,生成物是X和Q
B.反应后生成15gZ
C.参加反应的Y与Q的质量比是1:1
D.该反应方程式中X与Q的化学计量数比为2:3
现有18.6g NaOH与Na2CO3的固体混合物,测得其中钠元素与碳元素的质量比为23:3。在室温下,将该混合物与100g稀硫酸混合,恰好完全反应,所得不饱和溶液的质量为114.2g,则原固体混合物中含有钠元素的质量为
| A.2.3g | B.9.2g | C.4.6g | D.6.9g |
两份质量相同的碳酸钙,第一份加热使其完全分解,第二份加入足量的稀盐酸充分反应,则它们生成的二氧化碳的质量是
| A.第一份多 | B.两份一样多 | C.第二份多 | D.无法确定 |
一定质量的木炭在氧气和氮气的混合气体的密闭容器中燃烧产生CO和CO2,且反应后测得混合气体中碳元素的质量分数为24%,则其中氮气的质量分数不可能为
| A.10% | B.20% | C.30% | D.40% |
为了测定液化气中丙烷(C3H8)在氧气不足时的燃烧产物,将一定量的丙烷和氧气置于一个封闭的容器中引燃,测得反应前后各物质的质量如下表
| 物质 |
丙烷 |
氧气 |
水 |
二氧化碳 |
X |
| 反应前质量/g |
4.4 |
12.8 |
0 |
0 |
0 |
| 反应后质量/g |
0 |
0 |
7.2 |
4.4 |
a |
下列判断正确的是
A.X可能含有氢元素 B.X可能是该反应的催化剂
C.表中a的值为5.6 D.X只含碳元素
为测定某石灰石样品中碳酸钙的质量分数,取2.0g石灰石样品于烧杯中,将20g稀盐酸分4次加入样品中,充分反应后经过滤,干燥、称重,得实验数据如表:
第一次 |
第二次 |
第三次 |
第四次 |
|
稀盐酸的用量/g |
5.0 |
5.0 |
5.0 |
5.0 |
剩余固体的质量/g |
1.5 |
1.0 |
0.5 |
0.3 |
已知石灰石中的杂质既不与盐酸反应,也不溶解于水。下列说法正确的是( )
A.第三次实验后碳酸钙无剩余
B.第四次实验后盐酸无剩余
C.盐酸中HCl的质量分数是3.65%
D.样品中碳酸钙的质量分数是85%
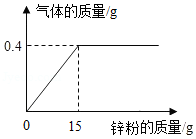
向133.4克稀盐酸中加入锌粉(仅含不溶于酸的杂质),所加锌粉的质量与产生气体的质量的关系如图所示。求:
(1)此过程产生气体的最大质量是 ;
(2)原稀盐酸中溶质的质量分数为多少?(请写出计算过程)
某金属单质 X与非金属单质Y可发生反应:2X+Y=X2Y.某实验探究小组进行了两次实验,测得数据如下表:
| 实验序号 |
X的用量/g |
Y的用量/g |
生成X2Y的质量/g |
| 1 |
7.4 |
1.6 |
8.0 |
| 2 |
9.6 |
3.2 |
12.0 |
参加反应的X与Y的质量比为
A.4:1 B.3:1 C.2:1 D.37:8
天平两边各放质量相等的烧杯,分别盛有100克溶质质量分数为9.8%的稀硫酸,此时天平平衡。若将下列各组的两种物质分别加入左右两烧杯中,充分反应后,天平仍平衡的是
| A.铜8克,氧化铜8克 |
| B.氯化钡溶液10克,氢氧化镁5克 |
| C.氧化铜4克,碳酸镁8.4克 |
| D.铁5克,铝5克 |
将相同状态的铁和镁分别与相同质量分数,足量的稀盐酸反应,产生氢气的质量与反应时间的关系如图所示,下列说法正确的是
| A.铁和镁的质量相同 |
| B.甲是铁、乙是镁 |
| C.铁和镁完全反应所消耗的稀盐酸质量相同 |
| D.反应后溶液的质量均减少 |
试题篮
()