垃圾分类就是新时尚。目前,践行“新时尚”的垃圾分类工作已在全国地级及以上城市全面启动。
(1)生活垃圾可分为可回收垃圾、餐厨垃圾、有害垃圾等。
①空饮料瓶、废旧报纸应放置于贴有标志 (填字母序号,下同)的垃圾箱中。
②废旧电池中含有铅、镉、汞等有害金属,如果将其随意丢弃,这些金属渗出会造成土壤及 污染,威胁人类健康,应将其放入废旧电池专用收集箱。
③餐厨垃圾是生活垃圾的主要来源。下列有关说法合理的是 。
A.餐厨垃圾沥干水分后放入家用垃圾袋
B.部分餐厨垃圾可作为沼气池中发酵的原料
C.外出就餐提倡“光盘行动”
(2)垃圾是“放错了地方的资源”。
①部分废旧塑料具有 (选填“热塑”或“热固”)性,可反复加工再利用。
②某化学兴趣小组从工厂收集到一份金属废料,可能含有Al、Zn、Fe、Ag四种金属中的一种或几种,为测定其组成,便于回收利用,现取样向其中加入一定质量的CuSO4溶液。
Ⅰ.充分反应,得到无色溶液及少量固体剩余物,且反应前后溶液的质量相等。该金属废料中一定含有 (填元素符号)。
Ⅱ.将Ⅰ中少量固体剩余物置于试管中,加入足量稀盐酸充分反应, (选填“一定有”、“可能有”或“一定没有”) H2生成。
③建筑工地废弃的大理石边角料(主要成分为CaCO3,杂质不参加反应)可用于制备轻质碳酸钙(常用作牙膏中的摩擦剂)。已知:CaCO3 CaO+CO2↑

Ⅰ.操作a的具体步骤包括 、洗涤、干燥。
Ⅱ.计算10g大理石边角料理论上最多得到轻质碳酸钙的质量(写出计算过程)。

某同学用质量分数为15%的稀硫酸处理某造纸厂含NaOH的碱性废水样品:
(1)用9.2g质量分数为98%的浓硫酸能配制上述稀硫酸 g(计算结果保留整数)。
(2)若上述造纸厂废水75g能与9.8g 15%的稀硫酸恰好反应(设只发生NaOH与硫酸的反应),试计算该废水中NaOH的质量分数(写出计算过程,结果精确到0.1%)。
CO2是最主要的温室气体,也是巨大的碳资源,CO2的低能耗捕集、转化和利用正受到世界各国的广泛关注。
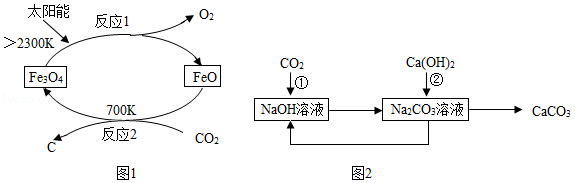
(1)以CO2为原料制取炭黑的太阳能工艺如图1所示。
①反应1的基本类型为 。
②反应2中碳元素的化合价 (填“升高”“不变”或“降低”)。
(2)利用NaOH溶液吸收CO2,部分转化关系见图2。
反应①的化学方程式为 ,该转化中循环使用的物质是 。
(3)利用Na2CO3或K2CO3溶液吸收低浓度的CO2,将其转化为NaHCO3或KHCO3,NaHCO3或KHCO3受热分解生成高浓度的CO2储存利用,生成的Na2CO3或K2CO3循环使用以降低生产成本。
吸收剂 |
Na2CO3 |
K2CO3 |
20℃最高浓度(g/L) |
212 |
1104 |
价格(元/Kg) |
1.25 |
9.80 |
根据表中信息,选择K2CO3溶液作吸收液的优点是 。
(4)利用一种新型“人造树叶”将CO2转化为乙醇(C2H5OH)的反应如下:2CO2+3H2O C2H5OH+3O2,研究显示,1L“人造树叶”每天能从空气中吸收968g CO2,计算1L“人造树叶”工作1天可得到乙醇的质量(写出计算过程)。
(5)某研究小组设计如图3所示实验,探究CO2和H2在一定条件下反应的产物。
查阅资料:①CO2和H2在合适催化剂和一定温度下反应转化为CO和H2O;
②白色无水硫酸铜吸水后变为蓝色。
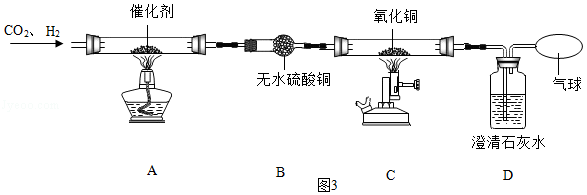
实验过程中观察到的主要现象有:B装置中白色固体变为蓝色,C装置中黑色固体变为红色,D装置中澄清石灰水变浑浊。
①设计B装置的目的是 。
②C装置中发生的反应的化学方程式为 。
③研究小组反思后认为,根据上述实验现象不能确认CO2和H2反应生成了CO,理由是 。
硼及其化合物在现代工农业、医学、国防中有着重要的应用价值。利用硼镁矿可制备硼,工艺流程如图所示。请回答下列问题:

(1)B2O3中B元素的化合价为 。
(2)为加快硼镁矿石与浓NaOH溶液的反应速率,可采取的措施是 ;回收副产物Mg(OH)2可制得流程 的反应物。
(3)H3BO3加热分解只生成两种氧化物,流程②的化学反应方程式为 。
(4)根据流程③的化学反应方程式:B2O3+3Mg 2B+3MgO,理论上制备1.1吨的硼,需消耗镁多少吨写出计算过程)?
南通滨临长江,将长江水净化处理可成为居民生活用水。
(1)水净化时先加入絮凝剂,沉降过滤后,通过活性炭。活性炭的作用是 。
(2)将硬水通过如图所示的阳离子交换柱后可变成软水(图中阴离子未画出),交换后的水仍然呈电中性。
①一个Ca2+可以交换出 个Na+。
②阳离子交换柱长时间使用后,Na+变少,失去硬水软化功能而失效。利用生活中常见物质检验阳离子交换柱已失效的方法是 。
(3)二氧化氯(ClO2)可用于饮用水的杀菌消毒。取100mL经ClO2消毒后的饮用水于锥形瓶中,调节溶液至弱碱性,加入足量KI充分反应,测得生成I2的质量为0.0254mg。上述过程中发生的反应为2ClO2+2KI═2KClO2+I2,其他物质不参与反应。计算该饮用水中ClO2的残留量(以mg/L计),在答题卡上写出计算过程。

我国塑料购物袋的年消耗量很大,废弃塑料的处理亟待解决。回答下列问题。
(1)购物袋等塑料制品的大量使用,可能会造成的一种环境污染是 。
(2)小林尝试用焚烧法对某类塑料购物袋(主要成分是聚氯乙烯)进行处理,并将燃烧产物用氢氧化钠溶液进行吸收。
【查阅资料】Ⅰ.聚氯乙烯的化学式为(C2H3Cl)n。
Ⅱ.氯化氢气体会污染环境
Ⅲ.Na2CO3+CaCl2═CaCO3↓+2NaCl
①聚氯乙烯完全燃烧的化学方程式如下:
2(C2H3Cl)n+5nO2 4nCO2+2nHCl+2nX,则X的化学式为 。
②将完全燃烧后的产物,全部通入到一定量的NaOH溶液中,得到吸收液,写出氢氧化钠溶液吸收氯化氢的化学方程式 。
③小林对吸收液的溶质成分产生了兴趣,进行如下探究:
[提出问题]吸收液中溶质的成分是什么?
[进行实验1]取吸收液少许置于试管中,滴加2~3滴无色酚酞试液,发现酚酞变红色,说明溶液呈 性。
[猜想]猜想1:NaCl、NaOH、Na2CO3
猜想2:
猜想3:NaCl、Na2CO3、NaHCO3
猜想4:NaCl、NaHCO3
[进行实验2]向实验1所得溶液中,加入过量的CaCl2溶液,小林观察到 (填实验现象),最终得出结论:猜想1正确。
[交流反思]实验结束后,小林对吸收液进行无害化处理,其方案是 ,然后倒入废液缸。
咨询老师后,小林获悉废弃塑料的资源化回收是减少环境危害的最好方法。
(3)聚氯乙烯的生产需要用到氯气。工业上获取氯气的方法是电解饱和食盐水,发生反应的化学方程式为:2NaCl+2H2O 2NaOH+H2↑+Cl2↑.某工厂需生产14.2t氯气(Cl2),至少需要氯化钠的质量为多少?(请写出计算过程)
为了测定某小苏打样品中碳酸氢钠的质量分数,小兰同学进行了如下实验:向盛有10g样品的烧杯中加入稀硫酸,恰好完全反应时,加入稀硫酸的质量为90g,反应后烧杯内物质的总质量为95.6g。(杂质不溶于水也不与酸发生反应)
已知反应的化学方程式如下:2NaHCO3+H2SO4═Na2SO4+2CO2↑+2H2O
(1)该反应生成二氧化碳的质量为 g。
(2)求该样品中碳酸氢钠的质量分数(写出计算过程)。
我国著名的化学家侯德榜发明了联合制碱法,大大提高了原料的利用率,其反应原理之一为NaCl+CO2+NH3+H2O═NaHCO3↓+NH4Cl,某化工厂消耗117t氯化钠,理论上可生产碳酸氢钠的质量是多少?
(注:在20℃时,将二氧化碳通入含NH3的饱和NaCl溶液中能生成 NaHCO3晶体和NH4Cl溶液)
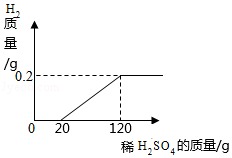
向表面生锈的铁片中滴加稀硫酸,产生氢气的质量与所加稀硫酸的质量关系如图所示,请回答:
(1)从图中可以看出完全反应后产生氢气的质量为 g。
(2)求所加稀硫酸中溶质的质量分数。(写出计算过程,计算结果精确到0.1%)
国家明令禁止在面粉生产中添加过氧化钙(CaO2)等食品添加剂。过氧化钙是一种安全无毒物质,常带有结晶水,广泛用于果蔬保鲜、空气净化、污水处理等方面。某化学兴趣小组为测定某过氧化钙样品(CaO2•xH2O)中的结晶水,称取4.86g过氧化钙样品,灼热时发生如下反应:
2[CaO2•xH2O] 2CaO+O2↑+2xH2O
完全反应冷却后称量,得到剩余固体的质量为3.36g。
(1)反应中生成O2的质量是 g。
(2)计算样品CaO2•xH2O中的x值(写出详细的计算过程)。
某化学兴趣小组的同学进行了如图所示实验。

请根据图示信息计算:
(1)实验中产生氢气的质量是 g。
(2)实验中所用稀硫酸溶质的质量分数是多少(要求书写计算过程)?
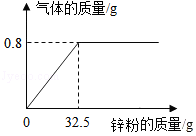
向一定量的稀硫酸中加入锌粉(仅含不溶于酸的杂质),所加锌粉的质量与产生气体的质量的关系如图所示。求:
(1)此过程中产生氢气的最大质量是 克。
(2)锌粉中锌的质量分数为多少。(请写出计算过程)
小华同学发现自家的水壶用久以后底部会附着一层白色固体,查阅资料后得知,水在加热或长久放置时,溶于水中的可溶性钙和镁的化合物会生成沉淀(水垢),于是他邀请同学小雪进行了以下实验探究。
探究一:自家的井水是软水还是硬水?
取少量井水样品于试管中,加入 ,振荡,出现大量浮渣,由此得出结论:自家的井水属于 。
探究二:白色固体的主要成分是什么?
[假设与猜想]猜想Ⅰ:CaCO3。
猜想Ⅱ: (填化学式)。
猜想Ⅲ:CaCO3和Mg(OH)2。
[实验与探究]取少量白色固体样品(不考虑杂质和微溶物对实验的影响)于试管中,向其中加入足量稀盐酸,白色固体溶解,有 产生,根据以上现象,小华认为:猜想Ⅰ正确。小雪认为小华的结论不严谨,理由是 。经过两人反复讨论,进一步设计了如下实验。
实验步骤 |
实验现象 |
实验结论 |
取上述实验中的上层清液于试管中,滴加足量NaOH溶液 |
无明显现象 |
猜想Ⅰ成立 |
|
猜想Ⅲ成立 |
[拓展与迁移]取含有MgCl2和HCl的混合溶液165.8g于烧杯中,向其中缓慢加入200g溶质质量分数为8%的NaOH溶液,恰好完全反应后过滤得到沉淀和滤液,其中滤液的质量为360g。请计算:
(1)生成沉淀的质量是 克。
(2)原混合溶液中,MgCl2的质量是多少?(请写出具体的计算过程,下同)
(3)恰好完全反应时,所得溶液的溶质质量分数是多少?(结果保留至0.1%)
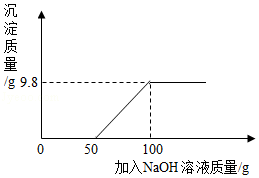
某学校化学实验室有一杯含盐酸和氯化铜的废液,该校化学兴趣小组的同学取109.8g废液于烧杯中,向其中逐滴加入一定溶质质量分数的氢氧化钠溶液,所加氢氧化钠溶液与生成沉淀的质量关系如图所示:
试计算:
(1)产生沉淀的总质量是 克;
(2)109.8g废液中氯化铜的质量是 克。
(3)计算加入100g氢氧化钠溶液并充分反应后烧杯内所得溶液中溶质的质量分数。
试题篮
()