某研究小组欲检验草酸晶体样品分解产物并测定器质量分数(假设杂质不参与反应)。草酸晶体( H2C2O4•2H2O)的理化性质见表。
| 熔点 |
沸点 |
热稳定性 |
与澄清石灰水反应 |
| 101°C~102°C |
150°C~160°C升华 |
100.1°C失去结晶水,175°C分解成CO2,CO,H2O |
与Ca(OH)2反应产生白色沉淀(CaC2O4) |
(1)加热分解草酸晶体最适宜的装置是____________(填图1字母序号)。
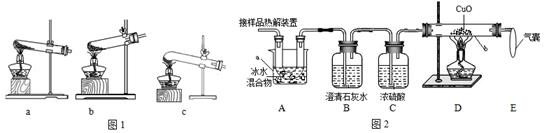
(2)图2是验证热分解产物中含CO,CO2的装置
①仪器a和b的名称分别是____________和____________。
②证明存在CO2的现象是________________________,证明存在CO的现象____________,D中反应的化学方程式是_____________。
③装置A的作用是____________________,气囊的作用是________________________。
(3)为测定样品中草酸晶体的质量分数,设计两种如下方案。
①称一定量样品用上图装置进行实验,测得装置D反应前后的质量差,由此计算出的实验结果比实际值偏低,排除仪器和操作的因素,其原因可能有:CO未完全反应、___________________________。
②称取8.75g草酸晶体样品配制50.00g溶液,取10.00g溶液加适量的稀硫酸,然后滴加25.00g3.16%KMnO4溶液,恰好反应完全。
(已知:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O)则KMnO4溶液显____________色,25.00g3.16%KMnO4溶液中KMnO4的质量____________g。样品中草酸晶体的质量分数为____________。
【Mr(H2C2O4)=90,Mr(H2C2O4•2H2O)=126,Mr(KMnO4)=158】。
实验小组欲测定双氧水中过氧化氢的物质的量。
【设计原理】将一定质量的双氧水样品与二氧化锰混合,测定反应产生的氧气的质量,再通过方程式计算,得到过氧化氢的量。(“碱石灰”是氧化钙和固体氢氧化钠的混合物,极易吸收水蒸汽)
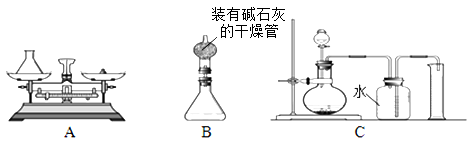
【过程方法】
(1)组长首先设计(如图A):向装有样品溶液的锥形瓶中投入二氧化锰,待双氧水完全反应完毕后测得产生氧气的质量是9.6g,则制取氧气为 (13) mol,双氧水中含过氧化氢多少mol?(写出具体计算过程) (14) 。
(2)小林对组长的设计提出质疑,在组长方案的锥形瓶上加一装有碱石灰的干燥管(如图B),然后再操 作,请说明小林质疑的理由是 (15) 。
(3)若用C装置来制取氧气并测得氧气的体积,此处的收集方法是 (16) 法,收集到氧气的体积约等于 (17) 。
6g大理石样品与50g稀盐酸恰好完全反应(杂质不参与反应且不溶于水),生成二氧化碳2.2g。求:反应后溶液中溶质的质量分数(计算结果保留一位小数)。
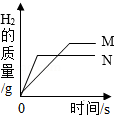
现有相同质量且相同形状的锌和铁两种金属,分别加入足量的溶质质量分数相同的稀硫酸中,产生氢气的质量与反应时间的关系如图所示。
(1)图中M代表 (填“铁”或“锌”)。
(2)请写出锌和铁两种金属中与稀硫酸反应速率较快的化学方程式: 。
一定条件下,CO与MgSO4反应会生成三种氧化物。某兴趣小组用如下装置探究该反应。
已知:SO2,CO2均能使澄清石灰水变浑浊,SO2能与高锰酸钾溶液反应,使高锰酸钾溶液裉色。
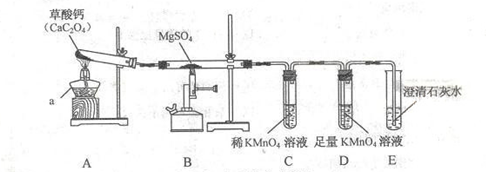
(1)装置A的作用是 。
(2)装置A中CaC2O4的分解会生成一种气体和一种相对分子质量为100的含钙的化合物,则A中反应的反应化学方程式为 。
(3)实验时观察到装置C中紫红色褪去,装置E中溶液变浑浊,则在C和E中反应的气体分别是 ﹑ ;
(4)装置B中反应的化学方程式是 ;
(5)装置D的作用是 ;
(6)实验结束,通过过滤、干燥等操作,兴趣小组同学测得装置E中的白色沉淀质量为2g(过程中损耗忽略不计),则E装置中吸收的二氧化碳质量至少是多少?
(7)该装置存在的明显不足之处是
二氧化氯(ClO2)是安全消毒剂,杀菌能力优于Cl2,可由NaClO2与Cl2反应制得。
(1)配平化学方程式: NaClO2+ Cl2═ ClO2+ NaCl。
(2)71g Cl2完全反应,理论上最多生成ClO2的质量为 g。
CO2的捕集与资源化利用是化学研究的热点。
(1)控制CO2的排放,是为了减缓 效应,加压水洗法可捕集CO2,是因为压强增大时CO2在水中的溶解度 (填“增大”“不变”或“减小”)。
(2)石灰石循环法可用于捕集烟气中的CO2,该方法以CaO捕集CO2,将所得产物在高温下煅烧可重新获得CaO,高温煅烧时反应的化学方程式为 ,生成的CaO疏松多孔,结构与活性炭相似,其在捕集过程中对CO2具有良好的 性。
(3)对CO2气体加压、降温,可获得干冰。从构成物质的微粒视角分析,该过程主要改变的是 。干冰能用于人工降雨,是因为 。
(4)CO2可用于食品保鲜,实验测得气体中CO2的体积分数与溶液pH的关系如图1所示。
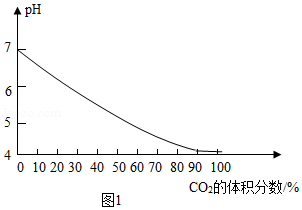
①气体中CO2体积分数增大时,造成图示变化的主要原因是溶液中 浓度增大(填化学式)。
②智能化食品包装通过颜色变化显示包装内CO2气体含量的变化,举出一种可通过颜色变化用于该智能化包装的物质 。
(5)已知一定条件下CO2与H2以质量比11:2反应可生成CH4.与该反应类似,不同条件下,CO2与H2反应也能生成甲醇(CH4O)。生成甲醇时参加反应的CO2与H2的质量比 。
(6)为研究某公园中植物与大气间的碳交换,对该公园一年内每天的气温及光合有效辐射进行测量,结果见图2和图3.通过测量其一年内每天空气中CO2含量等数据,分析所得碳交换的结果见图4.碳交换以每月每平方米植物吸收或释放CO2的质量表示,正值为净吸收CO2,负值为净释放CO2。

①由如图可推测,影响公园中植物与大气碳交换的因素有 。
②为进一步研究环境因素对公园中植物与大气碳交换的影响,从光合作用的角度出发,还需测量的重要因素是其一年内每天 的变化。
为了分析生铁中铁的含量,某学习小组进行了实验研究,即取6g生铁与10%的盐酸反应,并绘制了加入盐酸质量与放出气体质量的关系图(如图)。说明:生铁中杂质不溶于水,不与盐酸、硫酸铜溶液反应。
(1)铁完全反应用去盐酸的质量为_______g。
(2)生铁中铁的质量分数为多少? (写出计算过程,结果保留到小数点后一位)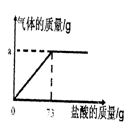
(3)某同学列出了如下计算式:
生铁与盐酸刚好反应完全时所得溶液质量=(73+6 a)g
a)g
小明对该计算提出了质疑,请指出其中的错误______________________________.
硫酸是化学实验室中常用的一种试剂,试回答下列问题:
(1)硫酸的相对分子质量为_________。
(2)配制184g质量分数为19.6%的稀硫酸,需要98%浓硫酸(密度为1.84克/厘米3)多少毫升?
新型材料纳米级Fe粉具有广泛的用途,它比普通Fe粉更易与氧气反应,其制备工艺流程如下图所示: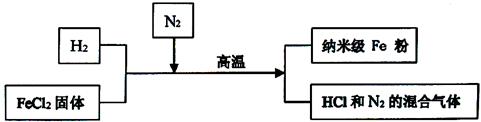
请回答下列问题:
(1)纳米级Fe粉在氧气中能自发燃烧生成黑色固体,此黑色固体的化学式为 。
(2)请补充完成上述制备工艺的化学方程式:H2 +FeCl2  Fe+ 。
Fe+ 。
(3)研究人员发现最后制得的纳米级Fe粉样品中混有少量的FeCl2杂质。
①为除去样品中的杂质,在无氧环境下,先加 溶解,然后再 、洗涤、烘干.
②取样品20g,加入足量的盐酸,生成氢气0.7g。请计算该样品中单质Fe的质量分数。
(请写出计算过程)____ 。
实验室里,常采用加热高锰酸钾或分解过氧化氢的方法制氧气。
(1)高锰酸钾属于 (填"酸"、"碱"或"盐"),用它制氧气的化学方程式是 。
(2)高锰酸钾制氧气的实验中,不需要使用的一组仪器是 (填序号)。
a.烧杯 玻璃棒
b.大试管 集气瓶
c.酒精灯 铁架台
d.导管 单孔塞
(3)利用化学方程式计算,制取4.8g氧气,至少需要过氧化氢的质量是多少?
73g盐酸与足量锌粒反应,生成的气体在标准状况下的体积为4.48L.(在标准状况下,氢气的密度为0.0899g/L)
(1)生成的气体的质量为 (结果保留1位小数)。
(2)计算盐酸中溶质的质量分数(写出计算过程)。
氧气是人类无法离开的物质。
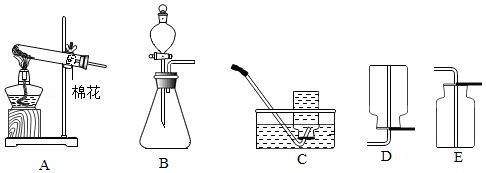
(1)工业上常采用分离液态空气的方法获取O2.能说明空气中存在氧气的事例有 (写一点即可)。
(2)实验室用双氧水和二氧化锰制取并收集氧气,可选择的装置组合是 。
(3)高锰酸钾制取O2时,常用 (填仪器名称)提供热源;现制取3瓶氧气,集气瓶容积为250mL,需要高锰酸钾的质量至少为 g(通常氧气的密度约为1.34g/L,结果精确到0.1g)。
(4)某些空气净化剂含超氧化钾,其净化原理为:4KO2+2CO2═2K2CO3+3O2.该方法一般不用于实验室制取氧气的原因是 (写一点即可)。
某同学在实验室里制取CO2和验证CO2的某些性质,根据如图回答问题.
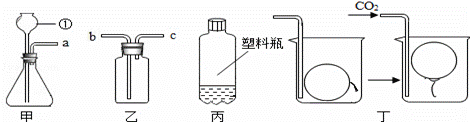
(1)写出图中仪器①的名称:______________;
(2)装置甲中应添加固体试剂的名称是____________,12.5g该固体(碳酸钙的质量分数为80%)最多可制得 g CO2气体;
(3)装置甲中发生反应的化学方程式为 _________________________ ;
(4)用装置乙收集CO2时,导管口a应与 _________ (填“b”或“c”)相连;
(5)用图丙所示的质地较软的塑料瓶收集满CO2,再倒入约1/3体积的紫色石蕊试液,立即旋紧瓶盖,振荡,观察到的现象① ② ;
(6)往图丁的烧杯内缓缓通入CO2,超薄材料做成的内充空气的气球会慢慢浮起,由此得出CO2具有的性质是 。
按下列要求各写一个化学方程式(1分×4=4分)
(1)实验室用固体混合物制氧气
(2)高炉中炼铁的原理
(3)用纯碱制烧碱
(4)波尔多液不能用铁制容器盛装
试题篮
()