(8分) “侯氏制碱法”制得的纯碱(Na2CO3)中常含有少量氯化钠。某化学兴趣小组的同学拟测定某纯碱样品中Na2CO3的质量分数。
【方案一】沉淀分析法(如下图所示)。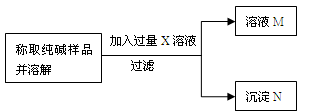
(1)溶液M含有的溶质是CaCl2和 ;沉淀N的化学式是 。
【方案二】气体分析法
称取该纯碱样品21.5g,加入到盛有150 g的稀盐酸的烧杯中,样品完全反应后,测得烧杯内混合物的质量为162.7 g。
(2)写出实验室检验反应中生成气体的化学方程式: 。
(3)求该纯碱样品中Na2CO3的质量分数。(写出具体计算过程) 。
(4)假如称量准确,通过计算得到的纯碱样品中Na2CO3的质量分数比实际数值偏小,你认为其中可能的原因是 。
为探究酸碱盐之间的反应,小红同学做了以下实验:在稀硫酸中加入了一定量的硝酸钡溶液。请回答:
(1)观察到的实验现象是 ,反应的化学方程式为 ,分析实验现象,溶液中减少的离子是 (写离子符号)。
(2)小红同学在稀硫酸中加入硝酸钡溶液时,硝酸钡溶液可能过量,检验溶液中含有少量
硝酸钡的方法是 。
(3)在98g质量分数为10%的稀硫酸中加入100g硝酸钡溶液,恰好完全反应,所加硝酸钡溶液中溶质的质量分数是 (计算结果精确到0.1%)。
(4)若要配制98g质量分数为10%的稀硫酸,需要质量分数为98%的浓硫酸(密度为
1.84g/cm3) mL(计算结果精确到0.1)。在实验室用浓硫酸配制稀硫酸的主要步骤有:计算、 、混匀、冷却至室温装瓶,并贴上标签。
氢氧化钠固体如果密封不严,会发生变质,为探究学校实验室内某瓶氢氧化钠固体
变质情况,化学兴趣小组进行了如下实验:
(1)取少量该瓶固体样品置于试管中,向其中加入一种无色溶液,发现有气泡产生,该小组确定氢氧化钠已经变质,那么该小组同学加入的无色溶液可能是
(2)为了继续探究氢氧化钠的变质程度,该兴趣小组同学取了10g样品,溶于足量水配成溶液,然后向溶液中滴加含足量氢氧化钙的溶液,恰好得到1g沉淀和500g溶液,请计算出最后所得溶液中溶质的质量分数为多少?(计算结果精确至0.1%)
过氧化钠(Na2O2)是一种淡黄色固体。在一次科技活动中,某化学兴趣小组的同学将包有Na2O2固体的棉花放入了如图1的实验中,发现了高低不同的两根蜡烛,下面的蜡烛先熄灭,上面的蜡烛后熄灭;同时也惊奇地发现棉花燃烧了起来。
(1)实验过程中“下面的蜡烛先熄灭,上面的蜡烛后熄灭”的现象说明二氧化碳具有
、 的性质。
(2)棉花为什么会燃烧呢?小组同学认为棉花要燃烧,除了满足“棉花是可燃物”这一条件,还另需满足a: 、 b: 两个条件。
[提出问题]:在上述实验中是如何给棉花提供a和b这两个燃烧条件的呢?
[查阅资料]:1、在常温下Na2O2和CO2能发生化学反应。
2、无水硫酸铜为白色固体,吸水后变为蓝色。
[设计实验]:经过讨论后,小组同学设计了如下图2的实验进行探究。
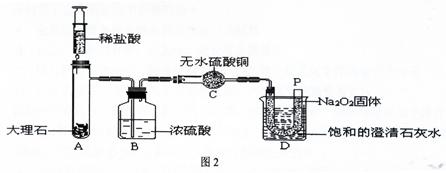
[实验步骤]:①检查整套装置的气密性;②把相关的试剂放入对应的仪器内(D装置的U型管内放有足量的Na2O2固体,烧杯内盛有饱和的澄清石灰水),并按图2组装整套实验仪器;③用力推动针筒的活塞,把稀盐酸注入试管内;④一段时间后,在P处放置一根带火星的小木条,观察现象。
注:整个实验中不考虑稀盐酸的挥发和空气对实验的影响。
[实验现象]:①无水硫酸铜没有变蓝色;②带火星的小木条复燃;③饱和的澄清石灰水变浑浊。
[实验分析]:①浓硫酸的作用是: 。
②D装置的烧杯内澄清石灰水变浑浊的原因是 。
[得出结论]:①“小木条复燃”说明Na2O2和CO2反应产生的一种气体,使图1中的棉花满足了燃烧的一个条件;②“饱和的澄清石灰水变浑浊”说明Na2O2和CO2反应将 能转化为热能,使图1中的棉花满足了燃烧的另一个条件。
[拓展提高]:①Na2O2和CO2反应除生成一种气体外,还生成了一种固体,小明认为生成的固体是NaOH,小红认为是Na2CO3,同学们经过思考后认为 同学的猜想是错误的,理由是: 。
②Na2O2和CO2反应的化学方程式是 。
某研究性学习小组设计了测定纯碱(Na2CO3)样品(只含NaCl杂质)中Na2CO3质量分数的实验方案.请回答下列问题:
小资料:碱石灰的主要成分是氢氧化钠和氧化钙的混合物
(1)气体法。
【原理思路】利用Na2CO3与稀硫酸反应产生CO2,通过测量丙装置实验前后的质量得出CO2质量,从而计算碳酸钠的质量分数。(不考虑原装置内空气的影响)
【实验分析】小科同学根据以上思路,设计了如图1的实验装置。
图1
①实验装置乙中盛放的试剂为 ,
其作用是 ;
装置丁中碱石灰的作用是 。(填字母)
A.吸收Na2CO3与稀硫酸反应产生CO2
B.防止外界空气中二氧化碳进入丙中
C.干燥二氧化碳
②实验中如果滴加稀硫酸的速度过快,会导致测得样品中碳酸钠的
质量分数 (填写“偏高”“偏低”或“不变”).
③小明同学认为小科的方案存在问题,即使操作规范下也会造成结果偏低,你
认为他的理由是 ,应该将装置甲中双孔橡
胶塞换成三孔橡胶塞,并增加图2装置,实验结束后缓缓通入一段时间空气,
目的是 ,其中NaOH溶液的作用是 。
图2
(2)沉淀法.
【实验原理】利用碳酸根离子与钙离子结合生成沉淀,通过沉淀的质量而得出碳酸钠的质量分数。
【实验步骤】①用托盘天平称取样品11.0g放入烧杯中,加水使其完全溶解;
②加入过量的CaCl2溶液充分反应。证明CaCl2过量(即Na2CO3已完全反应)的方法是: 静置,向上层清液中滴加 溶液,如果没有白色沉淀生成,证明CaCl2过量;
③过滤、操作X、干燥、称量沉淀的质量为10.0g,操作X的名称是 ,如果缺少此操作会造成碳酸钠质量分数 (填写“偏高”“偏低”或“不变”)。
④通过以上提供的数据计算出样品中碳酸钠的质量分数为 。(写出计算过程,结果保留至0.1%,共3分)
过碳酸钠(Na2CO4)在洗涤、印染、纺织、造纸、医药卫生等领域有大量应用,某化学研究性学习小组设计并完成了如下实验。
【实验目的】测定过碳酸钠样品(含有的杂质不溶于水且不与酸反应)的纯度。
【实验原理】2Na2CO4+ 4HCl → 4NaCl + 2CO2↑+ O2↑+ 2H2O
【实验装置】
【交流与讨论】
①甲同学认为测定产物中O2的体积即可测定样品的纯度。装置②的作用是:(15);装置③的作用是:(16);
②乙同学认为测定产物中CO2的质量(即反应前后装置②的质量差)就可测定样品的纯度。但利用上述实验装置测得CO2的质量并计算样品的纯度,结果会偏高,你认为原因可能是;(17)(填序号)
A.浓盐酸易挥发,产生的氯化氢气体被装置②吸收
B.二氧化碳气体逸出时带出的水蒸气在装置②中冷凝而被吸收
C.装置①、②内空气中的二氧化碳被装置②吸收
③丙同学提出了一种新方案,得到了大家的一致认可:称取样品12.5g,滴加足量浓盐酸至样品反应完全,再将烧瓶中所有的液体蒸发、结晶、烘干,得到0.2mol氯化钠。则该样品的中过碳酸钠的质量分数为多少?(写出计算过程)
某化学兴趣小组对某品牌牙膏中摩擦剂成分及其含量进行探究,查阅资料如下:
1、该牙膏摩擦剂由碳酸钙、氢氧化铝组成;
2、牙膏中其它成分遇到盐酸无气体生成;
3、碱石灰的主要成分为生石灰和氢氧化钠固体。
利用下图所示装置(图中夹持仪器略去)进行实验,充分反应后,测定B中生成的BaCO3沉淀的质量,以确定碳酸钙的质量分数。请回答下列问题: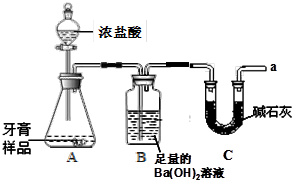
(1)B中反应生成BaCO3的化学方程式是 。
(2)C装置的作用是 。
(3)下列各项措施中,不能提高测定准确度的是 (填序号)。
| A.在加入盐酸之前,应排净装置内的CO2气体 |
| B.滴加盐酸不宜过快 |
| C.在A~B之间增添盛有浓硫酸的洗气装置 |
| D.在A~B之间增添盛有饱和碳酸氢钠溶液的洗气装置 |
(4)有同学认为该装置测定出来的碳酸钙质量分数会偏低,他的理由是
,解决方法是 。
(5)某同学认为不必测定B中生成的BaCO3质量,将B中的Ba(OH)2溶液换成浓H2SO4 ,通过测定C装置反应前后的质量差也可以测定CaCO3的质量分数。实验证明按此方法测定的结果明显偏高,原因是 。
(6)实验中准确称取8.00g样品三份,进行三次测定,测得BaCO3平均质量为3.94g 。请计算样品中碳酸钙的质量分数。(写出计算过程)
2014年12月28日,郑州地铁1号线投入试运营,不但缓解了市内交通压力,也改善了我市空气质量。
I.地铁站里氧气含量的测定
地铁站里氧气的含量应与地面保持一致。现有一瓶从地铁站里收集到的空气样品,康康利用如图实验装置测定样品中氧气的含量。请指出测定时需要注意的事项。(至少3条)
Ⅱ,铁的冶炼
地铁的修建需要大量的钢材。康康用下图装置模拟炼铁的化学原理,请写出反应的化学方程式: 。为了提高CO的利用率,你将怎样改进此装置?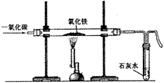
Ⅲ.金属材料在地铁方面的应用 在地铁修建过程中使用了大量的金属材料
(1)地铁入口处的雨篷骨架用铝合金而不用纯铁的原因是 。
(2)钢轨用锰钢的原因是 。
(3)出口处的广告架是金属经焊接而成的,焊条的熔点 (填“>”、“=”或“<”)组成焊条的纯属金属的熔点。
Ⅳ.金属的活动性
康康到工地了解了部分金属材料的防锈问题。技术人员告诉他,采用镀锌钢管做水管时,最好不要用铜质接头。为了探究这三种金属的活动性,康康把等表面积的铁片和锌片放入硫酸铜溶液中(如图所示)。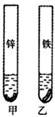
请回答:
(4)如何判断它们是否发生了化学反应?
(5)甲试管中反应前后溶液的质量(填“增重”、“不变”或“减轻”),乙试管中发生反应的化学方程式为 。
(6)上述实验不能够完全证明三种金属的活动性,需要补充的实验操作是 。
Ⅴ.郑州地铁1号线每车次运送乘客约1800人,走同样的路线,CNG公交车每车次消耗天然气akg(以甲烷计算),每辆CNG公交车运送乘客以60名计。若乘CNG公交车的乘客均改乘地铁1号线,则地铁每运行一车次,可减少二氧化碳排放多少千克?
金属材料在国防建设中起着量要的作用,图1为歼﹣15飞机在辽宁舰上起飞
(1)铝合金用于制造飞机的外壳,铝合金材质的主要优点是 、 。
(2)改装前的辽宁舰舰身锈迹斑斑,钢铁的锈蚀主要是铁与空气中的 共同作用的结果,工业生产中常用稀盐酸除去铁制品表面的铁锈,该反应的化学方程式为 。
(3)为了避免轮船的钢质外壳被腐蚀,通常在轮船外壳上镶嵌比铁活动性强金属。小明为探究锌、铁、铜三种金属的活动性顺序,设计了如图2的两个实验:
①实验一中,小明以“金属表面产生气泡的快慢”为标准来判断锌、铁的活动性强弱,有同学认为不够合理,理由是 。
②实验二中,若出现 现象,可证明铁的活动性强于铜,该反应的化学方程式为 。
(4)辽宁舰的建造耗费了大量的钢材.某兴趣小组在实验室用图3所示装置模拟炼铁的化学原理,并测定赤铁矿中氧化铁的质量分数(装置气密性良好,反应完全且赤铁矿中的杂质不参加反应,称量赤铁矿样品的质量为wg)。
①装置A中生成铁的化学方程式为 ,装置B中发生反应的化学方程式为 。
②要测定该赤铁矿样品中氧化铁的质量分数,需要测量的数据是 。
某兴趣小组的化学探究浓硫酸与铁钉(碳素钢)反应后产生气体的成分。
【查阅资料】①Fe与浓H2SO4 反应,加热,有SO2生成 ,
②C与浓H2SO4 反应,加热,有CO2和SO2生成,
③SO2 可使澄清石灰水变浑浊,
④SO2可使口红溶液的红色褪去,而CO2不能。
⑤SO2可使酸性高锰酸钾溶液褪色,而CO2不能。
⑥碱石灰的主要成分是NaOH和CaO
【实验探究】称取24.0克铁钉放入60.0ml浓硫酸中,加热,充分反应后得到溶液X并收集到气体Y。甲同学通过实验测定并推知气体Y中SO2的体积分数为66.7%。同学们认为气体Y中还可能含有H2和Z气体,则Z气体可能是 。探究实验的主要装置如下图所示:
⑵装置A中试剂的作用是 。
⑶为确认Z的存在,需将装置甲(如图所示)拉入上述装置(填编号) 之间。装置甲中的液体名称是 。
⑷在实验中,如果观察到装置D中 ,且装置E中 ,则可确认Y中含有H2气体。
⑸如果需要测定限定体积气体Y中H2的含量,(H2约为0.01克)。除可用测量
H2体积的方法外, (选填“能”或“不能”)用称量上图装置D装置E的质量变化的方法,通过计算并说明你判断的理由。
试题篮
()