类比法是化学研究物质的重要方法之一。草酸(H2C2O4)的化学性质与碳酸相似,受热分解后得到三种氧化物。某兴趣小组对草酸的有关性质进行探究。
【提出猜想】猜想一:草酸也能使紫色石蕊试液变______色;
猜想二:三种氧化物可能是CO2、CO和_______(填化学式),该猜想的依据是______ ___。
【查阅资料】1、无水硫酸铜是一种白色粉末,遇水变成蓝色。
2、向氯化钯溶液中通入CO,会产生黑色沉淀。
【实验探究】兴趣小组为验证猜想二,将草酸受热后得到的气体,依次通过下图中的A、B、C装置。
【实验结论】当观察到装置A中变蓝、B中变浑浊、C中_________________的实验现象时,证明猜想二是正确的。写出B中发生反应的化学方程式_______________________。
【实验反思】①根据实验结论,从环保角度考虑,实验中应对尾气进行处理。处理方法是_______________。
②草酸受热分解的化学方程式为_______________________________________。
小明家的新房装修,瓦工师傅用石灰浆(主要成分是氢氧化钙)抹墙。收工时瓦工师傅把未用完的石灰浆用沙土盖上,以备第二天再用,这样做的目的是防止石灰浆因变质而失效。
(1)请你根据所学知识写出石灰浆变质的化学方程式 。
(2)小明想通过实验验证石灰浆的变质情况,请你帮助小明完成以下实验。
| 实验步骤 |
实验现象 |
实验结论 |
|
| 取样,加一定量的水充分溶解后,过滤。 |
取少量滤渣于试管中,加入足量 。 |
|
反应的化学方程式为 ; 实验的结论是该石灰浆部分变质。 |
| 取少量滤液于试管中,滴入无色酚酞试液。 |
|
(3)由此小明联想到实验室里的一些药品必须密封保存。实验室中必须密封保存的药品可分为以下几类:
①药品能与空气中的成分发生反应,如澄清的石灰水;
②药品具有挥发性,如 ;
③ ,如浓硫酸。
张宁和刘明同学学习完酸、碱、盐后发现:碱溶液能使酚酞溶液变红,
溶液也能使酚酞溶液变红。通过学习知道,碱溶液使酚酞溶液变红,是因为碱在水中离解出
,那么
溶液中究竟是哪种粒子使酚酞溶液变红呢?请你帮助他俩完成实验探究。
【提出问题】
属于(填"酸"、"碱"、"盐"),为什么能使酚酞溶液变红?
【进行猜想】
(1)
使酚酞溶液变红。
(2)水分子使酚酞溶液变红。
(3)使酚酞溶液变红。
【设计实验】

(1)实验Ⅰ的目的是为了验证猜想不成立。
(2)刘明同学认为实验Ⅱ没必要做,他的理由是。
(3)实验Ⅲ滴入
溶液,振荡,酚酞试液变 红。向变红后的溶液中滴加
溶液至过量,振荡,出现的现象是,反应的化学方程式是。(提示:
溶液呈中性)
(4)由实验Ⅰ、Ⅱ、Ⅲ得出猜想(3)正确。张宁对此结论有些质疑,于是他查阅资料。
【查阅资料】
溶液中,
和
发生如下反应:
【得出结论】 溶液中使酚酞溶液变红的粒子是。
征得老师同意,爱动脑筋的小亮在实验室对放置已久的NaSO3的样品成分开展了探究:
【查阅资料】
【提出问题】钙亚硫酸钠是否变质了呢?是全部变质还是部分变质呢?
【猜想】猜想1:样品未变质(即:样品中含有
)
猜想2:样品全部变质(即:样品中只含 )。
猜想3 :样品部分变质(即样品含中
和
)
【实验探究】
| 实验操作 |
实验现象 |
结论 |
| ①用少量粉末装入试管,加少量蒸馏水溶解,向溶液中滴加足量的盐酸,并不断震荡 |
现象A |
猜想2不成立 |
| ②取步骤①中少量的液体于试管中然后,操作Ⅱ |
有白色沉淀 |
猜想1不成立 |
回答下列问题:
(1)猜想2中:样品中只含(填化学式)
(2)现象A为 。
(3)操作Ⅱ 。
(4)写出操作Ⅱ的化学方程式: 。
【反思】根据以上探究:实验室里亚硫酸钠必须密封保存。为了防止与空气中的二氧化碳反应变质。实验室必须密封保存的药品很多,试举一例:(填药品名称)
在盐酸除铁锈的实验中,我们常会发现生锈的铁钉表面有一些气泡产生,气泡是怎么产生的?针对这一问题,同学们提出了有关假设,并设计了如图甲所示的实验方案惊醒探究,实验时,观察到放有铁的试管中有气泡产生,而另一试管中没有,从而验证了自己的假设是成立的.
(1)分析上述实验,你认为同学们建立的建设是.
(2)有同学认为上述实验不够严谨,溶液中的水可能会对实验产生影响.于是他们又进行了对照试验,请你在答题卷的虚线框中用图示的形式将图乙的对照试验补充完整.
(3)还有同学想:气泡会不会是铁锈与水反应产生的?他认为还要补充一个铁锈与水反应的实验,你觉得有没有必要?.


某化学兴趣小组的四位同学对氢氧化钠溶液与稀盐酸混合后,所得溶液中溶质的成分进行了探究。
【作出猜想】小马猜想:溶质有
、
、
小程猜想:溶质只有
小宫猜想:溶质有
、
小尚猜想:溶质有
、
(1)老师认为小马的猜想是错误的,她的理由是。
【方案设计】小程和小宫分别设计了如下方案验证各自的猜想。
| 实验设计者 |
方案步骤 |
方案预估现象 |
方案结论 |
| 小程 |
用一根洁净的玻璃棒取反映后的溶液沾在
试纸上,把试纸所呈现的颜色与标准比色卡进行对照 |
小程猜想正确 |
|
| 小宫 |
取少量反应后的溶液于一支试管中,再向试管中滴加稀硝酸和硝酸银溶液 |
有白色沉淀生成 |
小宫猜想正确 |
【方案评价】(2)两位同学中的方案正确。
【方案反思】(3)请分析错误方案的原因(都正确,不作答)。
【拓展研究】(4)请你再设计一个实验方案验证小尚的猜想正确,填写下列实验报告。
| 方案步骤 |
方案预估现象 |
方案结论 |
| 小尚猜想正确 |
同学们在帮助老师整理实验室时,从1、2号橱窗中发现了两瓶失去标签的黑色粉末药品,并确定了这两瓶黑色粉末是木炭粉、铁粉、氧化铜、高锰酸钾中的两种。他们继续进行了分析、试验和反思:
【查阅资料】
、
等金属氧化物与酸反应,生成盐和水
(1)分析:小燕同学认为一定不是高锰酸钾,原因是;
(2)实验一:
| 实验操作 |
||
| ①取一种黑色粉末少许,加入到稀硫酸中 |
黑色粉末溶解,溶液颜色变 | 此粉末是氧化铜 |
| ②取另一种黑色粉末少许,加入到稀硫酸中 |
黑色粉末不溶解,没看到气体产生 |
此粉末一定不是铁粉 |
(3)反思:小华同学认为不做实验①,运用逻辑推理的方法也能得出其中之一是氧化铜的结论,原因是:;
(4)实验二:他们又进行了如下实验:将两种黑色粉末混合加热(实验装置如下图),发现黑色粉末逐渐变,澄清石灰水变。写出两种黑色粉末发生反应的化学方程式。

复分解反应的定义可以用字母AB+CD=AD+CB来表示.某化学兴趣小组探究稀盐酸与以下四种物质是否能发生复分解反应:
|
溶液 |
溶液 |
溶液 |
溶液 |
(1)甲同学提出稀盐酸与
溶液是否发生复分解反应?乙同学认为不反应,因为这两种化合物互相交换成分,所得的物质是一样的.你(填"同意"或"不同意")乙同学的看法.
(2)甲乙设计了以下三个实验,请你在空白处填写相关内容:
| 实验操作 |
实验现象 |
实验结论 |
|
| 实验1 |
在
溶液中加入稀盐酸 |
|
稀盐酸与
溶液发生了复分解反应 |
| 实验2 |
在
溶液中加入稀盐酸 |
有白色沉淀生成 |
|
| 实验3 |
在
溶液中加入稀盐酸 |
没有明显现象 |
甲乙同学:不发生反应 |
(3)写出实验2的化学方程式:.
(4)在实验3中,甲乙两同学因为观察到没有明显的实验现象,故判断该反应不能进行,你(填"同意"或"不同意")他们的看法,若不同意,请设计实验证明该反应能发生.可用试剂:
溶液、稀盐酸、石蕊试液.
| 实验内容与操作 |
实验现象 |
实验结论 |
乙炔(C2H2)气体和氧气反应能产生高温火焰,工人师傅常用氧炔焰切割或焊接金属。乙炔由碳化钙(块状固体,化学式为CaC2)与水反应生成,同时生成一种白色固体。
【提出问题】白色固体是什么物质?
【做出猜想】小明经过思考认为有以下几种可能:
猜想一:CaO;猜想二: ;猜想三:Ca(OH)2,他的依据是 。
【交流反思】经过同学们交流讨论,认为猜想一不成立。否定猜想一的理由是: 。
【进行实验】
| 实验操作 |
实验现象 |
实验结论 |
| 取少量白色固体放入试管中,滴加稀盐酸。 |
。 |
猜想二不成立:不是CaCO3。 |
| 取少量白色固体加入到水中,取上层清液, 。 |
。 |
猜想三成立:白色固体是Ca(OH)2 |
【拓展应用】已知碳化钙与水反应非常剧烈,乙炔的密度比空气略小,难溶于水。实验室欲制取并收集纯净的乙炔,要求做到节约、安全、随时发生、随时停止,你选择的装置是(填图中装置序号) 。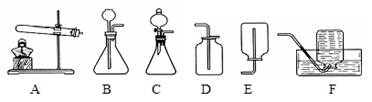
我校实验室有一瓶保管不当的试剂,其残缺的标签中只剩下“钠”和“10%”字样(如图所示)。已知它是初中化学常用的试剂。小强和小华同学很感兴趣,决定对其成分进行探究: 
【提出问题】这瓶试剂可能是什么溶液呢?
【交流讨论】根据受损标签的情况判断,这瓶试剂不可能是下列三类物质中的 (填序号)。
A、酸 B、碱 C、盐
【查阅资料】 Ⅰ、初中化学常见的含钠化合物有NaCl、NaOH、Na2CO3、NaHCO3。
Ⅱ、测定室温(20℃)时,四种物质的溶解度的数据如下:
| 物质 |
NaCl |
NaOH |
Na2CO3 |
NaHCO3 |
| 溶解度/g |
36 |
109 |
21.5 |
9.6 |
【得出结论】小华根据试剂瓶标注的溶质质量分数10%和上表中的溶解度的数据判断,这瓶试剂不可能是 。
【做出猜想】①可能是NaOH溶液;②可能是 溶液;③可能是NaCl溶液。
【设计并实验】 (1)小强取样品少量,滴加无色酚酞试液,液体变红色他认为猜想①正确,他的判断是否合理 ,原因是 。
(2)小华为了检验该溶液到底是什么又进行了如下实验:取样品于试管中,滴加氯化钡溶液,有白色沉淀生成,他得出猜想②正确。相应的化学方程式 。
老师在装有酸的储物柜中发现一瓶没有标签的溶液,让同学们鉴定该溶液是否为盐酸溶液。
| 实验步骤 |
实验现象 |
实验结论 |
| 1.取少量待测液体与试管中,滴加几滴石蕊溶液 |
|
溶液呈酸性 |
| 2.取少量待测液与试管中,滴加 溶液 |
产生了白色沉淀 |
该待测溶液为盐酸 |
| 3.往上述2中的沉淀滴加 溶液 |
|
写出上述操作2中所发生的化学方程式: 。
实验室有四瓶失去标签的溶液,现标为A、B、C、D,分别是碳酸钾溶液、氢氧化钠溶液、硫酸镁溶液和稀盐酸中的一种。
【提出问题】如何区分出四种溶液?
【进行实验】甲同学取少量A溶液于试管中,加入一定量氢氧化钡溶液,观察到无明显现象,由此甲同学认为A一定不是(1) ,甲同学继续向实验后的溶液中滴加酚酞溶液,酚酞溶液由无色变为红色,则甲同学得出结论:A是氢氧化钠溶液。
【表达与交流】乙同学不同意甲同学的结论,乙同学的理由是(2) 。
于是乙同学另取少量A于试管中,向其中滴加一种试剂是(3) 溶液,观察到的明显现象是(4) ,由此证明了甲同学的结论是错误的,同时确定了A。
同学们继续实验:取B、C、D三种溶液置于试管中,分别依次滴加氯化钡溶液和稀硝酸,观察现象。
【收集证据】观察到C中产生白色沉淀,滴加稀硝酸后,沉淀溶解,产生气泡;D中产生白色沉淀,滴加稀硝酸后,沉淀不溶解;B中无明显现象。
【解释与结论】写出D中发生反应的化学方程式(5) 。
同学们最终通过实验区分出了四种溶液。
某化学学习小组的同学围绕“澄清石灰水与碳酸钠溶液的反应”展开了如下探究活动。
(1)该反应的化学方程式为_______________________________________。
(2)反应后溶液中的溶质是什么?同学们一致认为有以下三种情况:①氢氧化钠和氢氧化钙;②氢氧化钠和碳酸钠;③____________________________。
(3)小新取少量溶液于试管中,滴加过量稀盐酸,发现无气泡产生,说明情况________(填序号)是不可能的。
为了进一步确定溶液的成分,同学们设计了如下实验方案:
| 实验步骤 |
现 象 |
结 论 |
| |
|
情况①正确 |
小红选择了另外一种不同类别的物质________________________________(填化学式),也得到了同样的结论。在同学们的合作下,他们顺利完成了探究任务。
小亮在做“盐酸中和氢氧化钠溶液”的实验时,滴加盐酸前忘了加入指示剂,导致无法判断该中和反应进行的程度,于是他对所得的溶液的酸碱性进行了探究。
【探究目的】探究所得溶液的酸碱性
【提出猜想】所得溶液可能呈碱性,也可能呈 性,还可能呈 性。
【实验验证】
| 实 验 操 作 |
实 验 现 象 |
结 论 |
| 用试管取该溶液1 mL~2 mL, 滴入1滴~2滴无色酚酞试液, 振荡 |
无色酚酞试液变 |
溶液呈碱性 |
| 无色酚酞试液不变色 |
溶液呈 |
【分析与思考】
(1)若溶液呈碱性,则溶液中使其呈碱性的离子是 (填写微粒符号),为避免碱性溶液污染环境,小亮对所得溶液进行了如下处理:向溶液中逐滴加入 溶液,直到不再产生沉淀为止。然后过滤,把滤液倒入蒸发皿中加热,得到氯化钠晶体,该过程涉及的化学反应的方程式为 。
(2)若无色酚酞试液不变色,为了进一步确定溶液的酸碱性,小亮提出以下方案:
方案一:取样,加入碳酸钠溶液,若观察到 ,
则所取溶液呈酸性;若无明显现象,则呈中性。
方案二:取样,加入金属锌,若有气泡产生,则所取溶液呈酸性,该反应的化学方程式为 ;若无明显现象,则呈中性。
为了探究碱的性质,甲、乙两组同学向相同体积的石灰水和烧碱溶液中分别通入CO2气体。观察到前者变浑浊,后者无明显现象。甲组同学认为CO2能与石灰水反应,但不能与烧碱溶液反应;而乙组同学认为CO2也能与烧碱溶液发生反应。
(1)为证明自己的观点,乙组同学又设计并做了以下实验:
①用石灰石和稀盐酸制取CO2气体。写出该反应的化学方程式:_____________,
并从甲图中选出正确的制取装置_____________。(填“A”或“B”)
②收集一烧瓶CO2气体,注入烧碱溶液后立即塞上带有导管和气球的橡皮塞(如乙图所示),振荡后观察到圆底烧瓶内气球膨大。由此乙组同学认为自己的观点是正确的。
(2)甲组同学提出反驳:因为_____________,所以还必须设置对照实验,即用________代替烧碱溶液进行实验,如果观察到气球膨大程度__________(填“增大”或“减小”),才能最终证明乙组同学的观点是正确的。
试题篮
()