酸、碱、盐是几类有广泛用途的重要化合物.
(1)酸和碱在组成和性质方面有很多共同的特点,请任写出其中的一条.
(2)氢氧化钙是一种常见的碱,列举其在生产、生活中的一种用途.
(3)某化学兴趣小组在实验室发现了一瓶标签受到腐蚀(如右图)的溶液,他们对此产生了兴趣.
提出问题:这瓶溶液究竟是什么?
经过询问实验老师平时的药品保管得知,这瓶无色溶液应该是碳酸钠、碳酸氢钠、氯化钠、硫酸钠、硝酸钠中的某一种.为了确定该药品,他们首先进行了理论分析:
①小明根据标签上的组成元素认为一定不可能是 (提示:只有其中一种).
②小英提出,碳酸氢钠、硝酸钠也不可能,你认为她的依据是:
设计实验:为了确定该溶液究竟是剩余两种盐的哪一种,他们设计了如下实验.
| 实验操作 |
实验现象 |
| 取少量样品于试管中,慢慢滴加BaCl2溶液 |
出现白色沉淀 |
| 静置一段时间后,倾去上层清液,向沉淀中滴加稀盐酸 |
白色沉淀全部溶解,并产生大量气泡 |
实验结论:③该瓶无色溶液是 .出现白色沉淀过程的化学方程式是: .
实验反思:④小强认为上述设计实验还可简化,也能达到目的.小强的实验操作是:
(4)若73 g质量分数为20%的盐酸与127g氢氧化钠溶液恰好完全中和,试计算反应后所得溶液中溶质的质量分数.
草酸(H2C2O4)是一种有机物,在受热条件下分解生成水和另外二种氧化物。某校兴趣小组对此展开探究:
(1)常用 试剂检验生成物中是否含有水。
(2)对分解产物中的另外二种氧化物进行假设和验证:(图中固定试管的仪器已略去)
| 假设 |
实验 |
现象 |
结论 |
| 假设一: 生成物中有二氧化碳 |
将生成的气体通入澄清的石灰水 |
现象是 |
生成物中含有二氧化碳。 |
| 假设二: 生成物中有一氧化碳 |
用下图装置进行实验 |
A中的现象是 |
生成物中含有一氧化碳。写出A中的反应化学方程式是 |
(3)下表是根据“假设二”设计的甲、乙两套实验方案,请指出它们各自的不足之处
| 方案 |
步骤 |
不足 |
| 方案甲 |
先通一氧化碳,再点燃酒精灯 |
|
| 方案乙 |
先点燃酒精灯,再通一氧化碳 |
|
查阅资料后同学们改进实验装置如图所示:
该实验过程中装置C的作用是
通常情况下,人体呼出气体中部分气体的含量和空气中部分气体的含量有所不同。请你根据所学的知识,完成下列实验报告。
| 操作步骤 |
现象 |
结论 |
| 取呼出气体和等体积的空气各一瓶,将燃着的小木条分别插入集气瓶中,盖上玻璃片 |
|
人体呼出气体中氧气的含量小于空气中氧气的含量 |
| 取呼出气体和等体积的空气各一瓶,向其中各滴入相同滴数的澄清石灰水 |
呼出气体瓶中澄清石灰水变浑浊,空气瓶中无明显现象 |
|
| |
被哈气的干燥玻璃片上有水珠,未被哈气的干燥玻璃片上没有明显现象 |
人体呼出气体中水蒸气的含量高于空气中水蒸气的含量 |
某学习小组在探究“酸的化学性质”时,做了如图所示的A、B两个实验.分别向氢氧化钠和碳酸钠溶液中加入一定质量的稀硫酸,反应结束后,把废液倒入同一个废液缸中,观察到废液缸中产生少量气泡.请回答下列问题:
(1)试管A中的化学方程式是 ,在实验过程中并没有观察到该反应的明显现象,请你写出一种能观察到变化发生的方法 (2)通过分析废液缸中的现象,你认为B试管的废液中溶质成分是 (填化学式,下同);
(3)小组同学对废液缸中最终废液的成分进行探究,请你一起参与探究.
【提出问题】最终废液中溶质是什么?
【查阅资料】硫酸钠溶液显中性.
【假设猜想】猜想①:Na2SO4
猜想②:Na2SO4、Na2CO3
猜想③:
【实验探究】请你设计实验,确定哪个猜想是正确的.
| 实验步骤 |
|
实验结论 |
| |
|
猜想1正确 |
| |
猜想2正确 |
|
| |
猜想3正确 |
利用金属和某些溶液能否发生置换反应可以确定金属活动性顺序.为了验证铝、铁、铜的金属活动性顺序,某同学设计了两个合理方案,所需试剂如下:
方案一:铝片、 、铜片;
方案二:铝粉、氯化亚铁溶液、硫酸铜溶液.
(1)方案一中缺少的试剂可以是 ;
(2)写出方案二的实验操作步骤、预期现象和反应的化学方程式.
某化学兴趣小组的同学按照课本上的实验装置做“测定空气中氧气的体积分数”实验(如图所示),但测出的氧气的体积分数明显小于1/5。请你参与探究:
(1)提出问题:造成误差的原因是什么?如何改进课本上的实验装置?
(2)查阅资料:红磷、白磷的一些性质如下表:
| |
颜色、状态 |
熔点/℃ |
着火点/℃ |
密度/(g/cm3) |
| 红磷 |
暗红色固体 |
590 |
240 |
2.34 |
| 白磷 |
白色或黄色固体 |
44.1 |
40 |
1.82 |
(3)猜想与假设:
①甲同学:可能是导管内原含有空气,后来留有吸入的水,影响实验的准确性。
②乙同学:可能是瓶内残留气体中还有氧气。
③你还能作出的猜想是 。
(4)交流与讨论:
①丙同学认为用木炭代替红磷,就可以消除误差,你认为他的猜想 ,(填“合理”或“不合理”)理由是 。
②他们对课本上的实验装置进行了图2所示的改进(其他仪器忽略)。
a.甲同学提出应把红磷换为白磷,理由是 _______________。
b.通过粗铜丝来点燃玻璃管内的白磷,这利用了金属的 性。
c.与课本上的实验装置相比较,该装置的一个优点是_________________________________.
(5)探究与反思:
①为了验证乙同学的猜想,将铜粉放在残余气体中加热,观察到铜粉变黑色,证明乙同学的猜想 (填“合理”或“不合理”)
②大家用改进的实验装置(如图所示)进行实验,待玻璃管冷却、管内白色的烟幕消失时,左玻璃管内的液面上升了1格,得到了较准确的结果,但又意外发现左玻璃管内壁上端附着黄色固体。左玻璃管上端的黄色固体的主要成分可能是 。
某研究小组在学习氧气的化学性质时发现:铁丝在氧气中燃烧没有火焰,而蜡烛在氧气中燃烧却有明亮的火焰。该小组同学进行了如下探究。
(1)写出铁丝在氧气中燃烧的文字表达式: 。
(2)探究一:蜡烛燃烧产生火焰的原因是什么?
点燃蜡烛,将金属导管一端伸入内焰,导出其中物质,在另一端管口点燃,也有火焰产生(如图所示)。由此可知:蜡烛燃烧产生的火焰是由 (填“固态”或“气态”)物质燃烧形成的。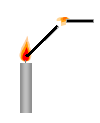
(3)探究二:物质燃烧产生火焰的根本原因是什么?
【查阅资料】
| 物质 |
熔点╱℃ |
沸点╱℃ |
燃烧时温度╱℃ |
| 石蜡 |
50∽70 |
300∽550 |
约600 |
| 铁 |
1535 |
2750 |
约1800 |
| 钠 |
97.8 |
883 |
约1400 |
由上表可知:物质燃烧能否产生火焰与其 (填“熔点”或“沸点”)和燃烧时温度有关。通过上表中石蜡、铁的数据对比,你认为物质燃烧时,什么情况下能产生火焰 。由此推测:钠在燃烧时, (填“有”或“没有”)火焰产生。
(4)根据硫在空气或氧气中燃烧的实验事实,请你推测硫沸点 硫燃烧时的温度(填“>”或“<”或“=”)
三瓶遗失标签的无色溶液分别是盐酸、氢氧化钠、氢氧化钙,为鉴别这三瓶溶液进行如下实验.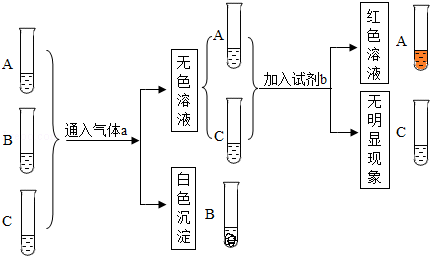
(1)①气体a的名称是 ,原A和B两只试管所盛溶液中对应溶质的化学式分别是 、 .
②生成白色沉淀的化学方程式是 .
③如果只用一种试剂来鉴别三种溶液,可选用的试剂是 .
(2)若遗失标签的是盐酸、碳酸钠、氢氧化钙三瓶溶液,鉴别时不需外加任何试剂,只需将其中的溶液①分别滴加到另外两种溶液②、③中,若实验现象是 ,则①是 .
经实验可知,硫酸铜溶液加到过氧化氢溶液中,也会产生大量的气泡.硫酸铜溶液中有三种粒子(H2O SO42﹣ Cu2+),小明想知道硫酸铜溶液的哪种粒子能使过氧化氢分解的速率加快,请你和小明一起通过下图所示的三个实验完成这次探究活动,并填写空白:
(1)你认为最不可能的是哪一种粒子? 。理由是 。
(2)要证明另外两种粒子能否加快过氧化氢分解的速率,还需要进行实验②和③:在实验②中加入稀硫酸后,无明显变化,说明 不起催化作用;在实验③中加入 后,会观察到大量气泡,证明起催化作用的是 。
(3)如果要确定硫酸铜是催化剂,还需通过实验确认它在化学反应前后 。
一次趣味化学活动中,王老师向同学们展示了一瓶标签受损的无色溶液,如图所示。要求同学们进行探究:确认这瓶溶液究竟是什么溶液?
【提出猜想】王老师提示:这瓶无色溶液只能是下列四种溶液中的一种:①硫酸镁溶液;②硫酸钠溶液;③硫酸溶液;④硫酸铵溶液
【查阅资料】
①常温下,相关物质的溶解度如下:
| 物质 |
MgSO4 |
Na2SO4 |
(NH4)2SO4 |
H2SO4 |
| 溶解度 |
35.1g |
19.5g |
75.4g |
与水任意比互溶 |
②(NH4)2SO4的水溶液显酸性
(1)【实.验探究】小明对王老师的提示进行了评价不可能是Na2SO4,原因是 。
(2)为确定其它几种猜想是否正确,小明同学继续进行探究:
| 实验操作 |
实验现象 |
实验结论 |
| ①取该溶液少许于试管中,向其中滴加几滴 溶液 |
溶液中有白色沉淀生成 |
猜想①成立 |
| ②用玻璃棒蘸取少许原溶液滴在pH试纸上,并跟标准比色卡对照 |
溶液pH小于7 |
猜想③成立 |
小雅对小明实验操作②的结论评价是 ,理由是 _;
(3)请你设计实验方案,确认该溶液是硫酸铵溶液并完成实验报告:
| 实验操作 |
实验现象 |
实验结论 |
| 取该溶液少许于试管中, ① ②将湿润的红色石蕊试纸放在试管口 |
①产生有刺激性气味的气体 ② |
猜想④成立,该反应的化学方程式为 |
某化学兴趣小组在做完制取二氧化碳的实验后(用石灰石和稀盐酸制取),对反应后反应器内的剩余溶液的溶质成分产生了兴趣,他们继续进行了以下实验探究.
【分析推断】根据制取二氧化碳的反应原理,可以确定剩余溶液中一定含有氯化钙.但其中是否含有氯化氢需要通过实验来证明.若剩余溶液显酸性(含有
),说明含有氯化氢.
【查阅资料】碳酸钙不溶于水,氢氧化钙微溶于水,氯化钙溶液呈中性.
【实验过程】将剩余的溶液倒入烧杯中,微热后冷却到室温.
| 实验操作 |
实验现象 |
实验结论 |
|
甲同学 |
取烧杯中溶液少许于试管中,向其中滴加 | 现象:溶液变为红色 |
溶液显酸性(含有
);溶质中有氯化氢. |
乙同学 |
取烧杯中溶液少许于试管中,向其中加入少量锌粒 |
现象:反应的化学方程式是: | |
丙同学 |
取烧杯中溶液少许于试管中,向其中加入少量石灰石 |
现象: |
【拓展提高】若要从剩余溶液中得到尽可能多的纯净的氯化钙固体,同学们认为可以向剩余溶液中加入稍过量的(填化学式),经、蒸发等操作后即可完成.
小明在实验室验证盐酸化学性质时,将碳酸钠溶液倒入装有稀盐酸的烧杯中看到有气泡产生.为了解两种物质间的反应情况,他决定从反应后溶液中溶质的组成入手进行探究.
(1)小明对反应后溶液溶质组成了两种猜想,请你再补充一种猜想
猜想1:溶质为
和
;
猜想2:溶质为 和 ;
猜想3:溶质为.
(2)比较三种猜想,说明你提出猜想3的理由:.
(3)小明设计两个不同的实验方案,用两种方法验证了猜想2成立.按要求填写下表.
| 实验操作 |
实验现象 |
实验结论 |
|
| 方法一 |
取少量反应后溶液,加入 | 猜想2成立 |
|
| 方法二 |
取少量反应后溶液,加入硝酸银溶液 |
|
猜想2成立 |
(4)反思与评价:
你认为方法二是否正确,说出理由:.
为了探究酸碱性对唾液淀粉酶催化作用的影响,小明利用蒸馏水、1%淀粉溶液、稀释的唾液、稀盐酸、氢氧化钠溶液、碘液等材料进行实验.请你完成相应的实验设计和问题分析.
【实验设计】
| 实验操作 |
设计要求 |
| 步骤一:取3支洁净的试管标为 、 、 ,在各试管中分别加入1%淀粉溶液2毫升;向 试管加入l 毫升稀盐酸和l毫升唾液;向 试管加入1毫升氢氧化钠溶液和1毫升唾液;向 试管加入 | 设置对照实验 |
| 步骤二: | 控制实验条件 |
| 步骤三:10分钟后,往3支试管中分别滴入1滴碘液,观察颜色变化. |
获取实验证据 |
【问题与分析】
正确操作后,小明观察到
试管呈蓝色,而
试管没有出现预期的蓝色.他想:为什么
试管不呈蓝色?他推测可能是氢氧化钠溶液变质或者
试管中液体碱性太弱.在老师的帮助下,他证实了氢氧化钠溶液没有变质,且
试管中液体碱性强度足以抑制酶的催化作用.请你对
试管没有出现蓝色作出一种合理的猜测:.
气体的密度容易受温度和压强的影响.为了测量常温常压下氧气的密度,在老师的指导下,小明进行了如下实验:
步骤一:检查发生装置的气密性.
步骤二:往烧瓶中装入适量的二氧化锰粉未.关闭分液漏斗的活塞,并将适童的过氧化氢溶液倒人分液漏斗中,测出发生装置的总质量为
克.
步骤三:取一个集气瓶,用记号笔在适当位置做标记,将水注入集气瓶到标记处,用量筒测出这些水的体积为
毫升.再将集气瓶灌满水倒扣在水槽中等待收集.
步骤四:打开活塞,滴入过氧化氢溶液,同时干始收集气休.调节集气瓶在水中的上下位置,当集气瓶内、外的液面相平且刚好达到标记处时(如图).暂停反应.
步骤五:重复步骤四,再收集9瓶气体.
步骤六:称出反应后发生装置的总质量为
克.
(1)小明通过该实验,测得氧气的密度是克/毫升.
(2)步骤四中,控制集气瓶内、外液而保持相平的目的是.
(3)如果实验中装置气密性不良,将对测得的密度值有何影响?请说明理由.
碳酸氢钠(
)俗称"小苏打",在生活中用途广泛.某化学实验小组的同学对碳酸氢钠的性质进行探究.
【探究实验1】碳酸氢钠溶液的酸碱性
用试管取适量碳酸氢钠溶液,滴加酚酞试液,振荡,溶液变浅红色.结论:.
【探究实验2】能与酸反应
取适量碳酸氢钠加入试管中,滴加稀盐酸,再把燃着的木条迅速伸入试管,木条熄灭,碳酸氢钠和盐酸的化学反应方程式:.
【探究实验3】能与碱反应
查阅资料:
;氢氧化钙微溶于水.用试管取适量碳酸氢钠溶液,滴加氢氧化钠溶液,无明显现象.(提示:可以选择
溶液做试剂,通过证明有
生成,从而证明二者发生了反应)如图,两位同学分别进行了甲、乙两个实验.回答下列问题:

比较甲、乙两个实验的目的性区别是;
有同学提出两个实验都不足以证明有
生成,其理由;要证明有
生成,还需要进行的操作是.
试题篮
()