初中化学课上,同学们利用下列实验探究碱的化学性质:
(1)A实验中反应的化学方程式为________________________________________。
(2)C实验中观察到的现象是____________________________________________。
(3)实验结束后,同学们将废液倒入同一只废液缸中,最后发现废液浑浊并显红色。
【提出问题】 废液中含有什么物质?
【假设猜想】 通过分析上述实验,同学们猜想:废液中除酚酞、碳酸钙及水以外一定含有___________。
老师问:废液中还可能有什么物质?引发了同学们热烈讨论,下面是大家的发言:
| 学生甲 |
可能有Ca(OH)2、NaOH |
学生丙 |
可能有Ca(OH)2、CaCl2 |
| 学生乙 |
可能有NaOH、Na2CO3 |
学生丁 |
可能有Na2CO3 |
| 学生戊 |
可能有NaOH |
…… |
………… |
【实验验证】 同学们对可能含有的物质进行确定,取一定量的废液过滤,向滤液中逐滴加入氯化钡溶液,得到白色沉淀,红色褪去。
【结论】上述滤液中,还含有________,没有______________________。
某学校科学兴趣小组在研究“带火星木条复燃与氧气体积分数的关系”的课题中,采取了以下实验步骤:①取5只250mL集气瓶,向5只集气瓶中分别装入25mL、50mL、75mL、100mL、125mL的水,并用毛玻璃片盖住,依次编号为1、2、3、4、5。②用分解过氧化氢(H2O2)的方法制取氧气,用制取的氧气通过排水法将上述1-5号瓶中的水排去。③将带火星的木条依次插入1-5号瓶中,把观察到的现象和计算数据,填入下表。
| 集气瓶标号 |
1 |
2 |
3 |
4 |
5 |
| 集气瓶中收集氧气的体积 |
25mL |
50mL |
75mL |
100mL |
125mL |
| 带火星木条的状况 |
微亮 |
亮 |
很亮 |
复燃 |
复燃 |
试回答下列问题:
⑴从观察到的现象知,使带火星的木条复燃所需氧气的最小体积分数介于( )号瓶至( )号瓶之间:
⑵实验室中采用分解过氧化氢的方法制取氧气,其反应的文字表达式为
,反应类型属于
⑶根据以上实验事实,下列说法中正确的是
A.只有在纯氧中才能使带火星的木条复燃
B.集气瓶中氧气的体积分数≥52.6%时,带火星的木条就能复燃
C.只要有氧气存在就可使带火星的木条复燃
⑷当4号瓶收集氧气为100 mL时,那么瓶中实际氧气所占的体积分数为 %
上述实验表明:物质燃烧的程度与氧气的浓度有关,氧气浓度越大,燃烧越剧烈。(如你能再设计一个实验来说明此问题可奖励2分)。
探究实验报告一:蜡烛及其燃烧的探究
探究实验的名称:蜡烛及其燃烧的探究
探究实验的目的:理解掌握蜡烛的有关性质知识
实验用品:蜡烛、火柴、 等
| 步骤和方法 |
现象 |
分析 |
|
| 点燃前[ |
|
蜡烛是白色蜡状固体,硬度小,稍有气味 |
|
| 用小刀切下一小块蜡烛投入水中 |
石蜡浮于水面 |
|
|
| 点燃蜡烛 |
|
蜡烛先熔化后气化,再燃烧;火焰明亮且明显分成三层 |
|
| 在烛焰上方罩一干燥烧杯 |
烧杯内壁出现水雾或水珠 |
|
|
| 在烛焰上方罩一个内壁沾有澄清石灰水的烧杯,振荡 |
烧杯内壁出现白色斑点 |
|
|
| 熄灭蜡烛 |
火焰熄灭,灯芯上产生一缕轻烟 |
轻烟为蜡烛蒸气冷却所致,遇明火可以燃烧。 |
结论:在通常情况下,蜡烛是白色蜡状固体,稍有气味,熔点、熔点较低,硬度较小,密度比水小。蜡烛在点燃条件下能燃烧,燃烧产物中有水和二氧化碳等。
问题和建议:为进一步说明蜡烛是先气化,然后是石蜡蒸气燃烧,可用一根尖嘴的细玻璃管插入焰心,然后在尖嘴处点燃。根据是否能点燃,可推断上述猜测是否正确。
科学探究是奇妙的过程,请你一起参与实验探究,并填写下列空白:
(1)[提出问题]小松同学用“双氧水”(过氧化氢溶液)清洗伤口时,不小心将过氧化氢溶液滴到水泥地板上,发现有大量气泡产生。小松联想到自己曾经用二氧化锰做过氧化氢分解的催化剂,他想,水泥块能否也可作过氧化氢分解的催化剂呢?于是他到附近建筑工地取回一些小水泥块,并用蒸馏水浸泡、冲洗、干燥,并进行以下探究。
(2)[猜想]水泥块能作过氧化氢分解的催化剂。
(3)[实验验证]
| |
实验步骤 |
实验现象 |
实验结论 |
| 实验一 |
|
木条不复燃 |
常温下过氧化氢溶液不分解 |
| 实验二 |
在装有过氧化氢溶液的试管中加入水泥块,然后将带火星的木条伸入试管中 |
木条复燃 |
|
(4)[结论]水泥块能加快过氧化氢的分解速率,故水泥块能作过氧化氢分解的催化剂。
(5)[讨论与反思]小芳认为:仅凭上述两个实验还不能证明水泥块为过氧化氢分解的催化剂,她觉得需要增加一个探究实验:探究 ;
[实验步骤]①准确称量水泥块的质量;②完成实验二;③待反应结束,将实验二试管里的物质进行过滤,洗涤干燥, ;④对比反应前后水泥块质量。
[分析]如果水泥块反应前后质量不变,则说明水泥块可以作过氧化氢分解的催化荆。
(6)但小华认为,要证明小松的猜想,小芳的补充实验还是不足够,还需要再补充一个探究实验:探究 。
小组探究实验室一瓶未知溶液的成分(溶质为一种含钠化合物)。
如下药品可供选用:
石蕊溶液、无色酚酞溶液、稀盐酸、稀硫酸、氢氧化钠溶液、石灰水、硫酸铜液、氯化铵溶液
【提出问题】这瓶未知溶液中溶质的成分是什么?
【查阅资料】查阅化学实验室药品手册,得知该实验室中含钠的化合物有:
、
、
,
、
、
【提出猜想】可能是
、
、
、
、
、
中的一种
【实验方案】小华设计实验方案进行探究,请你和她一起填写实验报告:
| 实验步骤 |
实验现象 |
实验结论 |
| (1)取少量未知溶液于一支 试管中,向其中加入足量的稀 盐酸 |
无气泡产生 |
未知溶液中溶质一定不是中的一种 |
| (2)取少量未知溶液于另一 支试管中,向其中滴加无色酚 酞溶液 |
无色酚酞溶液 |
未知溶液中溶质一定是 |
【提出质疑】通过上述实验(1)中的现象,小华认为
溶液与稀盐酸不发生化学反应。小明提出反对意见,并利用老师提供的药品设计实验证明自己的观点是正确的,请你完成小明的实验方案:
| 实验步骤 |
实验现象 |
实验结论 |
| 氢氧化钠与稀盐酸 发生了化学反应 |
【反思交流】小丽对实验台上
溶液产生了兴趣,她将一定量
溶液和
溶液在试管中混合,振荡,闻到了氨味。联想到氯化铵是一种农业上常用的肥,由此她得出这种化肥在使用时的注意事项是 。
【拓展应用】通过学习知道
除了能与指示剂、酸、盐类物质发生化学反应外,还能与某些非金属氧化物发生反应。
也是-种非金属氧化物,能与
反应生成偏硅酸钠(化学式:
)和水,请写出该反应的化学方程式:。
通过查阅资料可知,玻璃成分中含有
,偏硅酸钠的水溶液俗称水玻璃,可做粘合剂。由此可知,实验室盛放氢氧化钠溶液的试剂瓶应该使用 (填"橡胶塞"或"玻璃塞")。
如图是某种薯片的包装袋,里面被一种气体充得鼓鼓的。小明对这种气体产生了兴趣,请你和小明一起对该气体进行探究。
提出问题:该气体可能是什么呢?
查阅资料:食品和氧气接触容易被氧化而腐败;常填充某种气体以防腐。
作出假设:小明认为:可能是二氧化碳;你的认为:可能是_______________。
进行实验:
| 实验步骤 |
实验现象 |
实验结论 |
| 小明用注射器抽取袋内的气体,然后注入 __________中 |
|
小明的假设正确 |
反思讨论:实验后,小明认为作为食品的防腐气体应具备某些要求,你认为应该具备哪些要求?(答出3点)
你认为:气体包装食品除防腐外,还可以_______________________________。
小刚、小军、小红对一久置的NaOH白色粉末的成分进行探究并测定其成分的含量。
(一)成分的确定
三位同学都作出以下的猜想:①可能是NaOH;②可能是Na2CO3;③可能是NaOH与Na2CO3的混合物.做出②③猜想的依据是 (化学方程式表示)。
为了验证①②③猜想,他们分别做了下面的实验。
(1)小刚取少量白色粉末于试管中,再滴加稀HCl,有气泡产生,由此可推出白色粉末中一定含有 ,肯定猜想 (填序号)是错误的。
(2)小军又取少量白色粉末溶于水,向所得溶液中滴加酚酞试液,溶液变为红色.由此小军结合小刚的实验,认为猜想③是正确的.小红却认为小军的所得结论不确切,因为 。
(3)为探究白色粉末是否含有NaOH,小红设计了如下实验方案:
①沉淀B的化学式为 ;在操作1中要用到玻璃棒,其作用是 。
②小刚认为小红的这个方案也有问题,理由是 。
但只要稍加改进,就可以证明粉末中还含有NaOH,则小刚改进的方法是: 。 小刚对小红的实验作了正确的改进后进行了实验,实验现象和小红的一致,由此确定猜想③是正确的。
二、各成分含量的测定三位同学利用电子天平共同作了以下测定实验.实验数据记录如下:
| 称 量 项 目 |
称 量 时 间 |
质量(g) |
| 试样 |
|
10.00 |
| 装置+稀硫酸质量 |
|
241.20 |
| 装置+稀硫酸质量+试样 |
反应开始后15秒 |
249.20 |
| 装置+稀硫酸质量+试样 |
反应开始后35秒 |
249.00 |
| 装置+稀硫酸质量+试样 |
反应开始后55秒 |
249.00 |
试通过分析表中数据计算出试样中碳酸钠的成份的质量分数。
小强在实验室里做实验时,拿出一瓶久置的氢氧化钙粉末,进行如下实验:
(1)取氢氧化钙粉末溶于足量水中,有_______________现象出现,小强判断该药品已变质。
(2)小强进一步做如下实验探究,请你参与并完成下表:
| 实验操作步骤 |
实验现象 |
实验结论 |
|
| 取样、加适量的水,搅拌,过滤。 |
①取少量滤渣于试管中,加入_____ |
有气泡产生 |
粉末变质 |
| ②取少量滤液于试管中,滴入______溶液。 |
________________ |
氢氧化钙粉末部分变质。 |
下图是实验室制取气体的一些装置,回答下列问题。(提示:以下所选装置均填装置序号) (8分)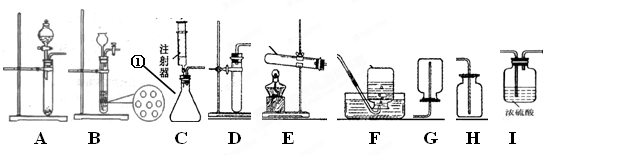
(1)写出指定仪器的名称:① 。
(2)实验室用过氧化氢代替加热高锰酸钾制取氧气,其优点是节能、简便、环保等,请写出高锰酸钾制氧气的化学方程式 。
(3)实验室利用大理石和稀盐酸用D装置制取二氧化碳,但是浪费了很多药品,老师发现后,要求节约药品,随时控制反应的发生和停止,则制取二氧化碳气体的发生装置是 ;某同学用碳酸钠和稀盐酸制取二氧化碳,请问他能否选择A或C装置 (填:能或不能),如果要除去氧气和二氧化碳中混有的水蒸气,实验装置中一定要有上述 装置。
(4)用氯酸钾制氧气的实验中,如果发现试管破裂,原因可能是 ,用排水法收集O2完毕后,停止实验时的操作顺序是 ,如果做氧气性质实验:铁在氧气中燃烧,那么用排水法收集O2时应在集气瓶中 。
小明在家中探究食用白醋的性质,选用了家庭生活中的下列常见物品:200ml的软透明塑料瓶、食品干燥剂、白醋、鸡蛋壳、紫罗兰花、锈铁钉、蒸馏水、纯碱、玻璃小杯。
【问 题】白醋是否具有酸类的性质?
【查阅资料】
(1)白醋为无色透明液体,其主要成分是醋酸,化学式可表示为HAc, Ac代表醋酸根;
(2)食品干燥剂的主要成分是氧化钙;
(3)紫罗兰花遇酸变为红色;
(4)醋酸盐中除银盐和汞盐外都易溶解于水。
【探究与验证】(请你帮助填写表中空白)
| 实验序号 |
实验操作 |
实验现象 |
实验结论 |
| 一 |
将白醋滴在紫罗兰花上 |
紫罗兰花变红 |
白醋的pH 7 |
| 二 |
将锈铁钉放在小玻璃杯中,加入白醋 |
刚开始时 ,一段时间后,有气泡冒出 |
1.白醋能与铁锈反应 2. |
| 三 |
向软塑料瓶中加入10ml白醋,将瓶捏扁,加入约5g鸡蛋壳,拧紧瓶盖 |
瓶中有气泡冒出,扁塑料瓶逐渐膨胀 |
白醋能与碳酸钙反应放出CO2 |
| 四 |
向白醋中加入纯碱 |
白醋中有 |
白醋能与碱反应 |
【反思与评价】
(1)小明将干燥剂袋口打开一段时间后,袋中的白色颗粒粘在了一起,请写出变化的化学方程式 。
(2)上面“实验结论”中,错误的是(填实验序号) 。
(3)上述实验三的现象还不足以得出表中所述的相应结论,为此还需要补充相应的实验,写出该实验发生反应的化学方程式 。
为了提高实验探究能力,振华中学的老师提供了一包白色粉末,它可能是碳酸钙、氢氧化钙两种物质中的一种或两种的混合物。
(1)为确定白色粉末的成分,实验时需要用到两种物质性质的不同是(试举一例):
。
(2)同学们设计了以下3种实验方案:
方案Ⅰ:取样加入试管中,滴加稀盐酸,有气泡产生,则白色粉末是碳酸钙。
方案Ⅱ:取样加入试管中,滴加稀盐酸,无气泡产生,则白色粉末是氢氧化钙。
方案Ⅲ:取样加入试管中,加水振荡,下层有不溶物,上层溶液中滴入酚酞试液,溶液变红,则白色粉末是碳酸钙和氢氧化钙的混合物。
以上三种方案中,你认为不合理的是 (填方案序号)。分析其表述现象,不合理的理由是 。
(3)请设计一种方案,证明该粉末为两种物质的混合物,简要写出实验操作及现象:
。
酒精灯灯焰分焰心、内焰和外焰三个部分。为探究灯焰温度,科研人员用特殊的测温装置进行实验,结果如下(探头位置是指测温探头离灯芯的垂直高度)。
| 火 焰 |
焰 心 |
内 焰 |
外 焰 |
||||
| 探头位置(cm) |
0.5 |
1.5 |
2.5 |
3.0 |
3.5 |
4.0 |
4.5 |
| 火焰温度(℃) |
537 |
670 |
775 |
806 |
801 |
750 |
667 |
| 平均温度(℃) |
603 |
794 |
708 |
(1)根据上表数据,灯焰三部分温度由低到高的顺序为________________。
(2)灯焰焰心温度较低,其原因是_________________________。
(3)实验中,若燃着的酒精灯中酒精不足,现要添加酒精,采取的操作是:先__________,再向酒精灯中添加酒精。
如图是某橙汁饮料标签上的部分内容.
(1) 除配料中涉及的营养物质外,人体必须的营养物质还有________________(写出一种即可)。
(2) 该饮料的pH____7 (填“>”、“<”或“二”).
(3) 如何检验一种无色溶液具有酸性?请设计实验方案(简要写出实验的步骤、现象及结论)
| 实验步骤 |
现象与结论 |
| |
|
已知在溶液中氢氧化钙和碳酸钠反应生成碳酸钙和氢氧化钠。现实验室有一瓶失去标签但密封保存良好的白色粉末,可能是碳酸钠,也可能是氧化钙或氢氧化钙。为确定其组成,某同学设计了以下实验方案进行探究,请你按要求帮助完成探究活动。
(1)提出假设:假设①白色粉末是碳酸钠;假设②白色粉末是氧化钙;假设③白色粉
末是氢氧化钙。
| 设计的相关实验操作 |
实验中观察到的现象 |
假设是否成立 |
| 取一定量粉末加入稀盐酸 |
没有气体产生 |
假设① |
| 取一定量粉末溶于水 |
溶液浑浊且温度升高 |
假设② |
| 假设③ |
(2)设计实验,通过实验分析进行判断并填空:
根据假设②的现象写出对应的化学方程式________________________________;
(3)实验后思考:假定这包白色粉末是混有少量氧化钙的碳酸钠粉末,将混合物溶于水可观察到的现象是_____________________________________________________;若将反应后的混合物进行固液分离,分离的方法是________;再将分离后的溶液蒸干,得到的固体物质是________、__________(填化学式)。
| 假设是否成立 |
| 否 |
| 是 |
| 否 |
以下是金属活动性探究实验的一部分。
① ② ③ ④ ⑤ ⑥ ⑦
实验甲:Mg、Zn、Fe、Cu分别 实验乙:金属与盐溶液的作用
与10%的盐酸反应
根据实验回答下列问题:
(1)实验甲判断金属活动性强弱的依据是_______________________________,得出的金属活动性强弱顺序为________________。
(2)实验乙得出的金属活动性顺序为_____________________。
(3)两组实验中不发生反应的是________(填试管的序号)。
(4)反思与评价:若实验甲中②④改用10%的稀硫酸,①③仍用10%的盐酸进行实验,能否保证得出同样准确的实验结论?__________;实验乙只需选择其中的2个就可以得出正确的实验结论,其中必须进行的一个实验是____(填试管的序号)。
试题篮
()