(某研究性学习小组在实验中发现:不仅碱溶液可以使酚酞溶液变红,Na2CO3溶液也能使酚酞溶液变红。碱溶液可以使酚酞溶液变红,是因为碱在水溶液中解离出了OH-,那么Na2CO3溶液中究竟是哪种粒子可以使酚酞溶液变红呢?他们设计了下图3个实验,请你和他们一起探究。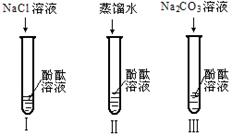
(1)实验Ⅰ可以证明 。
(2)实验Ⅱ加入蒸馏水的目的是 。小组内有同学认为实验Ⅱ没必要做,你认为他们的理由是 。
(3)实验Ⅲ滴入K2CO3溶液,振荡,酚酞溶液变红,向变红后的溶液中再逐渐滴入过量的CaCl2溶液,红色逐渐消失,同时还观察到 现象。由实验Ⅰ、Ⅱ、Ⅲ得出结论:CO32-可以使酚酞溶液变红。
(4)小组同学在与老师交流上述结论时,老师说:“其实Na2CO3溶液能使酚酞溶液变红也是由于溶液中存在OH-。”你认为Na2CO3溶液存在OH-的原因是 。
实验室中有一瓶标签受损的无色溶液,如图所示。
这瓶无色溶液中的溶质是什么呢? 化学兴趣小组的同学进行了探究。
实验员老师告诉大家,该溶液中的溶质只能是氧化钠、氯化钠、氢氧化钠、硫酸钠、碳酸钠中的一种。
(1)大家讨论后一致认为不可能是氧化钠,理由是 。
(2)为确定该溶液中溶质的成分,同学们继续进行实验探究,最终确定这瓶溶液中的溶质是氯化钠。请只用2种试剂完成实验并书写实验报告:
| 实验操作 |
预期现象和结论 |
| ① |
|
| ② |
|
碳酸钠、碳酸氢钠是中学常见的化合物。
探究一:碳酸钠、碳酸氢钠与酸反应
如图所示,将两气球内的NaHCO3和Na2CO3同时倒入试管中。已知盐酸足量,且装置气密性良好。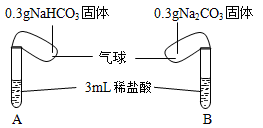
回答下列问题:
(1)碳酸钠俗名是 。
(2)实验过程中观察到的现象是: 。
(3)NaHCO3和Na2CO3都能与盐酸反应产生二氧化碳、水和氯化钠。任写出其中一个反应的化学方程式 。
(4)已知NaHCO3、Na2CO3的相对分子质量分别为84、106,通过计算:实验结束后, (填“A”或“B”)试管的气球更大。
探究二:碳酸氢钠、碳酸钠固体与酸反应的热效应
【发现问题】在探究一实验过程中用手触摸试管,发现盛NaHCO3的试管温度降低,而盛Na2CO3的试管温度升高。
【猜想与推测】甲同学由此推测:NaHCO3和盐酸反应为吸热反应,Na2CO3和盐酸反应为放热反应。
【实验与数据】乙同学认为甲同学推测不妥,通过以下多次实验后取平均值数据记录如下:
| 步骤① |
步骤② |
步骤③ |
步骤④ |
步骤⑤ |
| 测量10mL水温/℃ |
加入物质0.5 g |
溶解后测量溶液温度t1/℃ |
静置一段时间后测量溶液温度t2/℃ |
加入20%盐酸10 mL反应后测量溶液温度t3/℃ |
| 20 |
NaHCO3 |
18.5 |
20.0 |
20.8 |
| 20 |
Na2CO3 |
23.3 |
20.0 |
23.7 |
【分析与结论】
(1)由步骤①~③比较得到的结论是 。
(2)由步骤④~⑤比较得到的结论是: 。
(3)结合上面探究活动,你认为甲同学推测的不妥之处是 。
(13分)某校化学兴趣小组用下图装置探究铁生锈的条件。
(1)气体发生装置的选择
A装置用双氧水和二氧化锰制取氧气,为了控制反应速率,得到平稳的氧气流,应选择下图中的 (填“甲”、“乙”或“丙”)装置,该反应的化学方程式为 。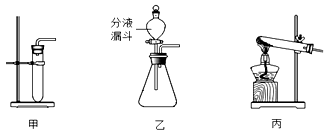
(2)铁生锈条件的探究
①上图C装置中浓硫酸的作用是 。
②打开K1、K2、K3,通入氧气,检验氧气已充满整个装置的方法是 。
关闭K1、K2、K3,2天后观察到:B处铁丝表面布满铁锈,D处铁丝依然光亮,E中铁丝表面有部分铁锈。
实验结论:铁生锈主要是铁与 和 发生反应。
③B、E处实验现象对比说明:影响铁生锈快慢的一种因素是 。
梧州市某中学化学兴趣小组的同学发现,熟鸡蛋在常温下放置一、两天后就会变臭了。富有营养而鲜美的鸡蛋,怎么会散发出臭味呢?同学们旋即对此进行了研究。
【提出问题】这种散发出刺激性臭味的无色气体是什么?它有怎样的性质?
【猜想假设】大家按照查阅到的鸡蛋中主要含有的元素是C、H、O、N、S的信息,及相应元素的化合价,列出了气体的可能存在形式分别有以下几组:
甲组—含碳化合物:CH4、CO、CO2
乙组—含氮化合物:NH3、NO、NO2
丙组—含硫化合物:SO2、SO3
虽然列出了上述可能,但大家都一致提议排除甲组的可能性,大家提出的理由是:__________________。
【查阅资料】
| 物质 |
NH3 |
NO |
NO2 |
SO2 |
SO3 |
| 一些特性 |
碱性 |
在空气中会迅速变成NO2 |
红棕色 |
酸性,有刺激性气味,能使KMnO4溶液褪色 |
沸点44.8℃ |
根据所查阅的资料,大家进一步排除了NO、NO2,理由是___________________;
也排除了SO3的可能,理由是_____________________________________________。
【实验验证】
毫无头绪的同学们向老师请教,老师笑而不语,拿出了两集气瓶的气体M,告诉大家这就是该刺激性臭味气体的主要成分,具有可燃性,至于还有什么性质,让大家在注意防护和试验安全的条件下进行探究。
(1)小吴同学用针筒抽取了部分气体M,注入盛有石蕊试液的试管中,结果没有看到溶液变_________的现象,证明该气体不是NH3;
(2)小周同学设法点燃了气体M,并拿一个干冷的小烧杯罩在火焰的上方,看到烧杯内壁有小水珠出现,说明了M气体中含有_______元素;燃烧后的气体带有刺激性,并能使另一个内壁沾有KMnO4溶液的小烧杯,出现红色褪去的现象,说明M气体中还含有_______元素。
(3)为了进一步探究M气体的组成,小施将3.4g的M气体完全燃烧后,设法将燃烧后所得气体,全部通入如下装置进行中。(注:碱石灰为固体NaOH和CaO的混合物)
经充分吸收后称重,发现A装置增重1.8g,C装置增重6.4g。通过计算可知,除了上述小周确定的两种元素外,M气体中________(填“含”或“不含”)其他元素;并确定了M的化学式为___________。而上图中B装置的作用是___________________;D装置的作用是__________________。经过严谨的思考与细致的实验,同学们终于揭开了这种气体的组成。
春节期间,小颖你妈妈去医院打点滴,发现护士往输液管上放了一个纸包,经询问得知它是输液恒温贴。可以温暖输入人体中的液体。小颖对包里的东西能产生热量感到很奇,于是,他向护士要了一只输液恒温贴,带回来进行了如下探究。
撕开真空包装封口,解开内衣包装袋,倒出其中的粉末,发现成黑色。
【提出问题】黑色粉末可能含有哪些物质呢?
【猜想与假设】该黑色粉末可能含有碳粉、铁粉、二氧化锰、氧化铜、四氧化三铁中的一种或几种。
【初步认证】将磁铁靠近黑色粉末,部分被吸引。
【查阅资料】四氧化三铁能被磁铁吸引。四氧化三铁与盐酸反应生成氯化亚铁,氯化铁和水
【初步结论】黑色粉末可能含有 。
【进行实验】
| 实验编号 |
实验操作 |
实验现象 |
| ① |
取少量黑色粉末于试管中,加足量稀硫酸 |
固体部分溶解,有气泡产生,溶液变为浅绿色, |
| ② |
将实验①试管中的物质过滤,向滤液中加入足量铁粉 |
有气泡产生,无红色物质析出 |
| ③ |
取实验②滤渣灼烧,将内壁涂有澄清石灰水的小烧杯罩在上方 |
澄清石灰水变浑浊 |
由上述实验可知,该黑色粉末肯定含有 ,肯定不含 ;写出实验①中产生气体的化学方程式 .
【交流讨论】
①输液恒温贴真空包装的原因:铁粉在空气中会与 发生缓慢氧化转化成铁锈
并放出热量。
②输液恒温贴中炭粉的作用是 。
氢化钙固体是登山运动员常用的能源提供剂。某探究小组的同学通过查阅资料得知,氢化钙(CaH2)与水反应生成氢氧化钙和氢气。
请写出该反应的化学方程式:
探究小组的同学把一定量的CaH2加入碳酸钠溶液中,充分反应后过滤,得到滤渣和滤液,经检验滤渣的成分是碳酸钙。
【提出问题】滤液中溶质的成分是什么?
【猜想与假设】猜想一:氢氧化钠、碳酸钠、氢氧化钙
猜想二:氢氧化钠、碳酸钠
猜想三:
猜想四:氢氧化钠
经过讨论,大家一致认为猜想 不合理,请用化学方程式说明原因:
【实验验证】
| 实验 |
现象 |
结论 |
| 实验一:取滤液,向其中滴入少量碳酸钠溶液 |
无明显现象 |
猜想 不成立 |
| 实验二:另取滤液,向其中加入足量稀盐酸 |
|
猜想二成立 |
【反思与拓展】
①若向氯化铵的浓溶液中加一定量CaH2,充分反应,产生的气体是 ;
②登山运动员常用CaH2作为能源提供剂,与氢气相比,其优点是 。
【定量分析】
探究小组的同学称取氢化钙样品的质量为10g,加入碳酸钠溶液中(假设氢化钙样品中的杂质不反应),充分反应后过滤、洗涤、烘干,得到滤渣质量为20g,试计算氢化钙样品中氢化钙的质量分数。(要求写出计算过程)
(8分)在一次用餐中,同学们对燃料“固体酒精”产生了好奇,于是对其成分进行研究.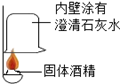 【查阅资料】(1)该固体酒精是用酒精、氯化钙和氢氧化钠按一定的质量比混合制成.
【查阅资料】(1)该固体酒精是用酒精、氯化钙和氢氧化钠按一定的质量比混合制成.
【提出问题】(1)酒精中是否含有碳元素?(2)固体酒精中的氢氧化钠是否变质?
【实验探究】
(1)按如图实验,发现澄清石灰水变浑浊,可得出酒精中含有碳元素的结论.此结论 (选填“合理”或“不合理”)
(2)取少量固体酒精于烧杯中,加足量的水充分溶解后静置,发现烧杯底部有白色沉淀.取沉淀于试管中加稀盐酸,有气泡产生.写出产生气体的化学方程式
分析实验并结合资料得出氢氧化钠已变质.
(3)为进一步确定氢氧化钠的变质程度,同学们设计了如下实验方案,请你一起完成下列实验报告.
| 实验操作 |
实验现象 |
实验结论 |
| (1)取少量样品溶于水,加入过量的 BaCl2溶液 |
|
该反应的化学方程式为 |
| (2)将上述反应后的混合液过滤,取滤液加入 ; |
|
固体酒精中的氢氧化钠部分变质 |
(4)【反思交流】判断实验操作(1)中所加BaCl2溶液是否过量的方法
(5)【拓展应用】要除去实验室部分变质的氢氧化钠溶液中的少量杂质,可选择适量的___(填字母)
A.Ba(OH)2溶液 B.CaCl2溶液 C.Ca(OH)2溶液
如图为用镀锌铁片制成的日常用品。镀锌铁是指通过镀锌工艺在铁皮上进行镀锌而制成的一种产品,热镀锌产品广泛用于建筑、家电、车船、容器制造业、机电业等,几乎涉及衣食住行各个领域。为测定铁片镀锌层的厚度实验过程如下。
【实验步骤】
(1)剪取一片镀锌铁片,量得长度=2.0 cm,宽度=l.9 cm。
(2)用电子天平称量质量0.857g。
(3)实验中需要溶质质量分数为10%的稀盐酸200 mL(密度=1.05g/mL),需要量取溶质质量分数为37%的浓盐酸(密度=1.18g/mL)____(保留至小数点后1位)mL,然后稀释。
(4)将镀锌铁片放入溶质质量分数为10%盐酸中。当观察到_______,可以判断镀锌层恰好反应。
(5)将溶液中的铁片取出清洗、擦干、烘干后用电子天平称量质量0.837g。
【计算结果】
(1)铁片镀锌层的质量有____g。
(2)已知锌的密度7.1g/cm3,计算出铁片镀锌层厚度mm。
【实验反思】
实际计算结果偏大,同学们分析,这是因为很难通过观察现象判断镀锌层恰好反应,造成镀锌铁片浸泡在盐酸中时间____(填“偏长”或“偏短”)。
【实验改进】
资料卡片:如图甲所示,两种金属活动性不同的金属放入酸、碱、盐溶液中,会有电子的流动,从而产生电流。
将上述实验改进成如图乙的装置,当观察到____,此时锌层恰好反应。
小红同学想探究实验室中碳酸钙和盐酸制取二氧化碳后废液中溶质的成分,请你一同参与探究并回答问题。
【提出问题】废液中的溶质是什么物质?
【作出猜想】小红认为废液中溶质只有CaCl2。
你认为还可能含有的溶质是 (填化学式)。
【查阅资料】CaCl2溶液呈中性。
【实验与结论】
(1)请你写出碳酸钙和盐酸反应的化学方程式 。
(2)分别取少量该废液和CaCl2溶液加入到两支试管中,并向其中分别滴入无色酚酞试液做对比试验,结果两支试管中溶液均无色,于是小红认为自己的猜想是正确的。
(3)你认为小红的实验 (填“能”或“不能”)证明她的猜想,理由是 。
(4)如果要证明你的猜想是正确的,你选择 。
(填字母:A、石蕊试液 B、氢氧化钠溶液 C、稀盐酸)来代替酚酞试液。
某兴趣小组在学习碱的化学性质时,进行了如图所示的实验。
实验后,同学们将三个实验的废液倒入同一废液缸中,最终看到废液浑浊并呈红色。
【提出问题】废液中含有哪些物质?
【交流讨论】(1)一定含有的物质:碳酸钙、指示剂、水和 。
(2)还含有能使废液呈碱性的物质。能使废液呈碱性的物质是什么?
猜想1:只有碳酸钠。
猜想2:只有氢氧化钙。
猜想3:是氢氧化钠和碳酸钠。
你的猜想:还可能是 。
【实验设计】小斌想用氯化钙溶液来验证他们的猜想。查阅资料获悉氯化钙溶液呈中性,并设计如下实验。请你将小斌的实验设计补充完整。
| 实验内容 |
预计现象 |
预计结论 |
| 取少量废液缸中上层清液于试管中,加入过量的氯化钙溶液,静置。 |
①有白色沉淀生成,溶液呈红色 |
猜想3正确。 |
| ② |
正确。 |
|
| ③ |
正确。 |
【反思拓展】
在分析化学反应后所得物质的成分时,除考虑生成物外还需考虑 。
氯气是自来水厂常用的消毒剂,某校化学兴趣小组的同学对它的性质很感兴趣,查阅下列有关资料并进行相关实验的探究:
【资料1】氯气的某些化学性质与氧气相似。
【猜想一】氯气有助燃性
【实验探究Ⅰ】点燃,把燃着的氢气放入装满氯气的集气瓶中,氢气能继续燃烧,生成一种有刺激性气味的无色气体,反应的化学方程式为: 。
由此可知【猜想一】 (填“成立”或“不成立”)
【资料2】氯气能与水发生化学反应:Cl2+ H2O = HCl + HClO。
其中次氯酸(HClO)中氯元素的化合价为 。
【猜想二】氯气可用于消毒是因为与水反应生成的盐酸,还是次氯酸(HClO)能消毒?
【资料3】某些物质能用于杀菌消毒是因为能分解出氧气。
某同学根据已有知识和阅读【资料3】后能够确定消毒的物质肯定不是 。
【实验探究Ⅱ】他将氯气通入装有适量水的试管中充分反应后,把试管放在阳光下照射,将带火星的木条伸入试管中时,发现木条能复燃。
【实验结论】氯气与水反应生成的 有杀菌消毒的作用
【拓展应用】次氯酸在水溶液中能离解为H+和ClO-,请问次氯酸能否与烧碱溶液发生中和反应?若能则写出相关的化学方程式 (若不能则可不写化学方程式.)
(7分)某化学兴趣小组的同学对碳酸钙高温加热一段时间剩余固体的成分进行探究。
【提出问题】剩余固体成分是什么?
【猜想与假设】剩余固体成分为:
A.全部是碳酸钙
B.既有碳酸钙也有氧化钙
C.全部是氧化钙
【设计并完成实验】
| 实验操作 |
实验现象 |
实验结论, |
| (1)取少量固体试管中,加适量水震荡后静置,再滴几滴无色酚酞溶液 |
溶液变红 |
说明固体成分中一定含有 |
| (2)再取少量固体另一试管中滴加过量稀盐酸 |
有气泡产生 |
说明固体成分中一定含有 |
【实验结论】该化学兴趣小组得出的结论是:剩余固体成分与【猜想与假设】中的 (填“A”或“B”或“C”)相符合。
【交流与反思】实验操作产生的气体是 ,剩余固体的成分若与C相符,则两步操作的实验现象与 (填“(1)”或“(2)”或“(1)(2)”)不同。写出操作(1)中发生反应的化学方程式 。
化学教师为了调动同学们探究的积极性,布置了一个探究任务:粉笔的成份是初中化学中常见的盐类,请同学们探究粉笔的化学成份。某化学兴趣小组进行了以下探究实验。
【提出猜想】
(1)粉笔的成份氯化物;(2)粉笔的成份碳酸盐;(3)粉笔的成份硫酸盐。
【实验探究】
(1)取一个段白色的粉笔(约1g),在研钵中研成粉末,倒入大烧杯中,加入100mL蒸馏水充分搅拌,静置,发现烧杯底部有较多的白色固体未溶解。根据下表以及后面实验操作现象,判断粉笔的成份属于哪类物质? 。
| 溶解度(20℃) |
﹤0.01g |
0.01g~1g |
1g~10g |
﹥10g |
| 物质分类 |
难溶 |
微溶 |
可溶 |
易溶 |
(2)从烧杯中取少许上层清液注入试管,滴加几滴酚酞,无明显现象。粉笔溶液(酸碱性)不可能呈 性;
(3)从烧杯中取少许上层清液注入试管,滴加盐酸溶液,无明显现象产生;
(4)从烧杯中取少许上层清液注入试管,滴加Na2CO3溶液,产生白色沉淀;
(5)从烧杯中取少许上层清液注入试管,滴加BaCl2溶液,产生白色沉淀。
【实验判断】
根据探究实验中出现的现象,请你做出粉笔化学成份可能合理的判断。完成下列填空:
(6)写出粉笔的主要成份化学式 ;
(7)写出【实验探究】(4)中化学反应的化学方程式 ;
(8)写出【实验探究】(5)中化学反应的化学方程式 。
某化学兴趣小组展示了他们设计的“火龙生字”创新实验,用硝酸钾的热饱和溶液先在白纸上书写“火”字,晾干后白纸上出现硝酸钾晶体如图所示。用带火星的木条接触硝酸钾晶体,立即有火花出现,并缓慢地沿着字的笔迹蔓延,最后呈现出“火”字的黑色痕迹(见下图)。现场的同学对此产生了浓厚的兴趣,随后进行了如下研究:
【提出问题】为什么附有硝酸钾的白纸更容易燃烧?
【查阅资料】硝酸钾不可燃烧,但受热易分解,生成亚硝酸钾(KNO2)和一种常见的气体单质。
【猜想与假设】对于产生的是什么气体,四位同学有如下猜测:
甲:二氧化氮; 乙:氮气; 丙:氧气; 丁:氢气;
丙同学首先排除了二氧化氮,理由是 ;同学认为也不可能是氢气,他的理由是 。
【进行实验】四位同学设计了实验对丙同学的猜想进行了验证,他们的操作方法是: ,观察到的现象是 ,说明丙同学的猜想正确,硝酸钾分解的化学方程式是 。
【解释与结论】白纸上写过字的地方更容易燃烧的原因是 。
【反思与评价】为什么要用“硝酸钾的热饱和溶液”书写文字?
已知硝酸钾在不同温度时的溶解度如下表:
你对上述问题的解释是 。
试题篮
()