某同学在验证次氯酸(
HClO)光照分解产物数字实验中,
HClO所发生反应的方程式为
2HClO 2HCl+O2,容器中
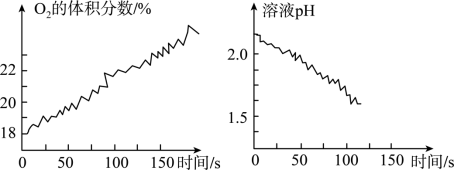
O2的体积分数的溶液的pH随时间变化的情况如图所示,下列说法错误的是( )
2HCl+O2,容器中
O2的体积分数的溶液的pH随时间变化的情况如图所示,下列说法错误的是( )
| A. |
光照前,容器内已有 O2 |
B. |
反应过程中,溶液的酸性不断增强 |
| C. |
反应前后氯元素的化合价不变 |
D. |
该实验说明 HClO化学性质不稳定 |
下列做法与目的不符的是( )
|
A |
鉴别空气与呼出气体 |
将燃着的小木条放入集气瓶中 |
|
B |
鉴别水和食盐水 |
观察颜色 |
|
C |
比较铝合金和铝硬度 |
相互刻画 |
|
D |
实验室制备纯净的水 |
蒸馏自来水 |
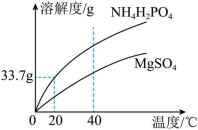
下图是亮亮看到的 NH4H2PO4和 MgSO4溶解度曲线,下列说法正确的是( )
| A. |
搅拌,可以使溶解度变大 |
| B. |
20℃时,在 100g水中加 33.7gNH4H2PO4形成不饱和溶液 |
| C. |
40℃时, NH4H2PO4的溶解度大于 MgSO4的溶解度 |
| D. |
NH4H2PO4溶液降温一定有晶体析出 |
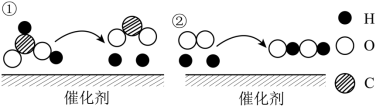
在通电条件下,甲酸与氧气的反应微观图如下,说法错误的是( )
| A. |
由此实验可知,分子是化学变化的最小粒子 |
| B. |
两个氢原子和一个氧分子结合形成 H2O2 |
| C. |
反应的化学方程式:
HCOOH+O2 |
| D. |
催化剂在反应前后的化学性质和质量不变 |
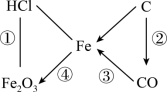
“—”表示物质可以发生反应,“→”表示物质可以转换,下列说法不正确的是( )
| A. |
①的现象是有气泡产生 |
B. |
②可用于碳的不完全燃烧 |
| C. |
③可用于工业炼铁 |
D. |
隔绝氧气或者水可以防止④的发生 |
下列日常生活与解释说明相符的是( )
|
日常生活 |
解释说明 |
|
|
A |
用铅笔写字 |
石墨具有导电性 |
|
B |
节约用电 |
亮亮同学践行低碳的生活理念 |
|
C |
用蜡烛照明 |
蜡烛燃烧生成 CO2和 H2O |
|
D |
晾晒湿衣服 |
水分子的质量和体积都很小 |
桃金娘烯醇 C10H16O是生物化工领域的一种产品,下列关于桃金娘烯醇说法正确的是( )
| A. |
桃金娘烯醇是氧化物 |
| B. |
桃金娘烯醇是由 10个碳原子, 16个氢原子, 1个氧原子构成的 |
| C. |
桃金娘烯醇中碳与氢质量比 5:8 |
| D. |
桃金娘烯醇中碳元素的质量分数最高 |
下列说法正确的是( )
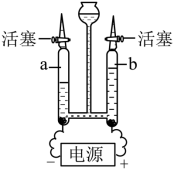
| A. |
a和 b质量比为 2:1 |
B. |
H2具有助燃性 |
| C. |
水是由氢元素和氧元素组成的 |
D. |
水的电解是物理变化 |
下列说法错误的是( )
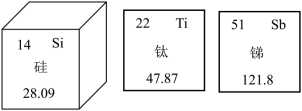
| A. |
这三种都是金属 |
B. |
硅的相对原子质量是 28.09 |
| C. |
钛的核外电子数为 22 |
D. |
锑的原子序数为 51 |
有关 NaOH说法错误的是( )
| A. |
NaOH固体溶解时放出热量 |
B. |
NaOH包装箱上张贴的标识是 |
| C. |
NaOH是所有气体的干燥剂 |
D. |
NaOH应密封保存 |
下列化学用语表达错误的是( )
| A. |
两个氦原子 2He |
B. |
氯离子: Cl+ |
| C. |
三氧化硫分子: SO3 |
D. |
碳酸钠: Na2CO3 |
化学和生活中资源,材料,生活,健康密切相关,下列说法正确的是( )
| A. |
深圳海洋资源丰富,可以随意开发 |
| B. |
生活中纯金属的使用一定比合金广 |
| C. |
为减少污染,应禁止使用化肥和农药 |
| D. |
为均衡膳食,应摄入合理均衡营养 |
羰基铁粉在国防军工领域有重要应用,我国是少数几个掌握其生产技术的国家之一。制备羰基铁粉的过程如图所示。

(1) Fe(CO)5中碳、氧元素的质量比为___________。
(2)反应1的化学方程式为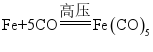 。用
100kg含铁
96%的海绵铁,理论上可制备
Fe(CO)5的质量是多少?(写出计算过程)
。用
100kg含铁
96%的海绵铁,理论上可制备
Fe(CO)5的质量是多少?(写出计算过程)
(3)反应2的化学方程式为 。
196kgFe(CO)5分解生成基铁粉的质量随时间的变化如下图所示。在
t1时,剩余 _____
kgFe(CO)5未分解;在___________时
Fe(CO)5恰好完全分解。
。
196kgFe(CO)5分解生成基铁粉的质量随时间的变化如下图所示。在
t1时,剩余 _____
kgFe(CO)5未分解;在___________时
Fe(CO)5恰好完全分解。
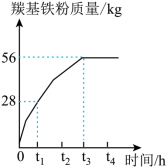
(4)制备羰基铁粉过程中循环利用的物质是______ 。
电解水制氢联合碳酸钙分解制备氧化钙,能减少碳排放,助力碳中和。该新方法的示意图如图所示。
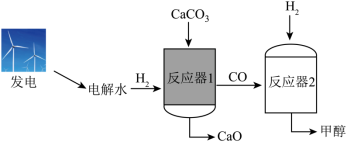
(1)传统方法: CaCO3在 900℃以上完全分解生成 CaO和__________(填化学式)。
(2)新方法:
i.电解水属于_____反应(填基本反应类型),反应前后氢元素的化合价_____(填“升高”“降低”或“不变”)。
ii.反应器1:一定的 H2环境及较低温度下 CaCO3可与 H2反应生成 CaO、CO和 H2O。 CO与 H2O的分子个数比为_______。
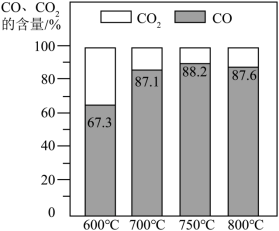
CaCO3还可以直接分解。反应器1中 CO、 CO2的含量随反应温度的变化如下图所示。________ ℃时,抑制 CO2生成的效果最好。
iii.反应器2:一定条件下, CO与 H2发生化合反应生成甲醇( CH3OH),化学方程式为_________ 。
(3)与传统方法相比,新方法的优点有__________________________(写两条)。
[科学探究]
耕地盐碱化影响粮食安全,盐碱地综合治理与利用可促进农业高质量发展,兴趣小组开展了与土壤盐碱化相关的探究活动。
(1)成因:由农业灌溉或化肥施用引起的土壤盐碱化如图所示,当进入土壤中盐的量超出植物的吸收能力时,随水分蒸发,__________导致土壤盐碱化。
(2)检测:配制土壤样品浸出液、用_______测定、若 pH>7、则浸出液显__________性。
(3)探究:某地土壤碱化可能由 Na2CO3、 Na2SO4中的一种两种引起。教师提供模拟盐碱化壤样品浸出液。
[查阅资料] BaCl2易溶于水; BaCO3为白色固体,难溶于水; BaSO4为白色固体,难溶于水和盐酸。
[提出问题]样品中的是什么?
[作出猜想]猜想1: Na2CO3
猜想2:_________
猜想3: Na2CO3和 Na2SO4
[实验探究]
(4)取少量出分别加管A、B中
|
实验序号 |
操作 |
现象 |
结论 |
|
1 |
向A中滴加少量 BaCl2溶液 |
产生白色沉淀 |
含 Na2SO4 |
|
2 |
向B中滴加过量稀盐酸 |
_______ |
含 Na2CO3 |
[分析评价]
(5)有同学认为实验1不够严谨,理由是______________(用化学方程式解释)
[补充实验]
(6)
|
实验序号 |
操作 |
现象 |
结论 |
|
3 |
向实验2反应后的溶液中滴加少量 BaCl2溶液 |
_______ |
猜想3成立 |
(7)交流:应对土壤盐碱化的合理措施有___________(多选,填字母)
| A. |
合理施肥 |
B. |
引海水灌溉 |
C. |
用熟石灰改良 |
D. |
种植耐盐碱作物 |
试题篮
()