某化学兴趣小组在实验室在利用废铜屑(含碳粉、铁屑、铁锈等)制取硫酸铜,实验流程如下:
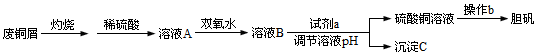
⑴废铜屑灼烧的目的是 。
⑵写出加入双氧水时发生反应的离子方程式 。
⑶试剂a可以是 ,溶液pH应控制在 范围之间。操作b的名称是 。
已知:
| 离子 |
开始沉淀时的pH |
完全沉淀时的pH |
| Fe2+ |
7.5 |
14 |
| Fe3+ |
1.4 |
3.7 |
| Cu2+ |
6.0 |
13 |
⑷在硫酸铜溶液中,各种离子浓度由大到小的顺序是 。向硫酸铜溶液中加入氨水,当Cu2+浓度小于2.2×10-4 mol·L-1时,溶液的pH至少是 。(已知Cu(OH)2的溶度积常数Ksp=2.2×10-20)
⑸工业上通常用FeS除去废水中的Cu2+,写出该沉淀转化离子方程式 。








 粤公网安备 44130202000953号
粤公网安备 44130202000953号