(15分) I.工业上用CO生产燃料甲醇。一定条件下发生反应:co(g)+2H2(g) CH3OH(g)。下图中甲图表示反应过程中能量的变化情况;乙图表示一定温度下,在体积为2L的密闭容器中加入4mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间的变化情况。
CH3OH(g)。下图中甲图表示反应过程中能量的变化情况;乙图表示一定温度下,在体积为2L的密闭容器中加入4mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间的变化情况。
请回答下列问题。
(1)下列说法正确的是 (填字母序号)。
a.在甲图中,曲线b表示使用了催化剂
b.起始充入的CO为2mol,从反应开始到达到平衡,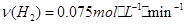
c.增大CO的浓度,CO的转化率增大
d.容器中压强恒定时,说明反应已达平衡状态
e.保持温度和密闭容器的容积不变,再充入1mol CO和2mol H2,再次达到平衡时 的值会变小
的值会变小
(2)该温度下CO(g)+2H2 (g)  CH3OH(g)的化学平衡常数为 。若保持其他条件不变,将反应体系升温,则该反应的化学平衡常数 (填“增大”“减小”或“不变”)。
CH3OH(g)的化学平衡常数为 。若保持其他条件不变,将反应体系升温,则该反应的化学平衡常数 (填“增大”“减小”或“不变”)。
(3)请在丙图所示坐标图中画出平衡时甲醇的百分含量(纵坐标)随温度(横坐标)的变化曲
线,要求画出压强不同的两条曲线(在曲线上标出P1、P2且P1<P2)。
(4)已知CH3OH(g)+3/2 O2(g)="===" C02(g)+2H2O(g) △H=-192.9kJ/mol,又知H20(1)=====H2O(g)
△H= +44kJ/mol,请写出32g CH3OH(g)完全燃烧生成CO2和液态水的热化学方程式
II.已知:在25℃时,H20 H+ + OH — Kw=10-14;
H+ + OH — Kw=10-14;
CH3COOH H+ + CH3COO — Ka=1.8×10-5 。
H+ + CH3COO — Ka=1.8×10-5 。
(5)醋酸钠水解的平衡常数Kh的表达式为
(6)0.5mol·L-1醋酸钠溶液的pH为m,其水解的程度(已水解的醋酸钠与原有醋酸钠的比值)为a;1mol·L-1醋酸钠溶液的pH为n,水解的程度为b。则a与b的关系为a b(填“大于”“小于”或“等于”)。
(7)0.9mol.L-1醋酸钠溶液中氢氧根离子的浓度为2.2×10-5mol·L-1 。在某溶液中含Mg2+、Cd2+ 、Zn2+ 三种离子的浓度均为0.01mol·L-1,向其中加入固体醋酸钠,使其浓度为0.9mol·L-1,则能生成的沉淀化学式为
已知:Ksp[ Mg(OH)2 ]=1.8×10-11、Ksp[ Zn(OH)2 ]=1.2×10-17 、Ksp [ Cd(OH)2 ]="2.5" x 10-14 。








 粤公网安备 44130202000953号
粤公网安备 44130202000953号